(1)硼酸(H3BO3)是一种白色固体,可溶于水,其水溶液为一元弱酸。硼酸分子中硼原子的杂化类型为______________ ;写出硼酸在水溶液中电离方程式 +H2O
+H2O
_______ 。
(2)CS2、NO2+具有相同的通式AX2,它们的价电子总数都是16。 CO32-、NO3-等微粒具有相同的通式:_______ ,它们的价电子总数是______________ ,因此它们与由第VIA族两元素组成的___________________ (填分子式)分子结构相同,呈______ 形。
(3)一个尿素[CO(NH2)2]分子中含有______ 个 键;1 mol化合物Fe(CO)5分子中所含
键;1 mol化合物Fe(CO)5分子中所含 键数目为
键数目为_________ 。
 +H2O
+H2O
(2)CS2、NO2+具有相同的通式AX2,它们的价电子总数都是16。 CO32-、NO3-等微粒具有相同的通式:
(3)一个尿素[CO(NH2)2]分子中含有
 键;1 mol化合物Fe(CO)5分子中所含
键;1 mol化合物Fe(CO)5分子中所含 键数目为
键数目为
更新时间:2017-10-25 10:51:40
|
【知识点】 物质结构与性质综合考查解读
相似题推荐
填空题
|
较难
(0.4)
【推荐1】我国科学家最近成功合成了世界上首个五氮阴离子盐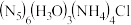 (用
(用 代表)。回答下列问题:
代表)。回答下列问题:
(1)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图(a)所示,其中除氮元素外,其他元素的
变化趋势如图(a)所示,其中除氮元素外,其他元素的 自左而右依次增大的原因是
自左而右依次增大的原因是__________ ;氮元素的 呈现异常的原因是
呈现异常的原因是_________ 。

(2)经 射线衍射测得化合物
射线衍射测得化合物 的晶体结构,其局部结构如图(b)所示。
的晶体结构,其局部结构如图(b)所示。
①从结构角度分析, 中两种阳离子的相同之处为
中两种阳离子的相同之处为__________ ,不同之处为__________ 。(填标号)
A 中心原子的杂化轨道类型 B 中心原子的价层电子对数
C 立体结构 D 共价键类型
② 中阴离子
中阴离子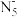 中的键总数为
中的键总数为__________ 个。分子中的大 键可用符号表示
键可用符号表示 ,其中
,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 )则
)则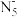 中的大
中的大 键应表示为
键应表示为__________ 。
③图(b)中虚线代表氢键,其表示式为 、
、__________ 、__________ 。
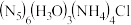 (用
(用 代表)。回答下列问题:
代表)。回答下列问题:(1)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图(a)所示,其中除氮元素外,其他元素的
变化趋势如图(a)所示,其中除氮元素外,其他元素的 自左而右依次增大的原因是
自左而右依次增大的原因是 呈现异常的原因是
呈现异常的原因是
(2)经
 射线衍射测得化合物
射线衍射测得化合物 的晶体结构,其局部结构如图(b)所示。
的晶体结构,其局部结构如图(b)所示。①从结构角度分析,
 中两种阳离子的相同之处为
中两种阳离子的相同之处为A 中心原子的杂化轨道类型 B 中心原子的价层电子对数
C 立体结构 D 共价键类型
②
 中阴离子
中阴离子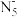 中的键总数为
中的键总数为 键可用符号表示
键可用符号表示 ,其中
,其中 代表参与形成大
代表参与形成大 键的原子数,
键的原子数, 代表参与形成大
代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 )则
)则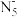 中的大
中的大 键应表示为
键应表示为③图(b)中虚线代表氢键,其表示式为
 、
、
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】(1)基态Fe2+的核外电子排布式为_________________________________ 。
(2)元素的第三电离能I3:Fe______ Mn(填“>”或:“<”)。
(3)H2O的沸点比H2S高的原因是_______________________________________ 。
(4)亚西尔•阿拉法特的死因被怀疑是钋—210中毒。钋与氧同族,基态钋原子有________ 个未成对电子。钋沉积在铍(9Be)上用作原子弹的中子源。铍的氯化物BeCl2室温下为雪白色易升华的固体,能溶于水和部分有机溶剂。室温下BeCl2固体属于__________ 晶体,500-600°C时,氯化铍以二聚体的形式存在,其二聚体的结构式为__________________ (配位键用“→”表示)。
(5)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:

①在Xm-中,数字标号为4的硼原子的轨道杂化类型为___________ ;m=_______ 填数字)。
②若硼砂的式量为382 , 则其化学式为______________ 。
(2)元素的第三电离能I3:Fe
(3)H2O的沸点比H2S高的原因是
(4)亚西尔•阿拉法特的死因被怀疑是钋—210中毒。钋与氧同族,基态钋原子有
(5)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:

①在Xm-中,数字标号为4的硼原子的轨道杂化类型为
②若硼砂的式量为382 , 则其化学式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】已知A、B、C、D、E五种元素的原子序数依次增大,A元素位于周期表的s区,其原子中电子层数等于未成对电子数;B的基态原子中电子占据三种能量不同的原子轨道,且每种原子轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体;A、B两种元素组成的原子个数之比为1∶1的化合物N是常见的有机溶剂;E有“生物金属”之称,E4+和氩原子的核外电子排布相同。
(1)E的基态原子的价电子排布图为______ 。
(2)B、C、D三种元素的氢化物的沸点高低顺序为__________ (用化学式表示,下同),稳定性顺序为__________ 。
(3)化合物M是同类物质中为数不多的气体,且分子中所有原子共平面,则M中σ键和π键个数比为____ ,B原子的杂化类型为____ ,M能和水以任意比混溶的原因是______________ 。
(4)E的一种氧化物Q,其晶胞结构如图1所示,则Q的化学式为____ 。

(5)电镀厂排放的废水中常含有剧毒的BC-,可在Q的催化下,先用NaClO将BC-氧化成BCD-,然后在酸性条件下BCD-可以继续被NaClO氧化成C2和BD2。
①与BCD-互为等电子体的分子是____ (写出一种即可);可以推知BCD-的空间构型为__ 。
②上述反应中后一步反应的离子方程式为_____________ 。
(6)E内部原子的堆积方式与铜相同,都是面心立方堆积方式,如图2所示,则E晶胞中E的配位数为____ ,若该晶胞的密度为a g·cm-3,阿伏伽德罗常数为NA,E原子的摩尔质量为M g·mol-1,则E原子的半径为____ cm。
(1)E的基态原子的价电子排布图为
(2)B、C、D三种元素的氢化物的沸点高低顺序为
(3)化合物M是同类物质中为数不多的气体,且分子中所有原子共平面,则M中σ键和π键个数比为
(4)E的一种氧化物Q,其晶胞结构如图1所示,则Q的化学式为

(5)电镀厂排放的废水中常含有剧毒的BC-,可在Q的催化下,先用NaClO将BC-氧化成BCD-,然后在酸性条件下BCD-可以继续被NaClO氧化成C2和BD2。
①与BCD-互为等电子体的分子是
②上述反应中后一步反应的离子方程式为
(6)E内部原子的堆积方式与铜相同,都是面心立方堆积方式,如图2所示,则E晶胞中E的配位数为
您最近一年使用:0次



