某浓度的硝酸与过量铁粉反应,生成4.48L N2O气体(标准状况)。如改与铝反应(生成NO气体),则最后可溶解铝的量是( )
| A.27g | B.9g | C.13.5g | D.8.9mol |
更新时间:2017-11-02 20:22:00
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室中利用洁净的铜片和浓硫酸进行如图实验,经检测,所得固体中含有Cu2S和白色物质X,下列说法错误的是
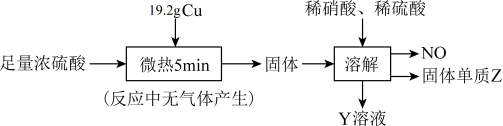

| A.白色物质X为CuSO4 |
| B.微热5min待Cu反应结束后,转移电子的物质的量为0.48mol |
| C.放出的NO在标准状况下的体积为0.896L |
| D.向Y溶液中逐滴加入过量的氨水,先产生蓝色沉淀,后沉淀溶解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学进行有关铜、硝酸、硫酸化学性质的实验,实验过程如图所示:
下列说法正确的是
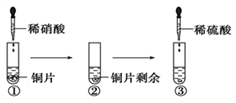
下列说法正确的是
| A.①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO2 |
| B.②中溶液存在:c(Cu2+) + c(H+) = c(NO3-) + c(OH-) |
| C.由上述实验得出结论:常温下,Cu既可与稀硝酸反应,也可与稀硫酸反应 |
| D.③中反应的化学方程式:3Cu+Cu(NO3)2+4H2SO4 === 4CuSO4 +2NO↑+4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】1.52 g铜镁合金完全溶解于50 mL密度为1.40 g·cm-3、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体物质的量为0.05 mol,向反应后的溶液中加入1.0 mol·L-1 NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )
| A.该合金中铜与镁的物质的量之比是1∶2 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol·L-1 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL |
您最近一年使用:0次



