由N、B等元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅的制造;由第二周期元素组成的与BCl3互为等电子体的阴离子为_________ (填离子符号,填一个)。
(2)氨硼烷(H3N→BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料.
①H3N→BH3中B原子的轨道杂化类型为___________ 。
②Ti(BH4)3由TiCl3和LiBH4反应制得,写出该制备反应的化学方程式_________________ ;基态Ti3+的未成对电子数有___ 个,BH4-的立体构型是________ ;其中所含化学键的类型有________ ;
③氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:
3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3
与上述化学方程式有关的叙述不正确的是_________ 。
A.氨硼烷中存在配位键
B.第一电离能:N>O>C>B
C.反应前后碳原子的轨道杂化类型不变
D.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
(3)磷化硼(BP)是受到高度关注的耐磨材料,如图1为磷化硼晶胞;
①磷化硼晶体属于______ 晶体;晶体中是否含有配位键:_______ 。
②晶体中B原子的配位数为____ 。
(4)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其结构和硬度都与金刚石相似,但熔点比金刚石低,原因是___________________ 。图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置____ 。其中“●”代表B原子,“×”代表N原子。

(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅的制造;由第二周期元素组成的与BCl3互为等电子体的阴离子为
(2)氨硼烷(H3N→BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料.
①H3N→BH3中B原子的轨道杂化类型为
②Ti(BH4)3由TiCl3和LiBH4反应制得,写出该制备反应的化学方程式
③氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:
3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3
与上述化学方程式有关的叙述不正确的是
A.氨硼烷中存在配位键
B.第一电离能:N>O>C>B
C.反应前后碳原子的轨道杂化类型不变
D.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
(3)磷化硼(BP)是受到高度关注的耐磨材料,如图1为磷化硼晶胞;
①磷化硼晶体属于
②晶体中B原子的配位数为
(4)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其结构和硬度都与金刚石相似,但熔点比金刚石低,原因是

更新时间:2017-11-20 20:34:24
|
【知识点】 物质结构与性质综合考查解读
相似题推荐
填空题
|
较难
(0.4)
【推荐1】(1)Br位于元素周期表第_____ 周期第_____ 族;基态Na+核外有_____ 种运动状态不同的电子;Mg基态原子核外电子排布式为_____ 。
(2)用“>”或“<”填空:
(3)已知多硫化钠﹣溴储能电池是一种二次电池,结构如图。电池总反应为:2Na2S3+2NaBr 3Na2S2+Br2。
3Na2S2+Br2。
①放电时Na+向_____ 极迁移(填“a 或 b”);
②充电时阴极电极反应式为:______________ 。
(4)已知N4为正四面体结构,N﹣N键能为167kJ/mol,N≡N 键能为 942kJ/mol。写 出N4(g)转化为N2(g)的热化学方程式________________ 。
(2)用“>”或“<”填空:
| 第一电离能 | 粒子半径 | 熔点 | 键的极性 |
| N | S2— | SO3 | H﹣O |
(3)已知多硫化钠﹣溴储能电池是一种二次电池,结构如图。电池总反应为:2Na2S3+2NaBr
 3Na2S2+Br2。
3Na2S2+Br2。
①放电时Na+向
②充电时阴极电极反应式为:
(4)已知N4为正四面体结构,N﹣N键能为167kJ/mol,N≡N 键能为 942kJ/mol。写 出N4(g)转化为N2(g)的热化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】C60、金刚石、石墨、二氧化碳和氯化铯的结构模型如图所示(石墨仅表示出其中的一层结构):

(1)C60、金刚石和石墨三者的关系是互为____ 。
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2)固态时,C60属于____ (填“原子”或“分子”)晶体,C60分子中含有双键的数目是____ 。
(3)晶体硅的结构跟金刚石相似,1 mol晶体硅中含有硅—硅单键的数目约是____ NA。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是____ 。
(5)观察CO2分子晶体结构的一部分,试说明每个CO2分子周围有____ 个与之紧邻且等距的CO2分子;该结构单元平均占有____ 个CO2分子。
(6)观察图形推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为___ ,每个Cs+周围距离相等且次近的Cs+数目为___ ,距离为___ ,每个Cs+周围距离相等且第三近的Cs+数目为____ ,距离为____ ,每个Cs+周围紧邻且等距的Cl-数目为___ 。

(1)C60、金刚石和石墨三者的关系是互为
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2)固态时,C60属于
(3)晶体硅的结构跟金刚石相似,1 mol晶体硅中含有硅—硅单键的数目约是
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是
(5)观察CO2分子晶体结构的一部分,试说明每个CO2分子周围有
(6)观察图形推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是________ (填元素符号),其中C原子的核外电子排布式为__________________ 。
(2)单质A有两种同素异形体,其中沸点高的是______ (填分子式),原因是__________________________________________ ;A和B的氢化物所属的晶体类型分别为________ 和________ 。
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为______________ ,中心原子的杂化轨道类型为________ 。
(4)化合物D2A的立体构型为________ ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_______________________________________________ 。
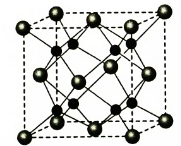
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566 nm,F的化学式为________ ;晶体F的密度(g·cm-3 )________________________________ 。(列出表达式)
(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为
(4)化合物D2A的立体构型为
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566 nm,F的化学式为

您最近一年使用:0次



