对于下列物质:①HNO3②CH4 ③NH4HSO4 ④Ba(OH)2 ⑤SO3⑥NaCl溶液⑦熔融的Al2(SO4)3⑧铜,请用序号作答:
(1)属于电解质的是____________ ,属于非电解质的是________________ ,能导电的是________________ 。
(2)将④的溶液滴加到①的溶液中的离子方程式______________________________ 。
(3)⑦溶于水的电离方程式__________ 。
(1)属于电解质的是
(2)将④的溶液滴加到①的溶液中的离子方程式
(3)⑦溶于水的电离方程式
更新时间:2017-12-13 10:41:59
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩矿泉水
请回答下列问题:
(1)以上物质中属于混合物的是___________ (填序号),以上物质中属于电解质的是___________ (填序号);以上纯净物中能导电的是___________ (填序号)。
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是___________
(3)写出⑧在水溶液中的电离方程式___________ 。
(4)在含40g溶质的①溶液中缓缓通入标准状况下66g CO2,则反应后溶液的溶质有___________ (填化学式)。
请回答下列问题:
(1)以上物质中属于混合物的是
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是
(3)写出⑧在水溶液中的电离方程式
(4)在含40g溶质的①溶液中缓缓通入标准状况下66g CO2,则反应后溶液的溶质有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列10种物质:①铝,②纯醋酸,③CO2,④硫酸,⑤Ba(OH)2固体,⑥熔融的氧化钠,⑦稀盐酸,⑧NaHSO4固体,⑨碳酸钙,⑩乙醇。
(1)上述物质中能导电的是____ ,非电解质有____ (填序号)。
(2)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为____ 。
(3)⑨和⑦混合,反应的离子方程式为____ 。
(4)②溶于水时电离方程式为____ 。
(1)上述物质中能导电的是
(2)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为
(3)⑨和⑦混合,反应的离子方程式为
(4)②溶于水时电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)有以下几种物质①干燥的食盐晶体 ②液态氯化氢 ③Cu ④蔗糖 ⑤NH3 ⑥KNO3溶液 ⑦CO2 ⑧熔融的KCl ⑨石墨。填空回答(填序号):以上物质中能导电的是______________ ;属于电解质的是__________ ;属于非电解质的是______________ ;
(2)用“双线桥”表示出反应中电子转移的方向和数目:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O_______
(3)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为________________ 。
(2)用“双线桥”表示出反应中电子转移的方向和数目:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(3)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】写出下列物质的电离方程式:
(1)Ba(OH)2_________________________________________________
(2)NaHCO3_________________________________________________
(3)NaHSO4___________________________________________________
(4)NH4NO3__________________________________________________
(1)Ba(OH)2
(2)NaHCO3
(3)NaHSO4
(4)NH4NO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】以下几种物质为中学化学中常见的物质,请用序号填空:
①氢氧化钠固体②铜丝③氯化氢气体④稀硫酸⑤二氧化碳气体⑥氨水⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩NaHSO4固体
(1)上述状态下可导电的是_______ 。
(2)属于电解质的是_______ 。
(3)上述状态下的电解质不能导电的是_______ 。
(4)写出③⑩在水溶液中的电离方程式:
③_______ ;
⑩_______ ;
①氢氧化钠固体②铜丝③氯化氢气体④稀硫酸⑤二氧化碳气体⑥氨水⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩NaHSO4固体
(1)上述状态下可导电的是
(2)属于电解质的是
(3)上述状态下的电解质不能导电的是
(4)写出③⑩在水溶液中的电离方程式:
③
⑩
您最近一年使用:0次
【推荐1】如下图为铁及其化合物的“价一类"二维图。
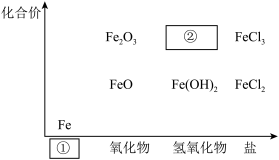
(1)填写二维图缺失的类别①______ 和化学式②______ 。
(2)某同学利用以下试剂(①Cl2②Fe③NaOH④H2SO4⑤AgNO3)
研究FeCl3性质、进行了如下预测:
从物质类别上看,FeCl3属于______ ,可能与______ 发生复分解反应(填上述试剂对应的序号)。
从化合价角度看,Fe3+具有______ 性,可能与______ 发生氧化还原反应(填上述试剂对应的序号)。
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应: Cu+2FeCl3=CuCl2+2FeCl2该反应的离子方程式为______ 。
(4)为了探究Fe2+、Cu2+、Ag+的氧化性强弱,设计实验如图所示。请回答:

实验Ⅰ、Ⅱ的现象和结论如下表:
①实验Ⅰ的现象为______ 。
②实验Ⅱ的结论为______ 。
③实验Ⅱ中的AgNO3完全反应后,抽出铜丝,洗净后干燥、称重,发现铜丝比反应前增重7.6g,则反应转移的电子为______ mol。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂(①Cl2②Fe③NaOH④H2SO4⑤AgNO3)
研究FeCl3性质、进行了如下预测:
从物质类别上看,FeCl3属于
从化合价角度看,Fe3+具有
(3)某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应: Cu+2FeCl3=CuCl2+2FeCl2该反应的离子方程式为
(4)为了探究Fe2+、Cu2+、Ag+的氧化性强弱,设计实验如图所示。请回答:

实验Ⅰ、Ⅱ的现象和结论如下表:
| 实验编号 | 实验现象 | 实验结论 |
| Ⅰ | ① | 氧化性:Cu2+>Fe2+ |
| Ⅱ | 溶液变蓝色 | ② |
②实验Ⅱ的结论为
③实验Ⅱ中的AgNO3完全反应后,抽出铜丝,洗净后干燥、称重,发现铜丝比反应前增重7.6g,则反应转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请写出下列反应的化学方程式或离子方程式:
(1)过量二氧化碳通入偏铝酸钠溶液的离子方程式:______________ ;
(2)向氯化铝溶液中加入过量的氢氧化钠溶液的离子方程式:__________ ;
(3)浓硝酸见光分解的化学方程式:__________ ;
(4)氨的催化氧化的化学方程式:______________ 。
(1)过量二氧化碳通入偏铝酸钠溶液的离子方程式:
(2)向氯化铝溶液中加入过量的氢氧化钠溶液的离子方程式:
(3)浓硝酸见光分解的化学方程式:
(4)氨的催化氧化的化学方程式:
您最近一年使用:0次

 =H2O+CO2↑
=H2O+CO2↑ +Ba2+=BaSO4↓
+Ba2+=BaSO4↓

