请根据物质在生产、生活等方面的应用填空:
(1)厨房里常使用小苏打,向其水溶液中滴加酚酞溶液后,溶液呈_______ (填“无”或“浅红”)色;
(2)检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用_______ (填“KSCN”或“H2SO4”)溶液;
(3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装_______ (填“浓硫酸”或“浓盐酸”)。
(1)厨房里常使用小苏打,向其水溶液中滴加酚酞溶液后,溶液呈
(2)检验某补铁剂中的Fe2+是否被氧化成Fe3+,可用
(3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装
更新时间:2017-12-04 10:59:56
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】补齐物质及其用途的连线。___________

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】补齐物质与其用途的连线,并回答问题。
物质 用途
A.漂粉精 a.焙制糕点
B.碳酸氢钠 b.游泳池消毒
C.过氧化钠 c.呼吸面具供氧
(1)补齐上图连线___________ 。
(2)上述漂粉精的用途,利用了它的___________ (填“物理”或“化学”)性质。
(3)过氧化钠可以用于呼吸面具供氧,用化学方程式解释其原因:___________ 、___________ 。
物质 用途
A.漂粉精 a.焙制糕点
B.碳酸氢钠 b.游泳池消毒
C.过氧化钠 c.呼吸面具供氧
(1)补齐上图连线
(2)上述漂粉精的用途,利用了它的
(3)过氧化钠可以用于呼吸面具供氧,用化学方程式解释其原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】硝酸的化学性质
(1)酸的通性
写出下列反应的离子方程式:
①硝酸和氢氧化钠反应:_________________________ 。
②硝酸和氧化钠反应:_________________________ 。
③硝酸和碳酸钙反应:_________________________ 。
(2)不稳定性:见光或受热易分解,化学方程式为_________________________________ 。
长期存放的浓硝酸呈黄色是因为其分解生成的____ 溶于硝酸中,实验室常将浓硝酸保存在____ 试剂瓶中,并放在____ 处。
(3)强氧化性
①和金属(Cu)反应的实验探究
写出上述反应的化学方程式:_________ ;_________ 。
②与Fe、Al反应
常温下浓硝酸可使铁、铝表面形成致密的氧化膜而____ ,保护内部金属不再与酸反应,所以可以用____ 制容器或____ 制容器盛放浓硝酸。加热时,铁、铝可以与浓硝酸反应。
③与非金属反应
写出碳与浓硝酸在加热时反应的化学方程式:____ 。
(1)酸的通性
写出下列反应的离子方程式:
①硝酸和氢氧化钠反应:
②硝酸和氧化钠反应:
③硝酸和碳酸钙反应:
(2)不稳定性:见光或受热易分解,化学方程式为
长期存放的浓硝酸呈黄色是因为其分解生成的
(3)强氧化性
①和金属(Cu)反应的实验探究
| 实验操作 |  两支试管中分别加入2 mL浓硝酸和稀硝酸 |
| 实验现象 | 浓硝酸反应比较 |
| 实验结论 | 硝酸无论浓、稀都有 |
写出上述反应的化学方程式:
②与Fe、Al反应
常温下浓硝酸可使铁、铝表面形成致密的氧化膜而
③与非金属反应
写出碳与浓硝酸在加热时反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氨及其化合物在工业生产中占有重要地位。回答下列问题:
(1)常温下, 是
是___________ (填“无色”或“红棕色”)气体。
(2)常温下,若将一片洁净的铝片置于浓 中,铝片不会溶解,该过程中
中,铝片不会溶解,该过程中___________ (填“发生化学反应”或“不发生化学反应”)。
(3)将氨气催化氧化的化学方程式补充完整:__________ ;
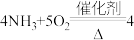 ___________
___________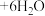 。
。
(1)常温下,
 是
是(2)常温下,若将一片洁净的铝片置于浓
 中,铝片不会溶解,该过程中
中,铝片不会溶解,该过程中(3)将氨气催化氧化的化学方程式补充完整:
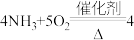 ___________
___________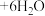 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】铜、铁、铝是应用最广泛的三种金属。
(1)它们在人类的金属使用历史中,由早到晚的顺序为__________________________ 。
(2)日常常用“铝壶”烧开水,是因为铝有良好的导热性、__________________________ 。
(3)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。写出反应的化学方程式________________________________________________ ,该反应是_______ (填:吸或放)热反应,其中铝发生________ (填:氧化或还原)反应。
(4)表面破损的铝制品,放久了破损处会有一层“白毛”产生,“白毛”既能溶于酸又能溶于碱溶液,写出形成“白毛”的化学方程式_____________________________ 。
(1)它们在人类的金属使用历史中,由早到晚的顺序为
(2)日常常用“铝壶”烧开水,是因为铝有良好的导热性、
(3)野外铺设钢轨时,通常用铝和氧化铁混合粉末反应得到的液态铁来焊接钢轨。写出反应的化学方程式
(4)表面破损的铝制品,放久了破损处会有一层“白毛”产生,“白毛”既能溶于酸又能溶于碱溶液,写出形成“白毛”的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】健康人体内含铁元素大约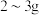 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:

(1)试剂1的名称是___________ ;试剂2的化学式为___________ 。
(2)加入新制氯水,溶液中发生反应的离子方程式是___________ 。
(3)加入试剂2时溶液为淡红色说明“速力非”中的 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有___________ 性。
(4)不仅溶液中 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:___________ ,现象为___________ 。
(5) 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入___________ ,防止 被氧化。
被氧化。
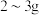 ,人体内铁元素以亚铁离子和三价铁离子的形式存在,
,人体内铁元素以亚铁离子和三价铁离子的形式存在, 易被吸收,所以给贫血者补充铁元素时,应补充含
易被吸收,所以给贫血者补充铁元素时,应补充含 的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中
的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中 的存在,设计并进行了如图实验:
的存在,设计并进行了如图实验:
(1)试剂1的名称是
(2)加入新制氯水,溶液中发生反应的离子方程式是
(3)加入试剂2时溶液为淡红色说明“速力非”中的
 已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有
已被部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有(4)不仅溶液中
 易被氧化成
易被氧化成 ,溶液中白色沉淀
,溶液中白色沉淀 更易被
更易被 氧化,请写出反应的化学方程式:
氧化,请写出反应的化学方程式:(5)
 溶液存放时应在试剂瓶中加入
溶液存放时应在试剂瓶中加入 被氧化。
被氧化。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】铬及其化合物有许多独特的性质和用途。如炼钢时加入一定量的铬可得到不锈钢, 是实验中常用的强氧化剂之一,从含有铬、锌、钢、铁、镉(Cd)、钴(Co)等单质的工业废料回收铬的生产流程如图:
是实验中常用的强氧化剂之一,从含有铬、锌、钢、铁、镉(Cd)、钴(Co)等单质的工业废料回收铬的生产流程如图:

几种金属离子生成氢氧化物沉淀的 见表:
见表:
请回答下列问题:
(1)写出提高酸浸速率的措施_______ (写出两点)。
(2)酸浸时形成的金属离子的价态均相同,料渣中含有大量的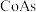 合金,写出除钴时反应的离子方程式
合金,写出除钴时反应的离子方程式_______ 。
(3)若仅从试剂的经济角度考虑,试剂X最好是_______ ,如果试剂X是 ,请写出其氧化
,请写出其氧化 的离子反应方程式
的离子反应方程式_______ 。
(4)已知氧化过程中铁、铬形成的离子均被完全氧化,则调 时应将
时应将 控制在
控制在_______ 范围内,单质铬与试剂Y反应时,反应中二者消耗量
_______ 。
(5)设计实验检验废液中是否含有 :
:_______ 。
 是实验中常用的强氧化剂之一,从含有铬、锌、钢、铁、镉(Cd)、钴(Co)等单质的工业废料回收铬的生产流程如图:
是实验中常用的强氧化剂之一,从含有铬、锌、钢、铁、镉(Cd)、钴(Co)等单质的工业废料回收铬的生产流程如图:
几种金属离子生成氢氧化物沉淀的
 见表:
见表:| 氢氧化物 |  |  | 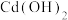 |  |
开始沉淀的 | 1.5 | 8 | 7.2 | 6 |
沉淀完全的 | 3.3 | 12 | 9.5 | 8 |
(1)写出提高酸浸速率的措施
(2)酸浸时形成的金属离子的价态均相同,料渣中含有大量的
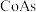 合金,写出除钴时反应的离子方程式
合金,写出除钴时反应的离子方程式(3)若仅从试剂的经济角度考虑,试剂X最好是
 ,请写出其氧化
,请写出其氧化 的离子反应方程式
的离子反应方程式(4)已知氧化过程中铁、铬形成的离子均被完全氧化,则调
 时应将
时应将 控制在
控制在
(5)设计实验检验废液中是否含有
 :
:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题:
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为____ ,反应后得到的溶液呈____ 色。用此溶液进行以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为_____ 。
(3)另取少量原溶液于试管中,滴入KSCN溶液,则溶液呈____ 色,离子方程式为____ 。
(4)另取少量原溶液于试管中加入足量的铁粉,溶液变为浅绿色,取浅绿色溶液于试管中,加入NaOH溶液得到白色沉淀,露置在空气中所观察到的现象为____ ,产生该现象的化学方程式为____ 。
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式为
(2)取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀生成,反应的离子方程式为
(3)另取少量原溶液于试管中,滴入KSCN溶液,则溶液呈
(4)另取少量原溶液于试管中加入足量的铁粉,溶液变为浅绿色,取浅绿色溶液于试管中,加入NaOH溶液得到白色沉淀,露置在空气中所观察到的现象为
您最近一年使用:0次





