某无色溶液放入铝片后有氢气产生,在该溶液中下列离子一定可以大量存在的是( )
| A.HCO3— | B.Mg2+ | C.Cl- | D.CO32— |
更新时间:2018-01-07 19:21:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列各组离子混合,最终一定有白色沉淀生成的是
A.Cu2+、Na+、 、OH- 、OH- | B.Ca2+、H+、 、 、 |
C. 、Mg2+、 、Mg2+、 、 、 | D.Na+、Ag+、Cl-、H+ |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色透明的溶液中:OH-、Na+、CrO 、SO 、SO |
B.c(S2O )=0.1mol·L-1的溶液中:Na+、K+、CO )=0.1mol·L-1的溶液中:Na+、K+、CO 、SO 、SO |
C.水电离出的c(H+)=1.0×10-13mol·L-1的溶液中:Na+、Mg2+、HSO 、NO 、NO |
D.能使蓝色石蕊试纸变红的溶液中:Na+、NH 、 、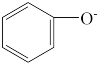 、Cl- 、Cl- |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】两份铝,一份加入足量强碱溶液中,另一份加入足量盐酸中,要使前后反应收集到的氢气量之比为1︰2,则两份铝质量比为
| A.1︰2 | B.2︰1 | C.1︰4 | D.1︰1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用相同的铝片、6 mol·L-1稀盐酸、3 mol·L-1稀硫酸、6 mol·L-1氢氧化钠溶液、试管等分别进行下表实验:
对上述实验的相关说法不正确 的是
| 实验方案 | 实验现象 | 实验原理(化学方程式) |
| (1)铝片与足量盐酸反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大量气泡产生 | Al2O3+6HCl=2AlCl3+3H2O 2Al+6HCl=2AlCl3+3H2↑ |
| (2)铝片与足量硫酸反应 | 铝片开始无现象,一段时间后反应缓慢,铝片表面有少量气泡产生 | Al2O3+3H2SO4=2Al2(SO4)3+3H2O 2Al+3H2SO4=2Al2(SO4)3+3H2↑ |
| (3)铝片与足量氢氧化钠溶液反应 | 铝片开始无现象,一段时间后铝片逐渐溶解,并有大量气泡产生 | Al2O3+2NaOH+3H2O=2Na[Al(OH)4] 2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑ |
| A.对比(1)、(2)、(3)中Al2O3参与的反应可得出:Al2O3既有碱性氧化物的某些性质,又有酸性氧化物的某些性质 |
| B.对比(1)、(2)、(3)中气体产生现象和酸碱的挥发性可得出:实验(3)最适宜于实验室制备H2 |
| C.对比实验(1)、(2)中后来产生气泡的现象,可得出:c(H+)越大,相同时间内产生气泡越多 |
D.对比实验(1)、(2)中后来产生气泡的现象,可得出:SO 对Al与H+的反应可能有阻碍作用 对Al与H+的反应可能有阻碍作用 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列方程式书写正确的是
A.氢氧化钡和稀硫酸: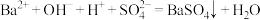 |
B.碳酸氢铵溶液中加入过量的氢氧化钠溶液: |
C.向NaOH溶液中通入过量 : : |
D.铝和氢氧化钠溶液反应: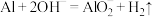 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列反应的离子方程式正确的是
A.向 溶液中滴加稀盐酸: 溶液中滴加稀盐酸: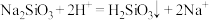 |
B.用饱和碳酸钠溶液浸泡 沉淀: 沉淀: |
C.Al与NaOH溶液反应: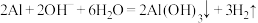 |
D.向 溶液中加入过量 溶液中加入过量 溶液: 溶液: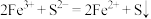 |
您最近半年使用:0次

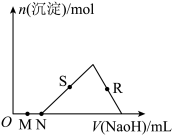
 、
、 、I-
、I- 、Cl-、CrO
、Cl-、CrO 、Br-、AlO
、Br-、AlO
 、SO
、SO

