下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
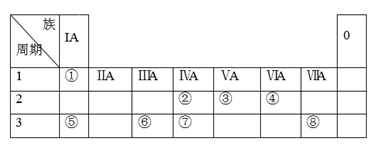
(1)①的元素符号为______ ;②的元素符号为______ ;③的元素符号为______ ;④的元素符号为______ ;⑤的元素符号为______ ;⑥的元素符号为______ ;⑦的元素符号为______ ;⑧的元素符号为_______ 。
(2)⑧的气态氢化物为_____________ (填化学式)。
(3)⑤对应的碱的化学式为__________ ;③的最高价含氧酸为___________ (填化学式)。
(4)⑤、⑥元素的金属性强弱依次为___________ (填“增大”、“减小”或“不变”)。

(1)①的元素符号为
(2)⑧的气态氢化物为
(3)⑤对应的碱的化学式为
(4)⑤、⑥元素的金属性强弱依次为
17-18高一·全国·课时练习 查看更多[2]
更新时间:2018-03-09 20:12:10
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,回答下列有关问题:
(1)在①~⑩元素中,最活泼的金属元素是___________ ,最活泼的非金属元素是___________ 。(填元素符号)。
(2)①②③元素的氢化物稳定性由强到弱的顺序___________ (请用化学式描述),请写出①的氢化物的电子式___________ 。
(3)在①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同),碱性最强的是___________ ,呈两性的是___________ 。写出在水溶液中三者之间相互反应的离子方程式:___________ ,___________ ,___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)①②③元素的氢化物稳定性由强到弱的顺序
(3)在①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)基态硫原子价电子排布式为___________ 。
(2)汞的原子序数为80,位于元素周期表第___________ 周期第ⅡB族。
(2)汞的原子序数为80,位于元素周期表第
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】C、N、O、F等元素的化合物在航天、美容、食品等多领域中有广泛的用途,请回答:
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为______ ;N、O、F的第一电离能由大到小的顺序为_____ (用元素符号表示)。
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为______ 晶体(填晶体类型)。
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第______ 周期第______ 族。
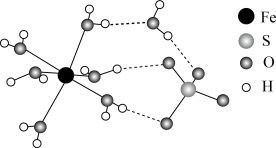
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO 的作用类型分别是
的作用类型分别是______ 、______ 。
A.离子键 B.配位键 C.氢键 D.金属键 中键角的大小并解释原因:
中键角的大小并解释原因:______ 。
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO
 的作用类型分别是
的作用类型分别是A.离子键 B.配位键 C.氢键 D.金属键
 中键角的大小并解释原因:
中键角的大小并解释原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
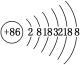
【推荐1】据报道,某些花岗岩会产生氡( Rn),对人体产生伤害。请回答:
Rn),对人体产生伤害。请回答:
(1)该原子的质量数是________ ,质子数是________ ,中子数是________ 。
(2)请根据Rn的原子结构预测,氡气的化学性质________ 。
A.非常活泼,容易与氧气等非金属单质反应
B.比较活泼,能与钠等金属反应
C.不太活泼
D.很难与其他物质发生反应
你选择该选项的理由是______________________________________________ 。
(3)研究发现,镭能蜕变为 Rn,故称
Rn,故称 Rn为镭射气;钍能蜕变为
Rn为镭射气;钍能蜕变为 Rn,故将
Rn,故将 Rn称为钍射气;锕能蜕变为
Rn称为钍射气;锕能蜕变为 Rn,故将
Rn,故将 Rn称为锕射气。则
Rn称为锕射气。则 Rn、
Rn、 Rn、
Rn、 Rn是
Rn是________ 。
A.同种元素 B.同位素
C.同种核素 D.同种原子
 Rn),对人体产生伤害。请回答:
Rn),对人体产生伤害。请回答:(1)该原子的质量数是
(2)请根据Rn的原子结构预测,氡气的化学性质

A.非常活泼,容易与氧气等非金属单质反应
B.比较活泼,能与钠等金属反应
C.不太活泼
D.很难与其他物质发生反应
你选择该选项的理由是
(3)研究发现,镭能蜕变为
 Rn,故称
Rn,故称 Rn为镭射气;钍能蜕变为
Rn为镭射气;钍能蜕变为 Rn,故将
Rn,故将 Rn称为钍射气;锕能蜕变为
Rn称为钍射气;锕能蜕变为 Rn,故将
Rn,故将 Rn称为锕射气。则
Rn称为锕射气。则 Rn、
Rn、 Rn、
Rn、 Rn是
Rn是A.同种元素 B.同位素
C.同种核素 D.同种原子
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】预测元素及其化合物的性质
| 项目 | 同周期(左→右) | 同主族(上→下) | |
| 原子 结构 | 核电荷数 | 逐渐 | 逐渐 |
| 电子层结构 | 电子层数 | 电子层数 | |
| 原子半径 | 逐渐 | 逐渐 | |
| 离子半径 | 阳离子逐渐减小,阴离子逐渐减小,但r(阴离子)>r(阳离子) | 逐渐增大 | |
| 性 质 | 主要化合价 | 元素的最高正化合价由+1→+7(O、F除外) 非金属元素负价由-4→-1 非金属元素负化合价= —(8—主族序数) | 相同 最高正化合价=主族序数 (O、F除外) |
| 元素的金属性 | 金属性逐渐 | 金属性逐渐 | |
| 元素的非金属性 | 非金属性逐渐 | 非金属性逐渐 | |
| 失电子能力 | 失电子逐渐减弱 | 失电子逐渐增强 | |
| 得电子能力 | 得电子逐渐增强 | 得电子逐渐减弱 | |
| 单质的还原性 | 还原性逐渐减弱 | 还原性逐渐增强 | |
| 单质的氧化性 | 氧化性逐渐增强 | 氧化性逐渐减弱 | |
| 阳离子的氧化性 | 阳离子氧化性逐渐增强 | 阳离子氧化性逐渐减弱 | |
| 阴离子的还原性 | 阴离子还原性逐渐减弱 | 阴离子还原性逐渐增强 | |
| 非金属元素气态氢化物的形成及稳定性 | 气态氢化物的形成越来越容易,其稳定性逐渐增强 | 气态氢化物的形成越来越困难,其稳定性逐渐减弱 | |
| 最高价氧化物对应水化物的酸碱性 | 碱性逐渐减弱 酸性逐渐增强 | 碱性逐渐增强 酸性逐渐减弱 | |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期律的一部分用元素符号或化学式、化学用语填空。
(1)在写出元素⑦的气态氢化物的电子式___ ;元素⑨的核外电子排布式为___ ;
(2)元素③的原子核外有___ 种能量不同的电子,有___ 种运动状态电子。
(3)元素⑧与⑥形成的晶体是___ 晶体:元素⑤和⑩形成的分子属于___ 分子(极性、非极性):
(4)写出元素②与④的最高价氧化物对应水化物之间反应的方程式___ ;
(5)元素⑨和⑩的非金属性比较更强___ (元素符号),用一个方程式说明这一结论___ 。
(6)关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是___ (写编号)。
a.原子半径:Na<Cl b.离子半径:F-<Mg2+
c.热稳定性:HF>HCl d.碱性:NaOH>Mg(OH)2
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ⑤ | ⑦ | ⑧ | ||||
| 3 | ② | ③ | ④ | ⑥ | ⑨ | ⑩ |
(1)在写出元素⑦的气态氢化物的电子式
(2)元素③的原子核外有
(3)元素⑧与⑥形成的晶体是
(4)写出元素②与④的最高价氧化物对应水化物之间反应的方程式
(5)元素⑨和⑩的非金属性比较更强
(6)关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是
a.原子半径:Na<Cl b.离子半径:F-<Mg2+
c.热稳定性:HF>HCl d.碱性:NaOH>Mg(OH)2
您最近一年使用:0次



