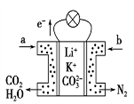
有报道称以硼氢化钠(NaBH4,强还原剂)和H2O2作原料的燃料电池,可用作空军通信卫星电源,其工作原理如右图所示。下列说法错误 的是
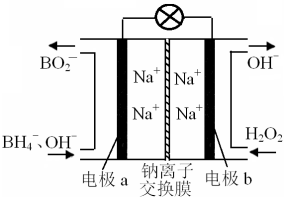

| A.电极b作正极,发生还原反应 |
| B.该电池的负极反应为:BH4-+8OH--8e-=BO2-+6H2O |
| C.每消耗3 mol H2O2,转移的电子为3 mol |
| D.不考虑能量损耗,当有1mol H2O2参加反应时,即有2 mol Na+从a极区移向b极区 |
更新时间:2018-09-03 14:14:31
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】以KOH溶液为电解质溶液,分别组成 、
、 、
、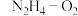 清洁燃料电池,下列说法正确的是
清洁燃料电池,下列说法正确的是
 、
、 、
、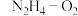 清洁燃料电池,下列说法正确的是
清洁燃料电池,下列说法正确的是| A.放电过程中,OH-均向正极移动 |
| B.放电过程中,KOH物质的量均减小 |
C.消耗等质量氧气时, 燃料电池的理论放电量最大 燃料电池的理论放电量最大 |
D.消耗等物质的量燃料时, 燃料电池的理论放电量最大 燃料电池的理论放电量最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】镁-次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,关于该电池的叙述不正确 的是
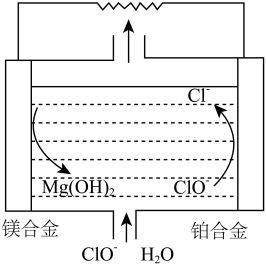

| A.铂合金为正极,附近溶液的碱性增强 |
| B.电池工作时,OH-向镁合金电极移动 |
| C.电池工作时,需要不断添加次氯酸盐以保证电解质的氧化能力 |
| D.若电解质溶液为H2O2,硫酸和NaCl的混合液,则正极反应为H2O2+2e-=2OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
| A.氢氧燃料电池工作时化学能全部转化电能 |
| B.氢氧燃料电池的负极反应为O2+4H++4e-=2H2O |
| C.氢氧燃料电池放电过程中消耗11.2LH2(标准状况下),转移的电子数目为6.02×1023 |
| D.反应2H2(g)+O2(g)=2H2O(g)的ΔH可通过下式估算:ΔH=反应中形成新共价键的键能之和—反应中断裂旧共价键的键能之和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】锌-空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,放电时电池总反应为2Zn+O2+4OH-+2H2O=2Zn(OH)42-。下列说法错误的是( )
| A.电解质溶液中K+向正极移动 |
| B.电解质溶液中c(OH)-逐渐减小 |
| C.负极反应式为Zn+4OH--2e-=Zn(OH)42- |
| D.电路中通过2mol电子时,消耗氧气22.4L(标准状况下) |
您最近一年使用:0次