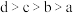短周期主族元素X、Y、Z、W的原子序数依次增大,其中只有Z为金属元素,X 的原子半径是所有原子中最小的,W原子的最外层电子数是Z原子的2倍。常温下,X、Y形成的一种化合物是应用广泛的气态清洁能源,W的单质是淡黄色固体。下列说法正确的是
| A.原子半径:X<Z<W |
| B.非金属性:X>Y |
| C.Y、W的最高价氧化物对应的水化物均属于强电解质 |
| D.Z、W形成的化合物溶于水既生成沉淀又生成气体 |
更新时间:2018-04-19 10:04:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种短周期元素的原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列叙述错误的是

| A.Z单质存在同素异形体 |
| B.该物质的阳离子中存在配位键 |
| C.Y是五种元素中第一电离能最大的 |
| D.标准状况下,22.4LX的氢化物中H原子的数目均为4NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知有如下四种元素:
①3p能级为半充满的元素 ②只有1个电子的元素 ③价层电子为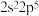 的元素 ④第三周期原子半径最大的元素
的元素 ④第三周期原子半径最大的元素
下列有关说法正确的是
①3p能级为半充满的元素 ②只有1个电子的元素 ③价层电子为
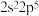 的元素 ④第三周期原子半径最大的元素
的元素 ④第三周期原子半径最大的元素下列有关说法正确的是
A.①②组成的化合物稳定性比 强 强 | B.①③组成的化合物均无孤电子对 |
| C.②③组成的化合物为强电解质 | D.②④组成的化合物可以是离子晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知Q、R、X、Y、Z均为短周期元素,原子序数依次增大,X原子的K层电子数比M层电子数少1个,Q与Z同主族。R是同周期元素中金属性最强,Y与Z相邻,可形成所有原子最外层均为8电子稳定结构的 分子,下列说法错误的是
分子,下列说法错误的是
 分子,下列说法错误的是
分子,下列说法错误的是A.简单离子半径: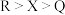 |
B. 分子中,Z显-1价 分子中,Z显-1价 |
C.简单氢化物的还原性: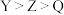 |
| D.R、X、Y的最高价氧化物对应的水化物能相互反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素X、Y、Z、W、N的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y的次外层电子数是其电子总数的 ,离子化合物ZX2是一种储氢材料,W与Y属于同一主族,NY2是医学上常用的水消毒剂、漂白剂。下列叙述正确的是( )
,离子化合物ZX2是一种储氢材料,W与Y属于同一主族,NY2是医学上常用的水消毒剂、漂白剂。下列叙述正确的是( )
 ,离子化合物ZX2是一种储氢材料,W与Y属于同一主族,NY2是医学上常用的水消毒剂、漂白剂。下列叙述正确的是( )
,离子化合物ZX2是一种储氢材料,W与Y属于同一主族,NY2是医学上常用的水消毒剂、漂白剂。下列叙述正确的是( )| A.Y和W分别与X形成的简单化合物的热稳定性:X2Y>X2W |
| B.离子半径由小到大的顺序为Y2-<Z2+<N-<W2- |
| C.ZX2和NY2中化学键一致,且微粒个数之比均为1:2 |
| D.含氧酸的酸性:N>W,可证明非金属性:N>W |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.短周期元素X、Y的原子序数相差2,则X、Y不可能处于同一主族 |
| B.可根据氢化物的稳定性和酸性强弱,来判断非金属元素得电子能力强弱 |
| C.非金属元素的最高化合价不超过其元素原子的最外层电子数 |
| D.单原子形成的离子,一定与稀有气体原子的核外电子排布相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】前四周期元素X、Y、Z、W的原子序数依次增大。基态时,X和Z原子L层上均有2个未成对电子。W位于第四周期,基态时其原子核外未成对电子数在同周期中最多。下列说法正确的是
A.原子半径: |
B.第一电离能: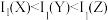 |
| C.Y的氧化物对应水化物是强酸 |
| D.W元素位于元素周期表的VIB族 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大,四种元素的原子序数之和等于42。下列叙述错误的是
| X | Y | ||
| Z | W |
A.简单离子半径: |
B.最高价氧化物对应水化物酸性: |
| C.Z的氧化物是两性氧化物 |
| D.Z和W反应中W作氧化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】A、B、C、D、E 为元素周期表中的前18号主族元素,原子序数依次增大,其中A与C、B与E均为同主族元素,原子半径:A<B<E<D<C,B原子最外层电子数是内层电子数的3倍,C、D的核外电子数之和与B、E的核外电子数之和相等。下列说法正确的是
| A.原子最外层电子数:B<A |
| B.B与E可以形成EB2型化合物 |
| C.A与E形成的化合物是离子化合物 |
| D.最高价氧化物对应水化物的碱性:C<D |
您最近一年使用:0次