现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向1 mol/L的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是________ 。
(2)利用胶体的____________________ 性质区分Fe(OH)3胶体和FeCl3溶液
(3)丁同学利用所制得的Fe(OH)3胶体进行实验:
①将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明Fe(OH)3胶体粒子带_____ (填“正”或“负”)电荷。
②向其中加入饱和Na2SO4溶液,产生的现象是____________________ 。
(4)写出甲同学的离子反应方程式_______________________________
甲同学:向1 mol/L的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至液体呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是
(2)利用胶体的
(3)丁同学利用所制得的Fe(OH)3胶体进行实验:
①将其装入U形管内,用石墨作电极,通电一段时间后发现阴极区附近的颜色逐渐变深,这表明Fe(OH)3胶体粒子带
②向其中加入饱和Na2SO4溶液,产生的现象是
(4)写出甲同学的离子反应方程式
更新时间:2018/11/15 14:40:47
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体。X、Y、Z是化合物。X溶液呈淡绿色,Y、Z的溶液都能使KSCN溶液变红。它们之间有如下图所示转化关系。
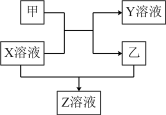
请回答:
(1)将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体,此液体不具有的性质是_____
(2)①单质甲、乙和Y溶液中的阳离子氧化性由强到弱的顺序为:____________________ (用化学式表示)
②少量单质甲通入X溶液中发生的离子方程式为______________________________
(3)实验室制备、收集纯净干燥的甲单质,所需仪器如下,装置A为发生装置;除装置A中所需的药品外,其他装置中供选择的药品有:浓硫酸、碱石灰、五氧化二磷、饱和食盐水、氢氧化钠溶液。
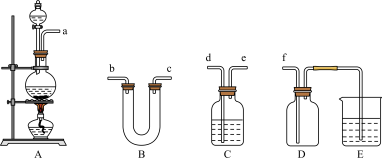
①装置A中发生反应的化学反应方程式:______________________
②按气流的方向连接各仪器接口,顺序为
a→_________ →_________ →_________ →_________ →f。
③指出装置B、C、E中的药品(从提供的药品中选择):
B:________________ C:___________________ E:__________________

请回答:
(1)将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体,此液体不具有的性质是_____
| A.光束通过该液体时形成光亮的“通路” |
| B.插入电极通过直流电后,有一极附近液体颜色加深 |
| C.向该液体中加入硝酸银溶液,无沉淀产生 |
| D.将该液体加热蒸干、灼烧后,有氧化物生成 |
②少量单质甲通入X溶液中发生的离子方程式为
(3)实验室制备、收集纯净干燥的甲单质,所需仪器如下,装置A为发生装置;除装置A中所需的药品外,其他装置中供选择的药品有:浓硫酸、碱石灰、五氧化二磷、饱和食盐水、氢氧化钠溶液。

①装置A中发生反应的化学反应方程式:
②按气流的方向连接各仪器接口,顺序为
a→
③指出装置B、C、E中的药品(从提供的药品中选择):
B:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如图所示为一“铁链”图案,某化学兴趣小组的同学在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。

(1)将分类依据代号填入相应的横线上:
①两种物质都不是电解质_______ ;
②两种物质都是钠的化合物_______ ;
③两种物质都是氧化物_______ ;
④两种物质都是盐_______ 。
(2)用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中逐滴加入图中某物质的饱和溶液,继续煮沸可制得一种红褐色胶体。
①该物质的化学式为_______ 。
②向该胶体中逐滴加入稀盐酸,会发生一系列变化:
a.先产生红褐色沉淀,原因是_______ 。
b.随后红褐色沉淀溶解,此时发生反应的离子方程式是_______ 。

(1)将分类依据代号填入相应的横线上:
①两种物质都不是电解质
②两种物质都是钠的化合物
③两种物质都是氧化物
④两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中逐滴加入图中某物质的饱和溶液,继续煮沸可制得一种红褐色胶体。
①该物质的化学式为
②向该胶体中逐滴加入稀盐酸,会发生一系列变化:
a.先产生红褐色沉淀,原因是
b.随后红褐色沉淀溶解,此时发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】绿矾( )是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al、
)是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al、 和
和 )制备磁性
)制备磁性 胶体粒子、绿矾和净水剂
胶体粒子、绿矾和净水剂 的实验流程如图:
的实验流程如图:
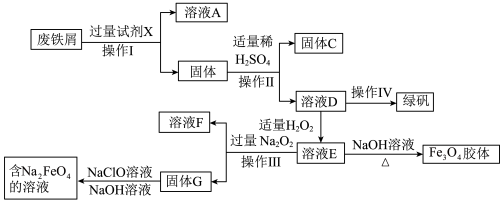
回答下列问题:
(1)试剂X为_____________ ,操作Ⅰ、Ⅱ、Ⅲ均为_____________ 操作。
(2)固体C为_________________ ,溶液D中加入KSCN溶液,无血红色产生,原因是(用离子方程式表示)_________________________ 。
(3)D中加入适量 反应的离子方程式
反应的离子方程式_________________________ ;若D中含a mol  ,则理论上加入
,则理论上加入____________ mol  可使溶液E中铁元素恰好转化为
可使溶液E中铁元素恰好转化为 胶体。
胶体。
(4)证明 胶体已经生成的方法是
胶体已经生成的方法是______________________________ 。
(5) 中铁元素的化合价为
中铁元素的化合价为_____________ ,由固体G生成 的离子方程式为
的离子方程式为___________________________________________________ 。
(6)由 配制450mL 1
配制450mL 1
 溶液,需要的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、
溶液,需要的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、_____________ 。
(7)以下操作会导致所配溶液浓度偏低的是 (填字母)。
 )是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al、
)是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al、 和
和 )制备磁性
)制备磁性 胶体粒子、绿矾和净水剂
胶体粒子、绿矾和净水剂 的实验流程如图:
的实验流程如图:
回答下列问题:
(1)试剂X为
(2)固体C为
(3)D中加入适量
 反应的离子方程式
反应的离子方程式 ,则理论上加入
,则理论上加入 可使溶液E中铁元素恰好转化为
可使溶液E中铁元素恰好转化为 胶体。
胶体。(4)证明
 胶体已经生成的方法是
胶体已经生成的方法是(5)
 中铁元素的化合价为
中铁元素的化合价为 的离子方程式为
的离子方程式为(6)由
 配制450mL 1
配制450mL 1
 溶液,需要的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、
溶液,需要的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、(7)以下操作会导致所配溶液浓度偏低的是 (填字母)。
| A.转移前容量瓶中有少量水 |
| B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中 |
| C.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线 |
| D.定容时俯视容量瓶刻度线 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的 溶液继续煮沸,至液体呈透明的红褐色。
溶液继续煮沸,至液体呈透明的红褐色。
(1)反应原理为_______ 。
(2)某同学按要求制备了 胶体,但是他又向
胶体,但是他又向 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:先出现红褐色沉淀,稀
溶液,结果出现了一系列变化:先出现红褐色沉淀,稀 溶液的量足够后沉淀溶解。沉淀溶解发生反应的离子方程式是
溶液的量足够后沉淀溶解。沉淀溶解发生反应的离子方程式是_______ 。
Ⅱ.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。工业碳酸钠(纯度约为98%)中含有 、
、 、
、 、
、 、
、 等杂质,提纯工艺线路如下:
等杂质,提纯工艺线路如下:
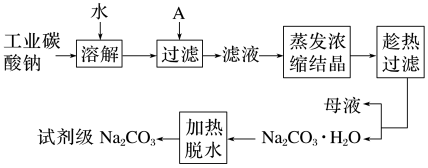
碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:

请回答下列问题:
(3)试剂 A 是过量 的NaOH溶液,作用是除去_______ 离子。“母液”中除了含有 、
、 、
、 外,还含有
外,还含有_______ 、_______ 等离子,过滤要“趁热”的目的是_______ 。
(4)检验试剂级 中
中 和
和 是否除尽,选用的试剂及加入的先后次序是_______(填字母)
是否除尽,选用的试剂及加入的先后次序是_______(填字母)
 溶液继续煮沸,至液体呈透明的红褐色。
溶液继续煮沸,至液体呈透明的红褐色。(1)反应原理为
(2)某同学按要求制备了
 胶体,但是他又向
胶体,但是他又向 胶体中逐滴加入了稀
胶体中逐滴加入了稀 溶液,结果出现了一系列变化:先出现红褐色沉淀,稀
溶液,结果出现了一系列变化:先出现红褐色沉淀,稀 溶液的量足够后沉淀溶解。沉淀溶解发生反应的离子方程式是
溶液的量足够后沉淀溶解。沉淀溶解发生反应的离子方程式是Ⅱ.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。工业碳酸钠(纯度约为98%)中含有
 、
、 、
、 、
、 、
、 等杂质,提纯工艺线路如下:
等杂质,提纯工艺线路如下:
碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:

请回答下列问题:
(3)
 、
、 、
、 外,还含有
外,还含有(4)检验试剂级
 中
中 和
和 是否除尽,选用的试剂及加入的先后次序是_______(填字母)
是否除尽,选用的试剂及加入的先后次序是_______(填字母)A.HCl、 / / | B. 、 、 、 、 |
C. 、 、 、 、 | D. 、HCl、 、HCl、 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】高三老师设计了“Fe3+的氧化性实验探究”学案,课后选取一学生学案,其中部分内容如下。依据已有知识及学案相关内容。
回顾:Fe2+呈淡绿色、Fe3+呈棕黄色、Fe(OH)3胶体是红褐色液体。
提供资料:FeSO3是墨绿色沉淀
设置问题:Na2SO3溶液与FeCl3溶液反应猜想
猜提一:Na2SO3溶液与FeCl3溶液发生氧化还原反应;
猜想二:Na2SO3溶液与FeCl3溶液发生相互促进的水解反应,产生了Fe(OH)3胶体;
猜想三:_______。
(1)请将划线空白处补充完整_______ 。
问题探究:
(2)若猜想一正确,预测的实验现象是_______ ,反应的离子方程式为_______ 。
小组实验i:
现象记录:溶液黄色逐渐加深,最终得到红褐色溶液W
(3)观察实验现象证实猜想二合理,用红色激光笔照射该红褐色液体,预测的现象是_______ ;反应的离子方程式为_______ 。
(4)组织同学讨论:氧化还原反应是否发生,怎样检验。(归纳同学得出的检验方案)
方来①:取少量W液作,加铁氧化钾溶液,检验是否有Fe2+;
方来②:取少量W液伸,加酸性高锰酸钾漆液,检验是否有Fe2+;
方来③:取少量W液伸,加盐酸酸化,再加氯化钾溶液,检验是否有SO 。
。
你认为方案②_______ (填“合理”或“不合理”),理由是_______ 。
完善证据:
分组实验ⅱ:
现象记录:产生由色沉淀
分组实验ⅲ:取少量W液体,加铁氰化钾溶液,发现有蓝色沉淀生成。
探究结论:Fe3+与SO 的反应体系中,氧化还原反应与水解反应下仅共存而且存在竞争。
的反应体系中,氧化还原反应与水解反应下仅共存而且存在竞争。
回顾:Fe2+呈淡绿色、Fe3+呈棕黄色、Fe(OH)3胶体是红褐色液体。
提供资料:FeSO3是墨绿色沉淀
设置问题:Na2SO3溶液与FeCl3溶液反应猜想
猜提一:Na2SO3溶液与FeCl3溶液发生氧化还原反应;
猜想二:Na2SO3溶液与FeCl3溶液发生相互促进的水解反应,产生了Fe(OH)3胶体;
猜想三:_______。
(1)请将划线空白处补充完整
问题探究:
(2)若猜想一正确,预测的实验现象是
小组实验i:
| 装置 | 操作 |
 | 向2mLmol·L-1的FeCl3溶液中逐滴滴加1mLmol·L-1的Na2SO3溶液 |
(3)观察实验现象证实猜想二合理,用红色激光笔照射该红褐色液体,预测的现象是
(4)组织同学讨论:氧化还原反应是否发生,怎样检验。(归纳同学得出的检验方案)
方来①:取少量W液作,加铁氧化钾溶液,检验是否有Fe2+;
方来②:取少量W液伸,加酸性高锰酸钾漆液,检验是否有Fe2+;
方来③:取少量W液伸,加盐酸酸化,再加氯化钾溶液,检验是否有SO
 。
。你认为方案②
完善证据:
分组实验ⅱ:
| 装置 | 操作 |
 | 取1mLW液体于试管中,滴加过量盐酸,再滴加5滴BaCl溶液 |
分组实验ⅲ:取少量W液体,加铁氰化钾溶液,发现有蓝色沉淀生成。
探究结论:Fe3+与SO
 的反应体系中,氧化还原反应与水解反应下仅共存而且存在竞争。
的反应体系中,氧化还原反应与水解反应下仅共存而且存在竞争。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】(1)NaCl中含有少量的Na2SO4,为测定NaCl纯度,某学生取样品a g溶解于水,然后滴入过量的BaCl2溶液使SO42-离子转化为沉淀,然后将所得沉淀过滤、洗涤、转移、干燥、称量质量为b g 。
①确认SO42-已沉淀完全的实验方法是___________________________ ;
②过滤后洗涤沉淀的方法是____________________________________ ;
③判断沉淀已经洗净的方法是___________________________________ ;
④氯化钠纯度(ω)的计算表达式为________________________
(2)Fe(OH)3胶体的制备:取一小烧杯,加入25 mL蒸馏水,加热至沸腾,然后向沸水中逐滴加入5 ~ 6滴________ ,继续煮沸至体系呈________ ,停止加热,即制得Fe(OH)3胶体,请写出胶体制备过程的离子方程式_____________ 。
①确认SO42-已沉淀完全的实验方法是
②过滤后洗涤沉淀的方法是
③判断沉淀已经洗净的方法是
④氯化钠纯度(ω)的计算表达式为
(2)Fe(OH)3胶体的制备:取一小烧杯,加入25 mL蒸馏水,加热至沸腾,然后向沸水中逐滴加入5 ~ 6滴
您最近一年使用:0次



