下列有关热化学方程式的叙述正确的是( )
| A.反应物的总能量低于生成物的总能量时,该反应必须加热才能发生 |
| B.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-akJ·mol-1,则中和热为0.5akJ·mol-1 |
| C.2H2(g)+O2(g)=2H2O(l);△H1=-akJ·mol-1,则氢气燃烧热为akJ·mol-1 |
| D.N2(g)+3H2(g)=2NH3(g);△H=-akJ·mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量 |
更新时间:2018-12-07 17:36:21
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
A. 稀 稀 与 与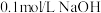 溶液混合时,其活化能接近于零,反应速率快,且该反应为放热反应 溶液混合时,其活化能接近于零,反应速率快,且该反应为放热反应 |
B.反应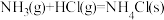 在低温下能自发进行,说明该反应的 在低温下能自发进行,说明该反应的 |
C.已知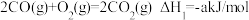 , ,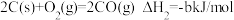 ,则 ,则 燃烧热的热化学方程式为 燃烧热的热化学方程式为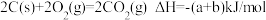 |
D.已知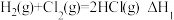 , ,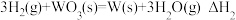 ,则 ,则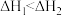 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关能量的判断和表示方法正确的是
| A.由C(s,石墨)=C(s,金刚石) ΔH=+1.9kJ·mol-1,可知:石墨比金刚石更稳定 |
| B.等质量的C2H5OH(g)和C2H5OH(l)分别完全燃烧,后者放出的热量更多 |
| C.由H+(aq)+OH-(aq)=H2O(l) ΔH= -57.3kJ·mol-1,可知:含1mol HCl的溶液与含1mol NH3•H2O的溶液混合,放出热量等于57.3kJ |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH1; 2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法错误的是
| A.已知298K时,2SO2(g)+O2(g)⇌2SO3(g) ∆H=-197kJ/mol,对该热化学方程式理解为:在该条件下,向密闭容器中通入2摩SO2和1摩O2,达到平衡时放出热量是197kJ |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的∆H=+(2×283.0)kJ/mol |
| C.吸热反应是指反应物所具有的总能量低于生成物所具有的总能量,而不是看反应过程是否需要加热 |
D.对下列反应:HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ∆H=-Q1kJ/mol; H2SO4(浓)+NaOH(aq)= H2SO4(浓)+NaOH(aq)= Na2SO4(aq)+H2O(l) ∆H=-Q2kJ/mol;上述反应均在溶液中进行,则Q2>Q1 Na2SO4(aq)+H2O(l) ∆H=-Q2kJ/mol;上述反应均在溶液中进行,则Q2>Q1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关热化学方程式的叙述正确的是( )
| A.已知2H2(g)+O2(g)=2 H2O(g) △H= -483.6kJ·mol-1,则氢气的燃烧热△H= -241.8 kJ/mol |
| B.已知2C(s)+2O2(g)=2CO2(g) △H1;2C(s)+O2(g)=2CO(g) △H2,则△H1>△H2 |
| C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为: NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) △H= -57.4kJ·mol-1 |
| D.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g) △H= +566.0kJ/mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验操作或装置能达到相应目的的是
| A | B | C | D |
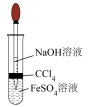 | 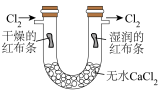 | 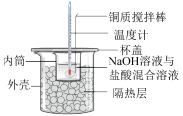 |  |
制备 | 验证干燥的氯气是否有漂白性 | 中和反应反应热的测定 | 证明化学反应存在一定的限度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



