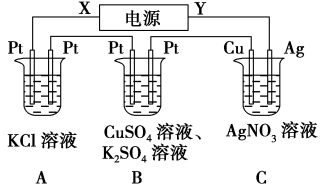
某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装 置的开关时,观察到电流表的指针发生了偏转。

请回答下列问题:
(1)甲池为原电池,通入 CH3OH 电极的电极反应为________ 。
(2)乙池中A(石墨)电极的名称为_____ (填“正极”“负极”或“阴极”“阳极”),总反应为_____ 。
(3)当乙池B极质量增加 5.4 g 时,甲池中理论上消耗 O2的体积为_____ mL(标准状况),丙池D极析出_____ g 铜。

请回答下列问题:
(1)甲池为原电池,通入 CH3OH 电极的电极反应为
(2)乙池中A(石墨)电极的名称为
(3)当乙池B极质量增加 5.4 g 时,甲池中理论上消耗 O2的体积为
18-19高一上·江西宜春·期末 查看更多[3]
河北省邯郸市磁县第二中学2019-2020学年高一下学期期中考试化学试卷(已下线)2019年12月8日 《每日一题》人教版(选修4)——每周一测江西省丰城中学2018-2019学年高一上学期课改期末考试化学试题
更新时间:2019-02-19 10:22:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】如图是一个化学过程的示意图。已知甲池的总反应式为:
2CH3OH+3O2+4KOH 2K2CO3+6H2O


(1)请回答图中甲、乙两池的名称。甲电池是_______ 装置,乙池是_______ 装置。
(2)请回答下列电极的名称:通入CH3OH的电极名称是__________ ,B(石墨)电极的名称是_______ 。
(3)写出电极反应式: 通入O2的电极的电极反应式是____________ 。
(4)乙池中反应的化学方程式为_______________________ 。
(5)当乙池中A(Fe)极的质量增加10.8g时,甲池中理论上消耗O2________ mL(标准状况下)
2CH3OH+3O2+4KOH 2K2CO3+6H2O


(1)请回答图中甲、乙两池的名称。甲电池是
(2)请回答下列电极的名称:通入CH3OH的电极名称是
(3)写出电极反应式: 通入O2的电极的电极反应式是
(4)乙池中反应的化学方程式为
(5)当乙池中A(Fe)极的质量增加10.8g时,甲池中理论上消耗O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】据图回答下列问题:
Ⅰ.(1)若烧杯中溶液为稀硫酸,则观察到的现象是__________ ,负极反应式为:_______________________ 。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________ (填Mg或Al),总反应化学方程式为________________________________ 。

Ⅱ. (3)由Al、Cu、浓硝酸组成原电池,其负极的电极反应式为______________________ 。
Ⅲ.中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇(CH3OH)燃料电池的工作原理如下图所示。

(4)该电池工作时,b口通入的物质为_______ ,c口通入的物质为______ 。
(5)该电池正极的电极反应式为:_____________ 。
Ⅰ.(1)若烧杯中溶液为稀硫酸,则观察到的现象是
(2)若烧杯中溶液为氢氧化钠溶液,则负极为

Ⅱ. (3)由Al、Cu、浓硝酸组成原电池,其负极的电极反应式为
Ⅲ.中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇(CH3OH)燃料电池的工作原理如下图所示。

(4)该电池工作时,b口通入的物质为
(5)该电池正极的电极反应式为:
您最近一年使用:0次
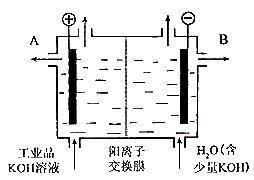
【推荐1】Ⅰ. 燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示:
燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示:
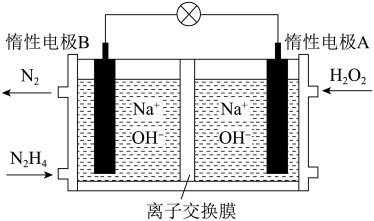
电池工作时,A极区 NaOH浓度不变,则离子交换膜为___________ (填"阳离子交换膜"或"阴离子交换膜");电极 B的电极反应式为___________ ;电池工作时参加反应的 =
=___________ (整数比)。
Ⅱ.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,弃去浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计的装置示意图如图所示。
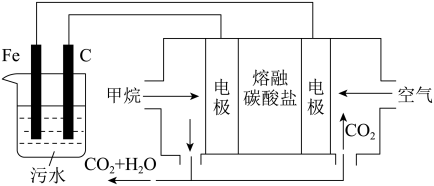
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的___________ (填选项字母)。
a.H2SO4 b.CH3CH2OH c.Na2SO4 d.NaOH
(2)电解过程中,电解池阳极发生了两个电极反应,其中一个为2H2O-4e-=O2↑+4H+,则另一个电极反应式为___________ 。
(3)熔融盐燃料电池以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,惰性材料为电极,正极的电极反应式为___________ 。
(4)实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗标准状况下的CH4体积___________ L。
 燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示:
燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示:
电池工作时,A极区 NaOH浓度不变,则离子交换膜为
 =
=Ⅱ.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,弃去浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计的装置示意图如图所示。

(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的
a.H2SO4 b.CH3CH2OH c.Na2SO4 d.NaOH
(2)电解过程中,电解池阳极发生了两个电极反应,其中一个为2H2O-4e-=O2↑+4H+,则另一个电极反应式为
(3)熔融盐燃料电池以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,惰性材料为电极,正极的电极反应式为
(4)实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池消耗标准状况下的CH4体积
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
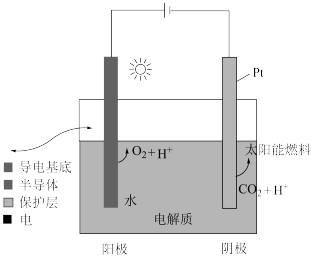
【推荐2】以TiO2为催化剂,在光照条件下可将 还原为HCOO-等有机物。
还原为HCOO-等有机物。
(1)制备TiO2:
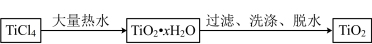
TiCl4转化为TiO2·xH2O的化学方程式是_______ 。
(2)光催化还原 的反应过程如下图所示。
的反应过程如下图所示。
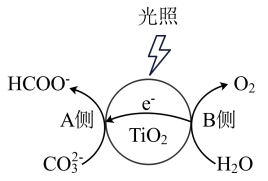
A侧产生HCOO-的反应式为_______ 。
在光照和TiO2存在下,以体积相同的0.25mol·L-1Na2CO3溶液为反应物,相同时间后检测HCOO-浓度,结果如下表。
(3)推测HCO 也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:
也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:_______ 。
(4)实验iii中HCOO-浓度明显低于实验i,可能的原因是_______ 。
(5)研究实验iv中HCOO-浓度明显高于实验i的原因,设计并完成实验v。
实验v:光照条件下,未添加TiO2时重复实验iv,没有检测到SO 。
。
①实验v中检测SO 的操作和现象为
的操作和现象为_______ 。
②对比实验iv、v,分析实验iv中Na2SO3的作用:_______ (答出2点)。
 还原为HCOO-等有机物。
还原为HCOO-等有机物。(1)制备TiO2:

TiCl4转化为TiO2·xH2O的化学方程式是
(2)光催化还原
 的反应过程如下图所示。
的反应过程如下图所示。
A侧产生HCOO-的反应式为
在光照和TiO2存在下,以体积相同的0.25mol·L-1Na2CO3溶液为反应物,相同时间后检测HCOO-浓度,结果如下表。
| 实验 | 溶液中添加的其它成分 | 通入的气体 | 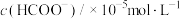 |
| ⅰ | - | - | 73.5 |
| ⅱ | - | CO2 | 92.6 |
| ⅲ | - | O2 | 2.1 |
| ⅳ | Na2SO3 | - | 158.1 |
 也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:
也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:(4)实验iii中HCOO-浓度明显低于实验i,可能的原因是
(5)研究实验iv中HCOO-浓度明显高于实验i的原因,设计并完成实验v。
实验v:光照条件下,未添加TiO2时重复实验iv,没有检测到SO
 。
。①实验v中检测SO
 的操作和现象为
的操作和现象为②对比实验iv、v,分析实验iv中Na2SO3的作用:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:
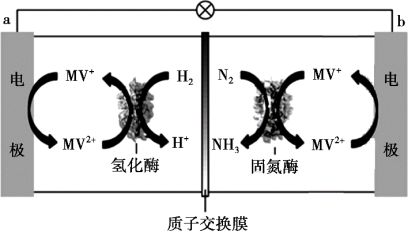
①氢化酶区域所发生反应的离子方程式为____ 。
②整个b电极区域所发生的总反应的离子方程式为____ 。
③相比传统工业合成氨,该方法的优点有____ 。
(2)若用如图所示生物燃料电池作甲装置的电源,并将甲装置中产生的CH4气体通入乙装置中,发生转化的过程如图:
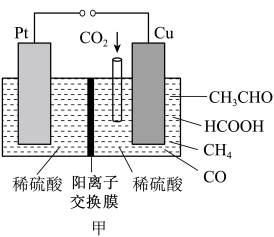
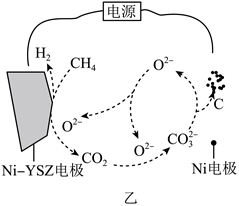
①甲装置中Pt电极应连接生物燃料电池的___ 电极(填“a”或“b”)。电解一段时间后,甲装置阳极区c(H+)____ (填“增大”“减小”或“不变”)。
②乙装置中Ni—YSZ电极上的反应为:CH4-4e-+2O2-=CO2+2H2,且整个过程中消耗的O2-和产生的O2-总数目相等。则在Ni—YSZ电极上消耗的O2-与CO2消耗的O2-数目之比为____ 。
③若开始电解一段时间后,甲装置中铜电极上只生成6.4gCH4,则甲装置铜极区溶液质量变化了____ g,乙装置中理论上生成碳的质量为___ g,生物燃料电池中理论上合成氨的质量为___ g(保留到小数点后两位)。
(1)目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①氢化酶区域所发生反应的离子方程式为
②整个b电极区域所发生的总反应的离子方程式为
③相比传统工业合成氨,该方法的优点有
(2)若用如图所示生物燃料电池作甲装置的电源,并将甲装置中产生的CH4气体通入乙装置中,发生转化的过程如图:


①甲装置中Pt电极应连接生物燃料电池的
②乙装置中Ni—YSZ电极上的反应为:CH4-4e-+2O2-=CO2+2H2,且整个过程中消耗的O2-和产生的O2-总数目相等。则在Ni—YSZ电极上消耗的O2-与CO2消耗的O2-数目之比为
③若开始电解一段时间后,甲装置中铜电极上只生成6.4gCH4,则甲装置铜极区溶液质量变化了
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为离子交换膜。请按要求回答相关问题:
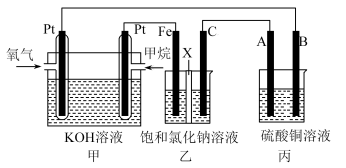
(1)甲烷燃料电池负极反应式是___________ 。
(2)Fe电极的电极反应式为___________ 。
(3)X选择___________ 离子交换膜(填“阴”,“阳”)。
(4)丙模拟粗铜的精炼,那么粗铜放在___________ (填“A”,“B”)极,反应结束后硫酸铜溶液的浓度___________ (填“变大”,“变小”,“不变”)。
(5)若在标准状况下,有11.2 L氧气参加反应,则乙装置中铁极上生成的气体体积为___________ L。
(6)写出图中电解饱和食盐水的总的化学反应方程式___________ 。

(1)甲烷燃料电池负极反应式是
(2)Fe电极的电极反应式为
(3)X选择
(4)丙模拟粗铜的精炼,那么粗铜放在
(5)若在标准状况下,有11.2 L氧气参加反应,则乙装置中铁极上生成的气体体积为
(6)写出图中电解饱和食盐水的总的化学反应方程式
您最近一年使用:0次