以TiO2为催化剂,在光照条件下可将 还原为HCOO-等有机物。
还原为HCOO-等有机物。
(1)制备TiO2:
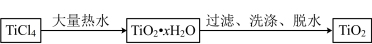
TiCl4转化为TiO2·xH2O的化学方程式是_______ 。
(2)光催化还原 的反应过程如下图所示。
的反应过程如下图所示。
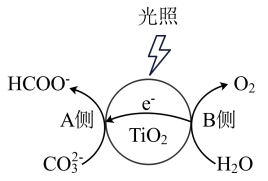
A侧产生HCOO-的反应式为_______ 。
在光照和TiO2存在下,以体积相同的0.25mol·L-1Na2CO3溶液为反应物,相同时间后检测HCOO-浓度,结果如下表。
(3)推测HCO 也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:
也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:_______ 。
(4)实验iii中HCOO-浓度明显低于实验i,可能的原因是_______ 。
(5)研究实验iv中HCOO-浓度明显高于实验i的原因,设计并完成实验v。
实验v:光照条件下,未添加TiO2时重复实验iv,没有检测到SO 。
。
①实验v中检测SO 的操作和现象为
的操作和现象为_______ 。
②对比实验iv、v,分析实验iv中Na2SO3的作用:_______ (答出2点)。
 还原为HCOO-等有机物。
还原为HCOO-等有机物。(1)制备TiO2:

TiCl4转化为TiO2·xH2O的化学方程式是
(2)光催化还原
 的反应过程如下图所示。
的反应过程如下图所示。
A侧产生HCOO-的反应式为
在光照和TiO2存在下,以体积相同的0.25mol·L-1Na2CO3溶液为反应物,相同时间后检测HCOO-浓度,结果如下表。
| 实验 | 溶液中添加的其它成分 | 通入的气体 | 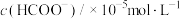 |
| ⅰ | - | - | 73.5 |
| ⅱ | - | CO2 | 92.6 |
| ⅲ | - | O2 | 2.1 |
| ⅳ | Na2SO3 | - | 158.1 |
 也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:
也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:(4)实验iii中HCOO-浓度明显低于实验i,可能的原因是
(5)研究实验iv中HCOO-浓度明显高于实验i的原因,设计并完成实验v。
实验v:光照条件下,未添加TiO2时重复实验iv,没有检测到SO
 。
。①实验v中检测SO
 的操作和现象为
的操作和现象为②对比实验iv、v,分析实验iv中Na2SO3的作用:
更新时间:2022-06-18 12:58:51
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)只用一种试剂或操作,除去下列物质中的杂质(括号内为杂质),先写出除杂时所选试剂或者操作,再写出发生的有关化学方程式。
①Fe2O3(Al2O3):___ ___
②FeCl2溶液(FeCl3):___ ___
③Na2CO3(NaHCO3):___ ___
(2)写出以下反应的化学方程式或离子方程式。
呼吸面具中CO2与过氧化钠反应化学方程式:___ ;
烧碱溶液与铝片的反应离子方程式:___ 。
①Fe2O3(Al2O3):
②FeCl2溶液(FeCl3):
③Na2CO3(NaHCO3):
(2)写出以下反应的化学方程式或离子方程式。
呼吸面具中CO2与过氧化钠反应化学方程式:
烧碱溶液与铝片的反应离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答下列问题:
(1)①磁性氧化铁的化学式是___________ ;② 的电子式是
的电子式是___________ 。
(2) 分子的空间结构为
分子的空间结构为___________ 。
(3)除去 粉末中混有的少量
粉末中混有的少量 ,所涉及的反应的化学方程式为
,所涉及的反应的化学方程式为___________ 。
(1)①磁性氧化铁的化学式是
 的电子式是
的电子式是(2)
 分子的空间结构为
分子的空间结构为(3)除去
 粉末中混有的少量
粉末中混有的少量 ,所涉及的反应的化学方程式为
,所涉及的反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学上研究物质的组成和性质时,首先要将所研究物质从混合物中分离出来,并加以提纯,下列情况除杂时选用哪种试剂,考虑应选用怎样的除杂方法,请按照要求填写
(1)除去Fe2O3中的Al2O3,所选试剂为___________ ,相关的离子反应方程式为___________ 。
(2)除去FeCl3中的FeCl2,所选试剂为___________ ,相关的化学反应方程式为___________ 。
(3)除去Na2CO3中混有的NaHCO3,除杂方法为___________ 。
(1)除去Fe2O3中的Al2O3,所选试剂为
(2)除去FeCl3中的FeCl2,所选试剂为
(3)除去Na2CO3中混有的NaHCO3,除杂方法为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某化学学习小组研究碳酸氢钠的性质。
(1)该组同学在盛有0.1 mol·L-1 NaHCO3溶液的试管中滴入1~2滴酚酞试液,溶液显浅红色。甲同学认为是NaHCO3水解使溶液显碱性,该反应的离子方程式是___________ 。
(2)乙同学认为该溶液中不仅存在HCO 的水解平衡,还存在HCO
的水解平衡,还存在HCO 的电离平衡,其电离方程式是
的电离平衡,其电离方程式是___________ 。查阅书籍获得常温下H2CO3的电离常数Ka1=4.3 ×10-7,Ka2=5.6 ×10-11。则HCO 的水解常数Kh =
的水解常数Kh =___________ (计算结果保留两位有效数字),由此可知HCO 的水解程度
的水解程度 ___________ (填“大于”“小于”或“等于”)HCO 的电离程度,因此NaHCO3溶液显碱性。
的电离程度,因此NaHCO3溶液显碱性。
(3)当加热滴有酚酞试液的NaHCO3溶液的试管时,溶液红色加深。实验测得该溶液的pH变化如下表所示。
关于这一现象,同学们提出两种可能的原因:
I.加热促进了HCO 的水解,溶液碱性增强;
的水解,溶液碱性增强;
II.NaHCO3受热分解生成Na2CO3,Na2CO3的水解程度大,溶液碱性增强。
丙同学将上述表格中所述50°C的溶液继续冷却至20 °C,测得pH=8.7,可得出结论:两种原因中起主要作用的是___________ (填“ I”或“II”)。
(4)丁同学发现,向0.1 mol· L-1NaHCO3溶液中滴加饱和CaCl2溶液时生成白色沉淀并产生无色无味的气体,经检验白色沉淀的成分是CaCO3,则反应的离子方程式为___________ 。
(5)该组同学发现,将等物质的量浓度的NaHCO3溶液与Na2CO3溶液混合后,向其中滴加少量盐酸时,混合液的pH几乎不变,请结合离子方程式解释产生该现象的原因是___________ 。
(1)该组同学在盛有0.1 mol·L-1 NaHCO3溶液的试管中滴入1~2滴酚酞试液,溶液显浅红色。甲同学认为是NaHCO3水解使溶液显碱性,该反应的离子方程式是
(2)乙同学认为该溶液中不仅存在HCO
 的水解平衡,还存在HCO
的水解平衡,还存在HCO 的电离平衡,其电离方程式是
的电离平衡,其电离方程式是 的水解常数Kh =
的水解常数Kh = 的水解程度
的水解程度  的电离程度,因此NaHCO3溶液显碱性。
的电离程度,因此NaHCO3溶液显碱性。(3)当加热滴有酚酞试液的NaHCO3溶液的试管时,溶液红色加深。实验测得该溶液的pH变化如下表所示。
| 温度/°C | 10 | 20 | 30 | 加热煮沸后冷却到50 °C |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
关于这一现象,同学们提出两种可能的原因:
I.加热促进了HCO
 的水解,溶液碱性增强;
的水解,溶液碱性增强;II.NaHCO3受热分解生成Na2CO3,Na2CO3的水解程度大,溶液碱性增强。
丙同学将上述表格中所述50°C的溶液继续冷却至20 °C,测得pH=8.7,可得出结论:两种原因中起主要作用的是
(4)丁同学发现,向0.1 mol· L-1NaHCO3溶液中滴加饱和CaCl2溶液时生成白色沉淀并产生无色无味的气体,经检验白色沉淀的成分是CaCO3,则反应的离子方程式为
(5)该组同学发现,将等物质的量浓度的NaHCO3溶液与Na2CO3溶液混合后,向其中滴加少量盐酸时,混合液的pH几乎不变,请结合离子方程式解释产生该现象的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______ c(HCO3-)(填“>”、“<”或“=”)。
②常温下,物质的量浓度相同的三种溶液:A.CH3COONa B.NaCN C.Na2CO3,其pH由大到小的顺序是________ (填编号)。
③将少量CO2通入NaCN溶液,反应的离子方程式是__________ 。
④室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是______ ,溶液中c(CH3COO-)/c(CH3COOH) =________ 。
(2)某温度下, pH=3的盐酸中[OH-]=10-9 mol/L. 该温度下, pH=2的H2SO4与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为______ .
(3)室温下,用0.100 mol/L盐酸溶液滴定20.00mL 0.l00mol/L 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。

①d点所示的溶液中离子浓度由大到小的顺序依次为_____ 。
②b点所示的溶液中c(NH4+)-c(NH3·H2O)=______ (写出准确数值)。
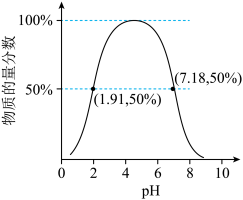
(4)在SO2溶于水形成的二元弱酸溶液中,含S元素的某微粒占所有含S元素微粒的物质的量分数与溶液pH的关系如下图所示,该微粒的化学式为_______ ;该二元弱酸的一级电离常数为Ka1,则pKa1=-lgKa1≈____ 。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka = 1.8×10-5 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
①0.1 mol/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)
②常温下,物质的量浓度相同的三种溶液:A.CH3COONa B.NaCN C.Na2CO3,其pH由大到小的顺序是
③将少量CO2通入NaCN溶液,反应的离子方程式是
④室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是
(2)某温度下, pH=3的盐酸中[OH-]=10-9 mol/L. 该温度下, pH=2的H2SO4与pH=11的NaOH混合后pH变为9,则硫酸与氢氧化钠的体积比为
(3)室温下,用0.100 mol/L盐酸溶液滴定20.00mL 0.l00mol/L 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。

①d点所示的溶液中离子浓度由大到小的顺序依次为
②b点所示的溶液中c(NH4+)-c(NH3·H2O)=
(4)在SO2溶于水形成的二元弱酸溶液中,含S元素的某微粒占所有含S元素微粒的物质的量分数与溶液pH的关系如下图所示,该微粒的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。请回答以下问题:

(1)B、D的电极名称分别是______ 、______ 。
(2)C极可以选用的材料是______ (填标号)。
(3)该装置开始工作时,Cl-向______ 极(填“C”或“D”)移动,工作一段时间后观察到D极的现象是______ ,C极发生的电极反应为______ 。
(4)甲装置中K+向______ 极(填“A”或“B”)移动,A极发生的电极反应为______ 。
(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为______ 。
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接______ (填“A”或“B”)极。

(1)B、D的电极名称分别是
(2)C极可以选用的材料是
| A.铁棒 | B.银棒 | C.石墨棒 | D.铜棒 |
(3)该装置开始工作时,Cl-向
(4)甲装置中K+向
(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答以下问题:
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.

Ⅱ.
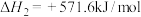
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式__________ 。
(2)在 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(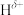 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(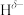 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是__________ 。
(3)100mLpH=10.00的 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为__________ mol。
(4)已知:25℃时碳酸的 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式__________ 。
(5)据文献报道, 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是__________ 。
(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是__________ 。
(7)乙醇的挥发性比水的强,原因是__________ 。
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.


Ⅱ.

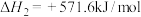
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
(2)在
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(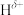 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(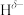 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是(3)100mLpH=10.00的
 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为(4)已知:25℃时碳酸的
 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式(5)据文献报道,
 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(7)乙醇的挥发性比水的强,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硫及其主要的化合物在化学研究及生产生活中都有重要的应用。
I.探究一:认识硫化钠
工业污水中含有的重金属离子(例如Cu2+、Pb2+)可以形成硫化物沉淀而除去,这种方法叫硫化钠沉淀法。(提示:CuS是一种不溶于酸也不溶于水的黑色固体)
(1)利用Na2S处理污水中的铜离子,该反应过程的离子方程式为_______
(2)从硫元素化合价的角度,Na2S具有什么性质_______ 。小荟同学预测硫化钠溶液可以与氯气发生氧化还原反应。他将不同浓度的硫化钠溶液分别注入两支盛有氯气的采集管中,振荡混合反应,发现其中一支试管中产生淡黄色沉淀物。据此写出发生反应的化学方程式_______ 得出的结论是Cl-的还原性_______ S2-(填“强于”或“弱于”)。另一支试管中无明显现象,小荟推测生成物可能为亚硫酸钠或硫酸钠。
(3)在Na2SO4和Na2SO3可能存在的体系中,如何检验 ?请用文字将检验过程描述完整,取少量反应后的混合溶液,
?请用文字将检验过程描述完整,取少量反应后的混合溶液,_______
II.探究二:认识亚硫酸钠
化学课上并未系统学习过亚硫酸钠,所以小荟针对亚硫酸钠的性质展开了归纳和探究。
(4)从元素化合价角度思考,Na2SO3应具有氧化性和还原性。据此预测亚硫酸钠与酸性高锰酸钾溶液反应的现象为_______
(5)她还预测亚硫酸钠与硫化钠溶液混合,应产生淡黄色沉淀,做实验时却观察到并无明显现象,你能推测原因或提出解决办法吗?_______
(6)取3.5g长期存放的Na2SO3粉末(可能部分氧化为Na2SO4),加入过量的100mL某浓度的盐酸中,加热使生成的气体全部逸出,测得该气体在标准状况下的体积为560mL,然后向溶液中渐渐加入0.5mol/L的Ba(OH)2溶液50mL,有沉淀生成,此时溶液呈中性。求Na2SO3的纯度_______ ;
I.探究一:认识硫化钠
工业污水中含有的重金属离子(例如Cu2+、Pb2+)可以形成硫化物沉淀而除去,这种方法叫硫化钠沉淀法。(提示:CuS是一种不溶于酸也不溶于水的黑色固体)
(1)利用Na2S处理污水中的铜离子,该反应过程的离子方程式为
(2)从硫元素化合价的角度,Na2S具有什么性质
(3)在Na2SO4和Na2SO3可能存在的体系中,如何检验
 ?请用文字将检验过程描述完整,取少量反应后的混合溶液,
?请用文字将检验过程描述完整,取少量反应后的混合溶液,II.探究二:认识亚硫酸钠
化学课上并未系统学习过亚硫酸钠,所以小荟针对亚硫酸钠的性质展开了归纳和探究。
(4)从元素化合价角度思考,Na2SO3应具有氧化性和还原性。据此预测亚硫酸钠与酸性高锰酸钾溶液反应的现象为
(5)她还预测亚硫酸钠与硫化钠溶液混合,应产生淡黄色沉淀,做实验时却观察到并无明显现象,你能推测原因或提出解决办法吗?
(6)取3.5g长期存放的Na2SO3粉末(可能部分氧化为Na2SO4),加入过量的100mL某浓度的盐酸中,加热使生成的气体全部逸出,测得该气体在标准状况下的体积为560mL,然后向溶液中渐渐加入0.5mol/L的Ba(OH)2溶液50mL,有沉淀生成,此时溶液呈中性。求Na2SO3的纯度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_____ (选填编号)。
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。
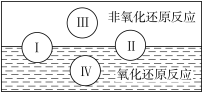
试写出有水参加且符合反应类型 IV 的一个化学方程式:___________________ 。
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
_____ NaIO3+ NaHSO3→ I2+ Na2SO4+ H2SO4+ H2O
②该反应还原剂是_____ ,_____ 元素被还原,若生成 1mol 氧化产物则转移电子数目为_____ NA。
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-_____ I-(填“>”或“<”),完成该反应_____________________________________ 。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。

试写出有水参加且符合反应类型 IV 的一个化学方程式:
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
②该反应还原剂是
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-
您最近一年使用:0次

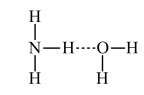 B.
B.

 、
、 、
、 、
、 、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:
、Cl-、K+等八种离子,向其中加入Na2O2粉末,则:

