新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。请回答以下问题:

(1)B、D的电极名称分别是______ 、______ 。
(2)C极可以选用的材料是______ (填标号)。
(3)该装置开始工作时,Cl-向______ 极(填“C”或“D”)移动,工作一段时间后观察到D极的现象是______ ,C极发生的电极反应为______ 。
(4)甲装置中K+向______ 极(填“A”或“B”)移动,A极发生的电极反应为______ 。
(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为______ 。
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接______ (填“A”或“B”)极。

(1)B、D的电极名称分别是
(2)C极可以选用的材料是
| A.铁棒 | B.银棒 | C.石墨棒 | D.铜棒 |
(3)该装置开始工作时,Cl-向
(4)甲装置中K+向
(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接
更新时间:2024-03-30 08:28:46
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.某同学做如下实验,以探究反应中的能量变化。

(1)在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是________ 热反应;(b)中温度降低,由此可以判断(b)中反应是________ 热反应。
(2)根据能量守恒定律,(b)中反应物的总能量应该________ 生成物的总能量。
II.某学习小组依据氧化还原反应原理:2Ag++Cu=Cu2++2Ag设计成的原电池如右图所示。
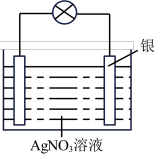
(3) 从能量转化角度分析,上述原电池将化学能转化为_________ ;
(4) 负极的电极材料为_____________ ;
(5) 正极发生的电极反应__________________________________ ;

(1)在实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是
(2)根据能量守恒定律,(b)中反应物的总能量应该
II.某学习小组依据氧化还原反应原理:2Ag++Cu=Cu2++2Ag设计成的原电池如右图所示。

(3) 从能量转化角度分析,上述原电池将化学能转化为
(4) 负极的电极材料为
(5) 正极发生的电极反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有A、B、C、D四种金属片,把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;把A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向由A经过导线到C。根据上述情况,回答下列问题:
(1)在中,金属片_______ 发生氧化反应
(2)在中,金属片_______ 做负极
(3)在中,电流流动方向为_______ 。
(4)如果把B、D用导线连接后同时浸入稀硫酸溶液中,则金属片_______ 上有气泡产生
(5)上述四种金属的活动顺序是_______ 。
(1)在中,金属片
(2)在中,金属片
(3)在中,电流流动方向为
(4)如果把B、D用导线连接后同时浸入稀硫酸溶液中,则金属片
(5)上述四种金属的活动顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】降低能耗是氯碱工业发展的重要方向。我国利用氯碱厂生产的H2作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。
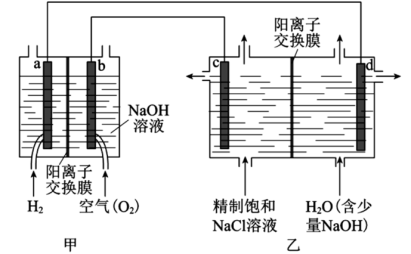
(1)a极为_______ (填“正”或“负”)极,c 极为_______ (填“阴”或“阳”)极。
(2)乙装置中电解饱和NaCl溶液的化学方程式为_______ ;反应一段时间后,d极产生1mol气体时,乙装置中转移电子_______ mol。
(3)下列说法正确的是_______ (填字母序号)。
A.甲装置可实现化学能向电能的转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是浓盐水
(4)实际生产中,阳离子交换膜的损伤会造成OH- 迁移至阳极区,从而在电解池阳极能检测到O2,产生O2的电极反应式为_______ 。

(1)a极为
(2)乙装置中电解饱和NaCl溶液的化学方程式为
(3)下列说法正确的是
A.甲装置可实现化学能向电能的转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是浓盐水
(4)实际生产中,阳离子交换膜的损伤会造成OH- 迁移至阳极区,从而在电解池阳极能检测到O2,产生O2的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】水是宝贵的自然资源,水的净化与污水处理是化学工作者需要研究的重要课题。
(1)在净水过程中用到混凝剂,其中不可以作为混凝剂使用的是__________ 。
A.硫酸铝 B.氧化铝 C.碱式氯化铝 D.氯化铁
(2)海水淡化是人类获得饮用水的一个重要方法,下列有关海水淡化处理的方法正确的是_____ 。
A.蒸馏法能耗最小,设备最简单;冷冻法要消耗大量能源
B.利用电渗析法淡化海水时,在阴极附近放阴离子交换膜,在阳极附近放阳离子交换膜
C.利用电渗析法淡化海水时,得到淡水的部分在中间区
D.利用反渗透技术可以大量、快速地生产淡水
(3)除了水资源,能源、信息、材料一起构成了现代文明的三大支柱。甲醇是一种重要的化工原料,以甲醇、氧气为基本反应物的新型燃料电池已经问世,其结构如图所示(甲醇解离产生的H+可以通过质子交换膜进入另一极)。请写出通入甲醇的电极上的电极反应式:____________ 。
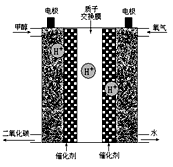
某同学以甲醇燃料电池为电源,以石墨为电极电解500mL 0.2mol·L1 CuSO4溶液,则与电源正极相连的电解池电极上的电极反应式为:_______________________________ ;电解一段时间后,在电解池两极上共产生7.84 L气体(标准状况下),此时甲醇燃料电池中共消耗甲醇_________ g 。
(1)在净水过程中用到混凝剂,其中不可以作为混凝剂使用的是
A.硫酸铝 B.氧化铝 C.碱式氯化铝 D.氯化铁
(2)海水淡化是人类获得饮用水的一个重要方法,下列有关海水淡化处理的方法正确的是
A.蒸馏法能耗最小,设备最简单;冷冻法要消耗大量能源
B.利用电渗析法淡化海水时,在阴极附近放阴离子交换膜,在阳极附近放阳离子交换膜
C.利用电渗析法淡化海水时,得到淡水的部分在中间区
D.利用反渗透技术可以大量、快速地生产淡水
(3)除了水资源,能源、信息、材料一起构成了现代文明的三大支柱。甲醇是一种重要的化工原料,以甲醇、氧气为基本反应物的新型燃料电池已经问世,其结构如图所示(甲醇解离产生的H+可以通过质子交换膜进入另一极)。请写出通入甲醇的电极上的电极反应式:

某同学以甲醇燃料电池为电源,以石墨为电极电解500mL 0.2mol·L1 CuSO4溶液,则与电源正极相连的电解池电极上的电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】试运用所学的电化学知识回答下列问题:
(1)①请设计一个原电池,可自发进行反应: ,该电池的两电极分别为铜棒、银棒,请画出该实验的装置示意图:
,该电池的两电极分别为铜棒、银棒,请画出该实验的装置示意图:_______ 。该电池中,电子的流向为_______ 。
②该电化学装置的能量变化形式为_______ 。若开始时两电极质量相等,当电路中转移0.2mol电子时,理论上两电极的质量差为_______ g。
(2)科学家用氮化镓材料与铜组装成如图所示的人工光合系统实现 的再利用。电池的总反应为
的再利用。电池的总反应为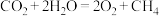 (已知:质子交换膜仅允许
(已知:质子交换膜仅允许 通过)。
通过)。_______ (填“GaN”或“Cu”)。
②该电池的Cu电极上发生的电极反应为_______ 。
③生成 ,消耗
,消耗 的物质的量为
的物质的量为_______ mol。
(1)①请设计一个原电池,可自发进行反应:
 ,该电池的两电极分别为铜棒、银棒,请画出该实验的装置示意图:
,该电池的两电极分别为铜棒、银棒,请画出该实验的装置示意图:②该电化学装置的能量变化形式为
(2)科学家用氮化镓材料与铜组装成如图所示的人工光合系统实现
 的再利用。电池的总反应为
的再利用。电池的总反应为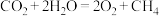 (已知:质子交换膜仅允许
(已知:质子交换膜仅允许 通过)。
通过)。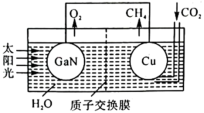
②该电池的Cu电极上发生的电极反应为
③生成
 ,消耗
,消耗 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)资料表明AgNO3溶液和KI溶液能发生反应:2Ag++2I-=2Ag+I2 △H<0,某同学设计如图实验装置证实了这一信息。

可供选择的用品:烧杯、直流电源、导线、盐桥、灵敏电流计、石墨棒、铁棒、银棒、KI溶液、AgNO3溶液、淀粉溶液
①电极材料A为_______ ,Y溶液是_______ ,为使实验现象更加明显,需向X溶液或Y溶液中加入的试剂是_______ 。
②负极反应物为_______ ,正极电极反应式为_______ 。
(2)氯碱工业的示意图如下,回答下列问题。
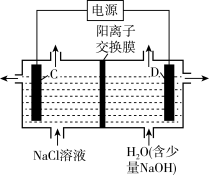
①D电极反应式为_______ ;实际生产中,阳离子交换膜的损伤会造成OH-迁移至阳极区,从而在电解池阳极上能检测到O2,下列生产措施有利于提高Cl2产量、降低阳极O2含量的是_______ 。
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用精制饱和食盐水提高c(Cl-)
②降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2,避免水电离的H+直接得电子生成H2,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为_______ 。
(1)资料表明AgNO3溶液和KI溶液能发生反应:2Ag++2I-=2Ag+I2 △H<0,某同学设计如图实验装置证实了这一信息。

可供选择的用品:烧杯、直流电源、导线、盐桥、灵敏电流计、石墨棒、铁棒、银棒、KI溶液、AgNO3溶液、淀粉溶液
①电极材料A为
②负极反应物为
(2)氯碱工业的示意图如下,回答下列问题。

①D电极反应式为
A.定期检查并更换阳离子交换膜
B.向阳极区加入适量盐酸
C.使用精制饱和食盐水提高c(Cl-)
②降低氯碱工业能耗的另一种技术是“氧阴极技术”。通过向阴极区通入O2,避免水电离的H+直接得电子生成H2,降低了电解电压,电耗明显减少。“氧阴极技术”的阴极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电解是最强有力的氧化还原手段,在化工生产中有着重要的应用。请回答下列问题:
(1)以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为________ ,阴极反应式为________ 。
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是
_______ (填序号)。

a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2OCH3CH2OH+CH3COOH

实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入________ (填化学式),电极反应式为________ 。电解过程中,阴极区Na2SO4的物质的量________ (填“增大”、“减小”或“不变”)。
②在实际工艺处理中,阴极区乙醛的去除率可达60%。若在两极区分别注入1 m3乙醛含量为3 000 mg/L的废水,可得到乙醇________ kg(计算结果保留小数点后一位)。
(1)以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是

a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2OCH3CH2OH+CH3COOH

实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入
②在实际工艺处理中,阴极区乙醛的去除率可达60%。若在两极区分别注入1 m3乙醛含量为3 000 mg/L的废水,可得到乙醇
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在硫酸铜溶液中,插入两个电极进行电解。
(1)若两极均为Pt电极,则阳极反应式是_________ ,阴极反应式是_________ ,电解的化学方程式是_________ 。
(2)若两极均为铜片,则阳极反应式是_________ ,阴极反应式是_________ ,电解过程中溶液的浓度变化是_________ 。
(3)若阳极为锌片,阴极为铜片,则阳极反应式是_________ ,电解过程中两极的变化是_________ 。
(1)若两极均为Pt电极,则阳极反应式是
(2)若两极均为铜片,则阳极反应式是
(3)若阳极为锌片,阴极为铜片,则阳极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某课外活动小组用如图装置进行实验,试回答下列问题:
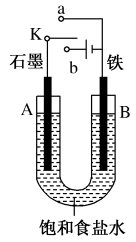
(1)若开始时开关K与a连接,则A极的电极反应式为____________________ B极的Fe发生__________ 腐蚀(填“析氢”或“吸氧”)
(2)若开始时开关K与b连接,下列说法正确的是________ (填序号)
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子且此时装置内总反应的离子方程式为_________
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为______________ ,此时通过阴离子交换膜的离子数________ (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口________ (填“A”“B”“C”或“D”)导出。

(1)若开始时开关K与a连接,则A极的电极反应式为
(2)若开始时开关K与b连接,下列说法正确的是
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子且此时装置内总反应的离子方程式为
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为
②制得的氢氧化钾溶液从出口
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】人工肾脏可用间接电化学方法除去代谢产物中的尿素(化学式 ),原理如下图。
),原理如下图。

(1)阳极室中发生的反应依次有:_______ 、_______ 。
(2)电解结束后,若两极共收集到气体13.44L(标准状况),则除去的尿素为_______ g(忽略气体的溶解,下同)。
(3)若关闭左下侧与左上侧溶液的导入导出,当电解过程中转移了2mol电子,则质子交换膜两侧电解液的质量变化差 为
为_______ g。
 ),原理如下图。
),原理如下图。
(1)阳极室中发生的反应依次有:
(2)电解结束后,若两极共收集到气体13.44L(标准状况),则除去的尿素为
(3)若关闭左下侧与左上侧溶液的导入导出,当电解过程中转移了2mol电子,则质子交换膜两侧电解液的质量变化差
 为
为
您最近一年使用:0次
【推荐2】根据电化学原理,回答下列问题。
(1)如图所示用惰性电极电解 溶液,
溶液, 电极上的电极反应式为
电极上的电极反应式为 ___________ ,若 电极产生
电极产生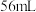 (标准状况)气体,则所得溶液的
(标准状况)气体,则所得溶液的
___________ (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入___________ (填字母)。

A. B.
B. C.
C. D.
D.
(2)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如下图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入 和空气,其中固体电解质是掺杂了
和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导
固体,它在高温下能传导 。则
。则 电极的名称为
电极的名称为___________ , 电极上的电极反应
电极上的电极反应___________ 。

(3)利用如图的装置电解饱和食盐水,制备一种家用“84”消毒液(有效成分为 )发生器,在制备消毒液时,
)发生器,在制备消毒液时, 电极上的电极反应式为
电极上的电极反应式为___________ 。

(1)如图所示用惰性电极电解
 溶液,
溶液, 电极上的电极反应式为
电极上的电极反应式为  电极产生
电极产生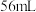 (标准状况)气体,则所得溶液的
(标准状况)气体,则所得溶液的

A.
 B.
B. C.
C. D.
D.
(2)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如下图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入
 和空气,其中固体电解质是掺杂了
和空气,其中固体电解质是掺杂了 的
的 固体,它在高温下能传导
固体,它在高温下能传导 。则
。则 电极的名称为
电极的名称为 电极上的电极反应
电极上的电极反应
(3)利用如图的装置电解饱和食盐水,制备一种家用“84”消毒液(有效成分为
 )发生器,在制备消毒液时,
)发生器,在制备消毒液时, 电极上的电极反应式为
电极上的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】用间接电化学法除去NO的过程,如图所示:
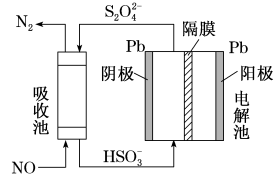
(1)已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:_______ 。用离子方程式表示吸收池中除去NO的原理:_______ 。
(2)目前已开发出电解法制取ClO2的新工艺。
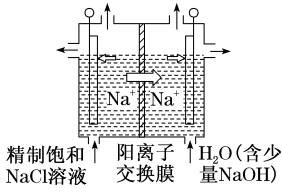
①用石墨作电极,在一定条件下电解饱和食盐水制取ClO2(如图所示),写出阳极产生ClO2的电极反应式:_______ 。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解,通过阳离子交换膜的阳离子的物质的量为_______ mol;用平衡移动原理解释阴极区pH增大的原因:_______ 。

(1)已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式:
(2)目前已开发出电解法制取ClO2的新工艺。

①用石墨作电极,在一定条件下电解饱和食盐水制取ClO2(如图所示),写出阳极产生ClO2的电极反应式:
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解,通过阳离子交换膜的阳离子的物质的量为
您最近一年使用:0次



