氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是__________ (至少答出两点)。
(2)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为________________________________________________________________________ 。
(1)与汽油相比,氢气作为燃料的优点是
(2)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
18-19高一·全国·假期作业 查看更多[2]
更新时间:2019-05-20 09:03:05
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】请运用图示概括你对“化学反应过程中的能量转化与利用”的认识________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成下列问题。
(1)常温下,0.1molCl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28kJ,该反应的热化学方程式为_______ 。
(2)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。已知:
①2O2(g)+N2(g)=N2O4(1) △H1
②N2(g)+2H2(g)=N2H4(1) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=_______ ,联氨和N2O4可作为火箭推进剂的主要原因为_______ 。
(3)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
①与汽油相比,氢气作为燃料的优点是_______ (至少答出两点)。
②利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______ 。
(1)常温下,0.1molCl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28kJ,该反应的热化学方程式为
(2)联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。已知:
①2O2(g)+N2(g)=N2O4(1) △H1
②N2(g)+2H2(g)=N2H4(1) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=
(3)氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
①与汽油相比,氢气作为燃料的优点是
②利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】放热反应和吸热反应
(1)化学反应中的能量变化
若反应物的能量小于生成物的能量,则反应过程中___________ 能量;若反应物的能量大于生成物的能量,则反应过程中___________ 能量。
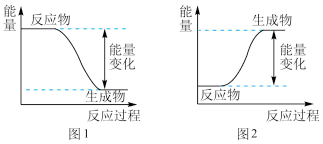
下图中,图1表示___________ 反应,图2表示___________ 反应。
(2)放热反应和吸热反应
___________ 热的反应称为吸热反应,吸热反应的ΔH___________ 0。
___________ 热的反应称为放热反应,反热反应的ΔH___________ 0。
(3)常见的放热反应和吸热反应
根据反应过程中放出或吸收能量,可将化学反应分为放热反应和吸热反应。
常见的放热反应有:①燃烧反应;②中和反应;③金属与水或酸反应放出氢气;④大多数化合反应;⑤铝热反应。
常见的吸热反应有:①大多数分解反应;②需要持续加热的反应;③CO2+C 2CO,C+H2O
2CO,C+H2O CO+H2;④铵盐与碱的反应,如Ba(OH)2、Ca(OH)2与NH4Cl的反应。
CO+H2;④铵盐与碱的反应,如Ba(OH)2、Ca(OH)2与NH4Cl的反应。
(4)放热过程和吸热过程
物质在发生物理变化时,也会放出或吸收能量。
常见的放热过程有:①浓硫酸稀释、NaOH溶于水;②物态变化:气态→液态→固态
常见的吸热过程有:①NH4NO3溶于水;②弱电解质的电离;③物态变化:固态→液态→气体
(1)化学反应中的能量变化
若反应物的能量小于生成物的能量,则反应过程中
下图中,图1表示

(2)放热反应和吸热反应
(3)常见的放热反应和吸热反应
根据反应过程中放出或吸收能量,可将化学反应分为放热反应和吸热反应。
常见的放热反应有:①燃烧反应;②中和反应;③金属与水或酸反应放出氢气;④大多数化合反应;⑤铝热反应。
常见的吸热反应有:①大多数分解反应;②需要持续加热的反应;③CO2+C
 2CO,C+H2O
2CO,C+H2O CO+H2;④铵盐与碱的反应,如Ba(OH)2、Ca(OH)2与NH4Cl的反应。
CO+H2;④铵盐与碱的反应,如Ba(OH)2、Ca(OH)2与NH4Cl的反应。(4)放热过程和吸热过程
物质在发生物理变化时,也会放出或吸收能量。
常见的放热过程有:①浓硫酸稀释、NaOH溶于水;②物态变化:气态→液态→固态
常见的吸热过程有:①NH4NO3溶于水;②弱电解质的电离;③物态变化:固态→液态→气体
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】目前,我国使用的能源主要是煤、石油、天然气等,这些能源都是不可再生且污染环境的能源,研究和开发清洁而又用之不竭的能源是未来发展的首要任务。科学家预测氢能将是21世纪最理想的新能源之一。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气。下列可供开发又较经济且资源可持续利用的制氢气的方法是________ (填序号)。
A.电解水 B.锌和稀硫酸反应 C.光解海水
(2)以甲烷为原料制取氢气是工业上常用的制氢方法。
已知:



由甲烷制氢气的一个缺点是________ 。
(3)将 进行热分解也可以制得氢气
进行热分解也可以制得氢气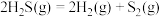
 。热分解制氢气时,常向反应器中通入一定比例的空气,使部分
。热分解制氢气时,常向反应器中通入一定比例的空气,使部分 燃烧,其目的是
燃烧,其目的是_________________________ 。
(4)镁铝合金(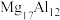 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的 、
、 单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为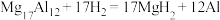 得到的混合物
得到的混合物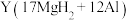 在一定条件下可释放出氢气。
在一定条件下可释放出氢气。
①熔炼制备镁铝合金(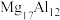 )时通入氩气的目的是
)时通入氩气的目的是____________________________________ 。
②在足量的 的
的 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。
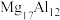 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量为
的物质的量为________ 。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气。下列可供开发又较经济且资源可持续利用的制氢气的方法是
A.电解水 B.锌和稀硫酸反应 C.光解海水
(2)以甲烷为原料制取氢气是工业上常用的制氢方法。
已知:




由甲烷制氢气的一个缺点是
(3)将
 进行热分解也可以制得氢气
进行热分解也可以制得氢气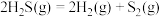
 。热分解制氢气时,常向反应器中通入一定比例的空气,使部分
。热分解制氢气时,常向反应器中通入一定比例的空气,使部分 燃烧,其目的是
燃烧,其目的是(4)镁铝合金(
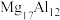 )是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的 、
、 单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为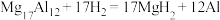 得到的混合物
得到的混合物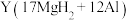 在一定条件下可释放出氢气。
在一定条件下可释放出氢气。①熔炼制备镁铝合金(
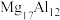 )时通入氩气的目的是
)时通入氩气的目的是②在足量的
 的
的 溶液中,混合物Y能完全释放出
溶液中,混合物Y能完全释放出 。
。
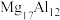 完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出
完全吸氢后得到的混合物Y与上述盐酸完全反应,释放出 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是____________ (至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:__________________ 。
(2)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为__________________ 。
(1)与汽油相比,氢气作为燃料的优点是
(2)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】有效地利用现有新能源和开发新能源已受到各国的重视。
(1)可用改进汽油组成的办法来改善汽油的燃烧性能。例如,在汽油中加入乙醇来生产“无铅汽油”。乙醇的分子式为C2H6O,试根据C、H、O成键的特点,写出C2H6O所有可能的结构式或结构简式__________________ 。
(2)天然气的主要的成分是甲烷,其燃烧产物无毒、热值高、管道输送方便,将成为我国西部开发的重点之一。能说明甲烷是正四面体而非正方形平面结构的理由是__________ 。(填写编号)
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体
③其三氯取代物不存在同分异构体 ④其四氯取代物不存在同分异构体
(3)氢能是人类未来的理想能源。1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h的速度行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气。下列既可行又经济的制氢方法是__________ (填写编号)
①电解水 ②锌和稀硫酸反应 ③光解海水
其次,制得纯氢气后,还需要解决的问题是______________________ 。(写出其中的一个)
(4)今有两个氢气燃烧生成水的热化学方程式
2H2(g)+ O2(g) ="=" 2H2O(g) △H=a kJ/mol
2H2(g)+ O2(g) ==2H2O(l) △H=b kJ/mol
请回答下列问题:(提示:︱b︱表示b的绝对值)
①若2 molH2完全燃烧生成水蒸气,则放出的热量__ (填“>”、“<”或“=”)︱b︱kJ
②若已知拆开1mol氢气中的化学键要消耗436 kJ能量,拆开1mol氧气中的化学键要消耗496kJ能量,水蒸气中1molH—O键形成时放出热量463kJ,写出该反应的热化学方程式:
___________________________________________________________________
(1)可用改进汽油组成的办法来改善汽油的燃烧性能。例如,在汽油中加入乙醇来生产“无铅汽油”。乙醇的分子式为C2H6O,试根据C、H、O成键的特点,写出C2H6O所有可能的结构式或结构简式
(2)天然气的主要的成分是甲烷,其燃烧产物无毒、热值高、管道输送方便,将成为我国西部开发的重点之一。能说明甲烷是正四面体而非正方形平面结构的理由是
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体
③其三氯取代物不存在同分异构体 ④其四氯取代物不存在同分异构体
(3)氢能是人类未来的理想能源。1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h的速度行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气。下列既可行又经济的制氢方法是
①电解水 ②锌和稀硫酸反应 ③光解海水
其次,制得纯氢气后,还需要解决的问题是
(4)今有两个氢气燃烧生成水的热化学方程式
2H2(g)+ O2(g) ="=" 2H2O(g) △H=a kJ/mol
2H2(g)+ O2(g) ==2H2O(l) △H=b kJ/mol
请回答下列问题:(提示:︱b︱表示b的绝对值)
①若2 molH2完全燃烧生成水蒸气,则放出的热量
②若已知拆开1mol氢气中的化学键要消耗436 kJ能量,拆开1mol氧气中的化学键要消耗496kJ能量,水蒸气中1molH—O键形成时放出热量463kJ,写出该反应的热化学方程式:
您最近一年使用:0次



