某化学兴趣小组,利用如图所示装置探究元素非金属性强弱的变化规律。

(1)仪器A的名称为_________ ,干燥管D的作用是_____ 。
(2)实验室中现有药品Na2S、浓盐酸、稀硫酸、MnO2,请选择合适药品设计实验探究氯和硫的非金属性强弱(必要时可以加热,图中省略):
①装置A中所装药品为_________ 。
②装置C中的实验现象为:有淡黄色沉淀生成,该装置中的化学反应方程式为__________ 。
③根据该实验探究出的结果,可知HCl的稳定性比H2S的稳定性____ 。(填“强”或“弱”)
(3)若要探究硫和碳元素的非金属性强弱,B、C中所装药品分别为Na2CO3固体、澄清石灰水,则A中反应的离子方程式为__________ ,观察到C装置中的现象为_________ 。

(1)仪器A的名称为
(2)实验室中现有药品Na2S、浓盐酸、稀硫酸、MnO2,请选择合适药品设计实验探究氯和硫的非金属性强弱(必要时可以加热,图中省略):
①装置A中所装药品为
②装置C中的实验现象为:有淡黄色沉淀生成,该装置中的化学反应方程式为
③根据该实验探究出的结果,可知HCl的稳定性比H2S的稳定性
(3)若要探究硫和碳元素的非金属性强弱,B、C中所装药品分别为Na2CO3固体、澄清石灰水,则A中反应的离子方程式为
更新时间:2019-05-28 11:08:03
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学为验证元素周期表中元素性质的递变规律,设计了如下系列实验。
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:_______ 与盐酸反应最剧烈,_______ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_______ 。
(3)利用下图装置可验证同主族非金属性的变化规律。

①若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,请写出C中的离子反应方程式_______ 。
②若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3,C中加Na2SiO3溶液,请写出C中的反应现象_______ 。该实验能否 _______ (填“能”或“否”)证明非金属性Cl>C。
(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
(3)利用下图装置可验证同主族非金属性的变化规律。

①若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,请写出C中的离子反应方程式
②若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3,C中加Na2SiO3溶液,请写出C中的反应现象
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】利用下图装置可以验证非金属性的变化规律。
(1)仪器A的名称为________ ,球形管D的作用是________ 。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________ 、________ 、________ ,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为____________________________________________________________ 。
(3)若要证明非金属性:C>Si,则A中加________ 、B中加Na2CO3、C中加________ ,观察到C中溶液的现象为_____________________________

(1)仪器A的名称为
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为
(3)若要证明非金属性:C>Si,则A中加

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次加入大小相近的钠、镁、铝、钾金属块,通过观察现象判断金属性的相对强弱。
(1)反应最剧烈的烧杯中的金属是____ (填字母)。
(2)实验中发现b、c两只烧杯中几乎没有什么现象,要想达到实验目的,请你帮他选出合适的方法____ (填字母)。
A.把烧杯中的冷水换成热水
B.把烧杯中的冷水换成盐酸
C.把烧杯中的冷水换成浓硝酸
Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱.根据要求完成下列各题。(已知酸性强弱:亚硫酸>碳酸)

(3)实验步骤:连接仪器、____ 、加药品后,打开a,然后滴入浓硫酸,加热。
(4)问题探究:
①装置E中酸性KMnO4溶液的作用是____ 。
②试管F中发生反应的离子方程式为____ 。
③能说明非金属性碳强于硅的实验现象是____ 。
④依据试管D中的反应,能否证明非金属性硫强于碳?____ (填“能”或“否”)。
Ⅰ.甲同学在a、b、c、d四只烧杯中分别加入50mL冷水,再各滴加几滴酚酞试液,依次加入大小相近的钠、镁、铝、钾金属块,通过观察现象判断金属性的相对强弱。
(1)反应最剧烈的烧杯中的金属是
| A.钠 | B.镁 | C.铝 | D.钾 |
A.把烧杯中的冷水换成热水
B.把烧杯中的冷水换成盐酸
C.把烧杯中的冷水换成浓硝酸
Ⅱ.乙同学设计实验探究碳、硅元素的非金属性的相对强弱.根据要求完成下列各题。(已知酸性强弱:亚硫酸>碳酸)

(3)实验步骤:连接仪器、
(4)问题探究:
①装置E中酸性KMnO4溶液的作用是
②试管F中发生反应的离子方程式为
③能说明非金属性碳强于硅的实验现象是
④依据试管D中的反应,能否证明非金属性硫强于碳?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】乐山某高中化学兴趣小组同学用西红柿(或洋葱)作为供水剂,设计了如图装置验证铁与水蒸气的反应,并对产物进行检验。回答下列问题:
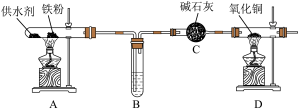
(1)A中铁与水蒸气反应的化学方程式是__ 。
(2)C中碱石灰的作用是__ 。
(3)D处实验现象为__ 。
(4)上述实验结束后,取出A中铁粉反应后的少量固体继续进行如下实验:

(Ⅰ)固体A中Fe3O4与稀硫酸反应的离子方程式为__ 。
(Ⅱ)试剂A是__ (选填字母)。
a.NaOH溶液 b.酸性KMnO4溶液 c.酚酞 d.新制氯水
(Ⅲ)有同学认为;即使得到了现象1和现象2的实验现象,也不能确定所得固体成分为Fe3O4。你认为该同学持此看法的理由是__ 。

(1)A中铁与水蒸气反应的化学方程式是
(2)C中碱石灰的作用是
(3)D处实验现象为
(4)上述实验结束后,取出A中铁粉反应后的少量固体继续进行如下实验:

(Ⅰ)固体A中Fe3O4与稀硫酸反应的离子方程式为
(Ⅱ)试剂A是
a.NaOH溶液 b.酸性KMnO4溶液 c.酚酞 d.新制氯水
(Ⅲ)有同学认为;即使得到了现象1和现象2的实验现象,也不能确定所得固体成分为Fe3O4。你认为该同学持此看法的理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某小组同学用如图所示装置制取NH3,并探究其性质及转化。
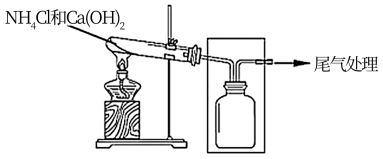
(1)试管中发生反应的化学方程式是_______ 。
(2)请将方框中的收集装置补充完整_______ 。
(3)将蘸有浓盐酸的棉球放在玻璃片上,再将集满NH3的集气瓶扣住棉球,可观察到的现象是_______ 。
(4)将如图滴管中的水挤入烧瓶中,打开止水夹。
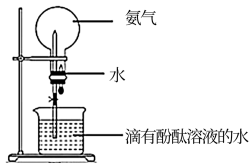
①可以观察到的现象是_______ 。
②通过该实验可以得到的结论有_______ 。
(5)NH3可以转化为其他含氮物质,如图为NH3转化为HNO3的流程。
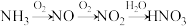
①写出NH3与O2反应转化为NO的化学方程式_______ 。
②NH3转化为HNO3的整个过程中,为提高氮原子的利用率,可采取的措施是_______ 。

(1)试管中发生反应的化学方程式是
(2)请将方框中的收集装置补充完整
(3)将蘸有浓盐酸的棉球放在玻璃片上,再将集满NH3的集气瓶扣住棉球,可观察到的现象是
(4)将如图滴管中的水挤入烧瓶中,打开止水夹。

①可以观察到的现象是
②通过该实验可以得到的结论有
(5)NH3可以转化为其他含氮物质,如图为NH3转化为HNO3的流程。
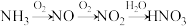
①写出NH3与O2反应转化为NO的化学方程式
②NH3转化为HNO3的整个过程中,为提高氮原子的利用率,可采取的措施是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】叠氮化钠(NaN3)是一种重要的化工产品,可用于合成抗生素头孢菌素药物和用作汽车安全气囊的气源。实验室可通过以下流程制备叠氮化钠并测定其纯度。请回答以下问题:
I.制备氨基钠(反应原理为: 2Na+2NH3 2NaNH2+H2)实验装置如图甲。
2NaNH2+H2)实验装置如图甲。

已知:氨基钠极易与水剧烈反应生成氨气,且其易被空气氧化
(1)仪器a的名称为_______ 实验开始时,应先打开分液漏斗使浓氨水流下,目的是_______ 。
(2)①B装置中的药品可选用_______ 。
A. P2O5 B.碱石灰 C.无水硫酸铜 D.无水氯化钙
②若无B装置,C中生成的氨基钠会发生的反应为_______ (用化学方程式表示)。
(3)某同学认为上述实验设计有缺陷,请对装置提出改正措施_______ 。
II. 制备NaN3
(4)将I中制备的NaNH2与N2O在210-220°C的条件下反应生成NaN3、NaOH和氨气,反应容器不选用玻璃材质,请用化学方程式说明不选用玻璃材质的原因_______ 。
III.测定NaN3的纯度水
精确称量0.1500g NaN3样品,设计如图乙所示装置,连接好装置后使锥形瓶倾斜,使小试管中的NaN3样品与M溶液接触,测量产生的气体体积从而测定其纯度(不考虑溶剂的挥发)。已知: 2NaN3~3N2(其他产物略),反应中放出大量的热。

(5)反应后对水量气管读数时,应注意
①_______
②调节水量气管和水准瓶中的液面相平
③视线平视凹液面
(6)常温下测得产生气体的体积为54.00mL(N2的密度为1.400g/L),计算NaN3样品的纯度为(质量分数)_______ 。
I.制备氨基钠(反应原理为: 2Na+2NH3
 2NaNH2+H2)实验装置如图甲。
2NaNH2+H2)实验装置如图甲。
已知:氨基钠极易与水剧烈反应生成氨气,且其易被空气氧化
(1)仪器a的名称为
(2)①B装置中的药品可选用
A. P2O5 B.碱石灰 C.无水硫酸铜 D.无水氯化钙
②若无B装置,C中生成的氨基钠会发生的反应为
(3)某同学认为上述实验设计有缺陷,请对装置提出改正措施
II. 制备NaN3
(4)将I中制备的NaNH2与N2O在210-220°C的条件下反应生成NaN3、NaOH和氨气,反应容器不选用玻璃材质,请用化学方程式说明不选用玻璃材质的原因
III.测定NaN3的纯度水
精确称量0.1500g NaN3样品,设计如图乙所示装置,连接好装置后使锥形瓶倾斜,使小试管中的NaN3样品与M溶液接触,测量产生的气体体积从而测定其纯度(不考虑溶剂的挥发)。已知: 2NaN3~3N2(其他产物略),反应中放出大量的热。

(5)反应后对水量气管读数时,应注意
①
②调节水量气管和水准瓶中的液面相平
③视线平视凹液面
(6)常温下测得产生气体的体积为54.00mL(N2的密度为1.400g/L),计算NaN3样品的纯度为(质量分数)
您最近一年使用:0次



