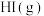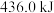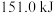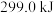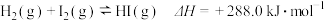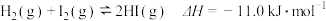含11.2 g KOH的稀溶液与1 L 0.1 mol·L-1的H2SO4溶液反应放出11.46 kJ的热量,下列能正确表示中和热的热化学方程式是( )
| A.KOH(aq)+0.5H2SO4(aq)===0.5 K2SO4(aq)+H2O(l) ΔH=-11.46 kJ·mol-1 |
| B.2KOH(s)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1 |
| C.2KOH(aq)+H2SO4===K2SO4(aq)+H2O(l) ΔH=114.6 kJ·mol-1 |
| D.KOH(aq)+0.5H2SO4(aq)===0.5 K2SO4(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 |
更新时间:2019-07-22 13:25:17
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】研究表明,在一定条件下,气态HCN(a)与HNC(b)两种分子的互变反应过程能量变化如图所示。下列说法正确的是
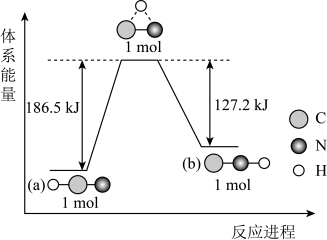

| A.HNC比HCN更稳定 |
B. 为吸热反应且反应一定要加热 为吸热反应且反应一定要加热 |
| C.1molHCN(g)中的所有化学键全部断开需要吸收186.5kJ的热量 |
D.由图可知,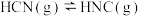 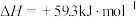 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】 2
2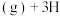 2
2 3
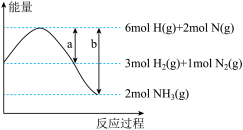
3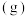 的能量变化如图所示,a、b均为正值,单位是kJ。下列说法正确的是
的能量变化如图所示,a、b均为正值,单位是kJ。下列说法正确的是
 2
2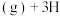 2
2 3
3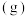 的能量变化如图所示,a、b均为正值,单位是kJ。下列说法正确的是
的能量变化如图所示,a、b均为正值,单位是kJ。下列说法正确的是
A. 2 2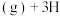 2 2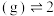 NH3 NH3 -1 -1 |
B. l-1 l-1 |
C.NH3中N-H键键能为 -1 -1 |
| D.压强越大,该反应的△H越小 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐1】已知25°C、101 kPa时,强酸与强碱的稀溶液发生中和反应生成1 mol水放出的热量为57.3kJ,则下列描述正确的是
| A.酸碱中和反应的中和热为57.3kJ |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=+57.3 kJ·mol-1 |
| C.1 mol强酸和1 mol强碱完全反应,放出的热量一定为57.3 kJ·mol-1 |
| D.稀盐酸与稀氨水反应生成1 mol水,放出的热量小于57.3 kJ·mol-1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
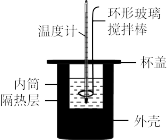
【推荐2】已知CH3COOH(aq) H+(aq)+ CH3COO-(aq) △H1>0,H+(aq)+OH- (aq)=H2O(l) △H2=573kJ·mol-1,某实验小组用0.50mol/LCH3COOH溶液和0.55mol/LNaOH溶液测定中和反应的反应热,简易量热装置如图所示。下列说法正确的是
H+(aq)+ CH3COO-(aq) △H1>0,H+(aq)+OH- (aq)=H2O(l) △H2=573kJ·mol-1,某实验小组用0.50mol/LCH3COOH溶液和0.55mol/LNaOH溶液测定中和反应的反应热,简易量热装置如图所示。下列说法正确的是
 H+(aq)+ CH3COO-(aq) △H1>0,H+(aq)+OH- (aq)=H2O(l) △H2=573kJ·mol-1,某实验小组用0.50mol/LCH3COOH溶液和0.55mol/LNaOH溶液测定中和反应的反应热,简易量热装置如图所示。下列说法正确的是
H+(aq)+ CH3COO-(aq) △H1>0,H+(aq)+OH- (aq)=H2O(l) △H2=573kJ·mol-1,某实验小组用0.50mol/LCH3COOH溶液和0.55mol/LNaOH溶液测定中和反应的反应热,简易量热装置如图所示。下列说法正确的是 
A.用环形铜质搅拌棒替代玻璃搅拌器,测得中和反应的 偏低 偏低 |
| B.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)的反应热△H <-57.3kJ·mol-1 |
| C.向内筒加料时,应一次性快速加入且立即盖紧杯盖 |
| D.增大反应物溶液的体积,测得的中和热同倍数增大 |
您最近半年使用:0次

 有关物质中的化学键断裂时吸收的能量:
有关物质中的化学键断裂时吸收的能量: