50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是________ 。
(2)烧杯间填满碎纸条的作用是________ 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________ (填“偏大”、“偏小”或“无影响”)。
(4)该实验常用0.50 mol·L-1 HCl和0.55 mol·L-1 NaOH溶液各50 mL进行实验,其中NaOH溶液浓度大于盐酸浓度的作用是______ ,当室温低于10 ℃时进行实验,对实验结果会造成较大的误差,其原因是_____________ 。
(5)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求得的中和热________ (填“相等”或“不相等”),简述理由: ______________ 。
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热ΔH将________ (填“偏大”、“偏小”或“无影响”)。

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)烧杯间填满碎纸条的作用是
(3)大烧杯上如不盖硬纸板,求得的中和热数值
(4)该实验常用0.50 mol·L-1 HCl和0.55 mol·L-1 NaOH溶液各50 mL进行实验,其中NaOH溶液浓度大于盐酸浓度的作用是
(5)实验中改用60 mL 0.50 mol·L-1盐酸与50 mL 0.50 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求得的中和热
(6)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热ΔH将
17-18高二上·内蒙古巴彦淖尔·阶段练习 查看更多[13]
广东省 广州市西关培英中学2023-2024学年高二上学期11月期中化学试题贵州省毕节市金沙县第一中学2021-2022学年高二上学期期中考试化学试题云南省绿春县第一中学2019届高三上学期开学考试化学试题云南省永胜县第一中学2020-2021学年高二下学期6月份考试化学试题贵州省贵阳市清镇养正学校2019-2020学年高二上学期期中考试化学试题(已下线)第01章 化学反应与能量(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)山西省忻州市第一中学2019-2020学年高一下学期开学考试化学试题黑龙江省安达市第七中学2019-2020学年高一3月月考化学试题河北省张家口市尚义县第一中学2019-2020学年高二10月月考化学试题云南省武定民族中学2019-2020学年高二上学期期末考试化学试题云南省鹤庆三中2018-2019学年高二下学期期末考试化学试题内蒙古集宁一中(西校区)2018-2019学年高一下学期期末考试化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题B
更新时间:2019-07-25 07:42:53
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式___________________________ ;
(2)如右图所示,仪器A的名称是_______________ ;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H_______ (填“偏大”、“偏小”或“无影响”);
(3)假设盐酸和NaOH溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18×10-3kJ/(g·℃)。为了计算中和热,某学生实验记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热△H=___________ ;(结果保留一位小数)
(4)若用0.50mol/L醋酸代替盐酸和氢氧化钠溶液反应则测得中和热会_______ (填“偏大”、“偏小”或“无影响”)。
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式
(2)如右图所示,仪器A的名称是
(3)假设盐酸和NaOH溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18×10-3kJ/(g·℃)。为了计算中和热,某学生实验记录数据如下:
| 实验序号 | 起始温度t1℃ | 终止温度t2℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |

依据该学生的实验数据计算,该实验测得的中和热△H=
(4)若用0.50mol/L醋酸代替盐酸和氢氧化钠溶液反应则测得中和热会
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。请回答下列问题:
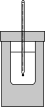
(1)从实验装置上看,图中缺少的一种玻璃仪器是_______ 。
(2)实验中改用6.94mL 15mol/L硫酸溶液与60mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所求得的生成1mol H2O(l)时放出的热量_______ (填“相等”或“不相等”),简述理由:_______ 。
(3)若三次平行操作测得数据中,起始时盐酸与NaOH溶液平均温度相同,而终止温度与起始温度差(t2-t1)分别为①3.3℃、②3.5℃、③4.5℃,则最终代入计算式的温度差的平均值为_______ ℃。

(1)从实验装置上看,图中缺少的一种玻璃仪器是
(2)实验中改用6.94mL 15mol/L硫酸溶液与60mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所求得的生成1mol H2O(l)时放出的热量
(3)若三次平行操作测得数据中,起始时盐酸与NaOH溶液平均温度相同,而终止温度与起始温度差(t2-t1)分别为①3.3℃、②3.5℃、③4.5℃,则最终代入计算式的温度差的平均值为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】利用如图所示装置测定中和热的实验步骤如下:
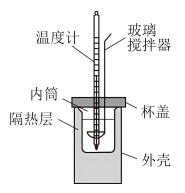
①用量筒量取50 0.50
0.50 盐酸倒入量热计的内筒,测出盐酸温度,用水将温度计上的酸冲洗干净,擦干备用;
盐酸倒入量热计的内筒,测出盐酸温度,用水将温度计上的酸冲洗干净,擦干备用;
②用另一量筒量取50 0.55
0.55
 溶液,用温度计测出其温度;
溶液,用温度计测出其温度;
③将 溶液分次缓慢倒入量热计的内筒中,搅拌使之混合均匀,测得混合液的平均温度;
溶液分次缓慢倒入量热计的内筒中,搅拌使之混合均匀,测得混合液的平均温度;
④重复测量2~3次,准确记录数据。
回答下列问题:
(1)上述步骤中有两点错误,分别是_______ 、_______ 。
(2)现将一定量的稀氢氧化钾溶液、稀氢氧化钙溶液、稀氨水分别和1L1 稀盐酸恰好完全反应,其反应热分别为
稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为_______ 。
(3)上述实验结果测得中和热数值偏低,产生的原因不可能为_______ (填序号)。
①实验装置保温、隔热效果差
②用量筒量取盐酸溶液体积时仰视读数
③分多次把 溶液倒入内筒中
溶液倒入内筒中
(4)温度、浓度对化学反应速率产生重要影响,请回答下列问题:向A、B两支试管中各加入5 0.1
0.1
 溶液,向C、D两支试管中各加入5
溶液,向C、D两支试管中各加入5 0.1
0.1 的
的 溶液,将A、C试管置于60℃热水中一段时间,然后分别将A与C、B与D混合。发生反应的化学方程式为
溶液,将A、C试管置于60℃热水中一段时间,然后分别将A与C、B与D混合。发生反应的化学方程式为_______ ,实验中产生明显现象需要时间较短的一组反应是_______ (填“A与C”或“B与D”)。
(5)反应
 ,在一容积可变的密闭容器中进行,试回答:
,在一容积可变的密闭容器中进行,试回答:
①增加 的量,其正反应速率
的量,其正反应速率_______ (填“增大”“不变”或“减小”,下同),平衡_______ 移动(填“不”“向正反应方向”或“向逆反应方向”,下同)。
②将容器的体积缩小一半,其正反应速率_______ ,平衡_______ 移动。
③保持体积不变,充入水蒸气,其正反应速率_______ ,平衡_______ 移动。

①用量筒量取50
 0.50
0.50 盐酸倒入量热计的内筒,测出盐酸温度,用水将温度计上的酸冲洗干净,擦干备用;
盐酸倒入量热计的内筒,测出盐酸温度,用水将温度计上的酸冲洗干净,擦干备用;②用另一量筒量取50
 0.55
0.55
 溶液,用温度计测出其温度;
溶液,用温度计测出其温度;③将
 溶液分次缓慢倒入量热计的内筒中,搅拌使之混合均匀,测得混合液的平均温度;
溶液分次缓慢倒入量热计的内筒中,搅拌使之混合均匀,测得混合液的平均温度;④重复测量2~3次,准确记录数据。
回答下列问题:
(1)上述步骤中有两点错误,分别是
(2)现将一定量的稀氢氧化钾溶液、稀氢氧化钙溶液、稀氨水分别和1L1
 稀盐酸恰好完全反应,其反应热分别为
稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为(3)上述实验结果测得中和热数值偏低,产生的原因不可能为
①实验装置保温、隔热效果差
②用量筒量取盐酸溶液体积时仰视读数
③分多次把
 溶液倒入内筒中
溶液倒入内筒中(4)温度、浓度对化学反应速率产生重要影响,请回答下列问题:向A、B两支试管中各加入5
 0.1
0.1
 溶液,向C、D两支试管中各加入5
溶液,向C、D两支试管中各加入5 0.1
0.1 的
的 溶液,将A、C试管置于60℃热水中一段时间,然后分别将A与C、B与D混合。发生反应的化学方程式为
溶液,将A、C试管置于60℃热水中一段时间,然后分别将A与C、B与D混合。发生反应的化学方程式为(5)反应

 ,在一容积可变的密闭容器中进行,试回答:
,在一容积可变的密闭容器中进行,试回答:①增加
 的量,其正反应速率
的量,其正反应速率②将容器的体积缩小一半,其正反应速率
③保持体积不变,充入水蒸气,其正反应速率
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】I.使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL)。
实验步骤:
(1)配制100mL待测白醋溶液。量取10.00mL食用白醋,注入烧杯中用水稀释后转移到___________ (填仪器名称)中定容,摇匀即得。
(2)取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴___________ 作指示剂。
(3)读取盛装0.1000mol/L KOH溶液的___________ (填仪器名称)的初始读数。如果液面位置如图所示,则此时的读数为___________ mL。

(4)滴定:当___________ 时,停止滴定,并记录KOH溶液的终点读数。重复滴定3次。
II.用如图所示的装置测定中和热。

实验药品:100mL0.50mol‧L-1盐酸、50mL0.50mol‧L-1NaOH溶液、50mL0.50mol‧L-1氨水。
实验步骤:略。
已知:NH3·H2O⇌ +OH-, ΔH>0
+OH-, ΔH>0
回答下列问题:
(1)从实验装置上看,还缺少___________ ;是否可以用铜质材料替代___________ (填“是”或“否”),理由是___________ 。
(2)烧杯间填满碎泡沫塑料的作用是___________ 。
(3)将浓度为0.5mol·L-1的酸溶液和0.50mol·L-1的碱溶液各50mL混合(溶液密度均为1g·mL-1),生成溶液的比热容c=4.18J·g-1·℃-1 , 搅动后,测得酸碱混合液的温度变化数据如下:
①某同学利用上述装置做甲组实验,测得中和热的数值偏低,试分析可能的原因___________ 。
A.测量完盐酸的温度再次测最NaOH溶液温度时,温度计上残留的酸液未用水冲洗干净。
B.做本实验的当天室温较高
C.大小烧杯口不平齐,小烧杯口未接触泡沫塑料板。
D.NaOH溶液一次性迅速倒入
②写出HCl+NH3·H2O的热化学方程式:___________ 。
③两组实验结果差异的原因是___________ 。
实验步骤:
(1)配制100mL待测白醋溶液。量取10.00mL食用白醋,注入烧杯中用水稀释后转移到
(2)取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴
(3)读取盛装0.1000mol/L KOH溶液的

(4)滴定:当
II.用如图所示的装置测定中和热。

实验药品:100mL0.50mol‧L-1盐酸、50mL0.50mol‧L-1NaOH溶液、50mL0.50mol‧L-1氨水。
实验步骤:略。
已知:NH3·H2O⇌
 +OH-, ΔH>0
+OH-, ΔH>0回答下列问题:
(1)从实验装置上看,还缺少
(2)烧杯间填满碎泡沫塑料的作用是
(3)将浓度为0.5mol·L-1的酸溶液和0.50mol·L-1的碱溶液各50mL混合(溶液密度均为1g·mL-1),生成溶液的比热容c=4.18J·g-1·℃-1 , 搅动后,测得酸碱混合液的温度变化数据如下:
| 反应物 | 起始温度t1/℃ | 终止温度t2/℃ | 中和热 | |
| 甲组 | HCl+NaOH | 15.0 | 18.3 | ΔH1 |
| 乙组 | HCl+NH3·H2O | 15.0 | 18. 1 | ΔH2 |
A.测量完盐酸的温度再次测最NaOH溶液温度时,温度计上残留的酸液未用水冲洗干净。
B.做本实验的当天室温较高
C.大小烧杯口不平齐,小烧杯口未接触泡沫塑料板。
D.NaOH溶液一次性迅速倒入
②写出HCl+NH3·H2O的热化学方程式:
③两组实验结果差异的原因是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】I.磷能形成多种含氧酸。
(1)次磷酸(H3PO2)是一种精细化工产品,向10mLH3PO2溶液中加入 等物质的量浓度的NaOH溶液后,所得的溶液中只有
等物质的量浓度的NaOH溶液后,所得的溶液中只有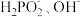 两种阴离子。
两种阴离子。
①写出H3PO2溶液与足量NaOH溶液反应后形成的正盐的化学式:_______ 。
②常温下,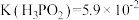 ,0.1mol/L的H3PO2溶液在加水稀释过程中,下列表达式的数据一定变小的是
,0.1mol/L的H3PO2溶液在加水稀释过程中,下列表达式的数据一定变小的是_______ (填标号)。
A.c(H+) B. C.
C.
(2)亚磷酸(H3PO3)是二元中强酸,25℃时亚磷酸的电离常数为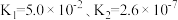 。试从电离平衡移动的角度解释
。试从电离平衡移动的角度解释 数据的差异:
数据的差异:_______ 。
(3)25℃时,HF的电离常数为 ;H3PO4的电离常数为
;H3PO4的电离常数为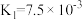 ,
,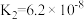 ,
,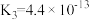 。足量
。足量 溶液和H3PO4溶液反应的离子方程式为
溶液和H3PO4溶液反应的离子方程式为_______ 。
(4)①相同温度下,等物质的量浓度的上述三种磷的含氧酸中,c(H+)由大到小的顺序为_______ (用酸的分子式表示)。
②已知: ,则
,则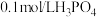 溶液与足量0.1mol/LNaOH溶液反应生成1molH2O(l)放出的热量为
溶液与足量0.1mol/LNaOH溶液反应生成1molH2O(l)放出的热量为_______ (填标号)。
A.=57.3kJ B.<57.3kJ C.>57.3kJ D.无法确定
II.已知25℃时水溶液呈弱碱性: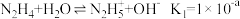 ;
; 。
。
(5)25℃时,向N2H4水溶液中加入H2SO4,欲使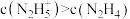 ,同时
,同时 ,应控制溶液中c(OH-)的范围为
,应控制溶液中c(OH-)的范围为_______ (用含a、b式子表示)。
(1)次磷酸(H3PO2)是一种精细化工产品,向10mLH3PO2溶液中加入
 等物质的量浓度的NaOH溶液后,所得的溶液中只有
等物质的量浓度的NaOH溶液后,所得的溶液中只有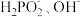 两种阴离子。
两种阴离子。①写出H3PO2溶液与足量NaOH溶液反应后形成的正盐的化学式:
②常温下,
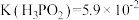 ,0.1mol/L的H3PO2溶液在加水稀释过程中,下列表达式的数据一定变小的是
,0.1mol/L的H3PO2溶液在加水稀释过程中,下列表达式的数据一定变小的是A.c(H+) B.
 C.
C.
(2)亚磷酸(H3PO3)是二元中强酸,25℃时亚磷酸的电离常数为
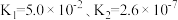 。试从电离平衡移动的角度解释
。试从电离平衡移动的角度解释 数据的差异:
数据的差异:(3)25℃时,HF的电离常数为
 ;H3PO4的电离常数为
;H3PO4的电离常数为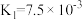 ,
,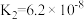 ,
,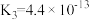 。足量
。足量 溶液和H3PO4溶液反应的离子方程式为
溶液和H3PO4溶液反应的离子方程式为(4)①相同温度下,等物质的量浓度的上述三种磷的含氧酸中,c(H+)由大到小的顺序为
②已知:
 ,则
,则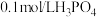 溶液与足量0.1mol/LNaOH溶液反应生成1molH2O(l)放出的热量为
溶液与足量0.1mol/LNaOH溶液反应生成1molH2O(l)放出的热量为A.=57.3kJ B.<57.3kJ C.>57.3kJ D.无法确定
II.已知25℃时水溶液呈弱碱性:
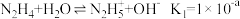 ;
; 。
。(5)25℃时,向N2H4水溶液中加入H2SO4,欲使
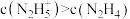 ,同时
,同时 ,应控制溶液中c(OH-)的范围为
,应控制溶液中c(OH-)的范围为
您最近半年使用:0次
【推荐3】测定
 盐酸和
盐酸和

 溶液反应的反应热的实验装置如图所示。
溶液反应的反应热的实验装置如图所示。
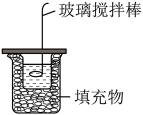
回答下列问题:
(1)图中缺少的一种仪器是_______ 。
(2)实验时玻璃搅拌器的运动方向是_______(填标号)。
(3)假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成的溶液的比热容
,又知中和反应后生成的溶液的比热容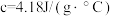 。实验记录数据如表:
。实验记录数据如表:
则中和反应生成
 的
的
_______  (保留1位小数)
(保留1位小数)
若计算结果与理论数据( )相比较,有误差,则可能导致该误差的原因是
)相比较,有误差,则可能导致该误差的原因是_______ 。
a.实验装置保温、隔热效果差
b.用量筒量取盐酸的体积时仰视读数
c.分多次把 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中
d.用温度计测定盐酸的起始温度后直接去测定 溶液的温度
溶液的温度
若改用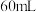
 盐酸和
盐酸和

 溶液进行反应,与上述实验相比,所求中和热
溶液进行反应,与上述实验相比,所求中和热_______ (填“相等”或“不相等”)。
(4)现将一定量的稀氢氧化钾溶液、稀氢氧化钠溶液、稀氨水分别和
 稀盐酸恰好完全反应,其反应热分别为
稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为_______ 。
(5)下列说法正确的是_______(填标号)。

 盐酸和
盐酸和

 溶液反应的反应热的实验装置如图所示。
溶液反应的反应热的实验装置如图所示。
回答下列问题:
(1)图中缺少的一种仪器是
(2)实验时玻璃搅拌器的运动方向是_______(填标号)。
| A.上下 | B.左右 | C.顺时针 | D.逆时针填充物 |
 ,又知中和反应后生成的溶液的比热容
,又知中和反应后生成的溶液的比热容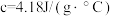 。实验记录数据如表:
。实验记录数据如表:| 实验序号 | 起始温度 | 终止温度 | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |

 的
的
 (保留1位小数)
(保留1位小数)若计算结果与理论数据(
 )相比较,有误差,则可能导致该误差的原因是
)相比较,有误差,则可能导致该误差的原因是a.实验装置保温、隔热效果差
b.用量筒量取盐酸的体积时仰视读数
c.分多次把
 溶液倒入盛有盐酸的小烧杯中
溶液倒入盛有盐酸的小烧杯中d.用温度计测定盐酸的起始温度后直接去测定
 溶液的温度
溶液的温度若改用
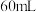
 盐酸和
盐酸和

 溶液进行反应,与上述实验相比,所求中和热
溶液进行反应,与上述实验相比,所求中和热(4)现将一定量的稀氢氧化钾溶液、稀氢氧化钠溶液、稀氨水分别和

 稀盐酸恰好完全反应,其反应热分别为
稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为(5)下列说法正确的是_______(填标号)。
| A.向内筒中加入稀碱时,应当缓慢而匀速地加入 |
| B.将用量筒量取好的稀盐酸加入内筒后,应当快速用水冲洗量筒内壁剩余的稀盐酸至内筒中,以免造成测量误差 |
| C.用量筒量取稀酸或碱时,眼睛必须与液体凹面最低处相平 |
D.内筒洗净后,未及时烘干,直接用该内筒进行实验,对生成  时所测得的中和反应的反应热 时所测得的中和反应的反应热 无影响 无影响 |
您最近半年使用:0次



