一包白色粉末可能含有Ba(NO3)2、CuSO4、K2CO3、NaCl、Na2SO4、KNO3中的一种或几种,为判断其组成,进行如下实验:①取少量该白色粉末溶于水,产生白色沉淀,上层清液为无色;②取上层清液滴在pH试纸上,pH>7;③过滤,往得到的白色沉淀中滴入稀盐酸,白色沉淀部分溶解。则该白色粉末中一定含有______ ,一定没有______ ,可能含有______ 。
10-11高三·甘肃天水·阶段练习 查看更多[1]
(已下线)2012届甘肃省天水一中高三第三阶段考试化学试卷
更新时间:2016-12-09 02:30:45
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】有一固体粉末,可能含有Na2CO3、Na2SO4、CuSO4、CaCl2、KCl的一种或几种,为检验它们,做了如下实验:
①将该粉末溶于水,搅拌后得无色透明溶液;
②往此溶液中滴加BaCl2溶液,有白色沉淀生成;
③过滤,将沉淀物置于足量稀硝酸中,发现沉淀全部溶解。
由上述现象判断:
(1)固体粉末中一定含有________________ ,一定不含有_________________ ,可能含有_______________________ 。
(2)写出实验②中反应的化学方程式:_________________________________ 。
①将该粉末溶于水,搅拌后得无色透明溶液;
②往此溶液中滴加BaCl2溶液,有白色沉淀生成;
③过滤,将沉淀物置于足量稀硝酸中,发现沉淀全部溶解。
由上述现象判断:
(1)固体粉末中一定含有
(2)写出实验②中反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】为探究盐酸的化学性质,某化学小组做了如下实验:

(1)下列编号为A~F的反应中,无论稀盐酸过量还是少量均无明显现象的是___________ (填字母编号),C中所发生反应的离子方程式为___________ 。
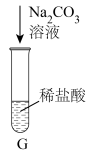
(2)G是向稀盐酸中逐滴加入一定量 溶液(见图),充分反应。将G中所得溶液、上题D中所得溶液倒入一个洁净的烧杯H中,观察到烧杯中先有气泡产生,且有白色沉淀出现。
溶液(见图),充分反应。将G中所得溶液、上题D中所得溶液倒入一个洁净的烧杯H中,观察到烧杯中先有气泡产生,且有白色沉淀出现。
①倒入烧杯前D试管中的溶质是___________ 。
②D、G试管中反应后的溶液的混合于烧杯H时,“白色沉淀出现”的离子方程式___________ 。
(3)将烧杯H中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
【提出问题】滤液中溶质的主要成分是什么?
【假设与猜想】猜想I:NaCl;
猜想II:NaCl和 ;
;
猜想III:___________ 。
【实验与结论】

(1)下列编号为A~F的反应中,无论稀盐酸过量还是少量均无明显现象的是
(2)G是向稀盐酸中逐滴加入一定量
 溶液(见图),充分反应。将G中所得溶液、上题D中所得溶液倒入一个洁净的烧杯H中,观察到烧杯中先有气泡产生,且有白色沉淀出现。
溶液(见图),充分反应。将G中所得溶液、上题D中所得溶液倒入一个洁净的烧杯H中,观察到烧杯中先有气泡产生,且有白色沉淀出现。
①倒入烧杯前D试管中的溶质是
②D、G试管中反应后的溶液的混合于烧杯H时,“白色沉淀出现”的离子方程式
(3)将烧杯H中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
【提出问题】滤液中溶质的主要成分是什么?
【假设与猜想】猜想I:NaCl;
猜想II:NaCl和
 ;
;猜想III:
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴加适量碳酸钠溶液 | 无现象 | 猜想 (填“I”“II”或“III”) |
| 取少量滤液于试管中,滴加足量 | 有气泡冒出 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】A、B、C、D 四种可溶性盐,其阳离子分别是 Na+、Ba2+、Cu2+、Ag+中的某一种,阴离子分别是 Cl-、SO 、CO
、CO 、NO
、NO 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。
(1)根据上述实验事实,推断这四种盐的化学式分别为:A___________ B___________ ; C___________ ;D___________ 。
(2)写出下列反应的离子方程式:
①B+D→:_____
②C+HCl→气体:_____
 、CO
、CO 、NO
、NO 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5 mL 蒸馏水的 4 支试管中,只有 B 盐溶液呈蓝色。②分别向 4 支试管中加入 2 mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。(1)根据上述实验事实,推断这四种盐的化学式分别为:A
(2)写出下列反应的离子方程式:
①B+D→:
②C+HCl→气体:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】有四瓶无色溶液,分别是 、
、 、
、 、
、 溶液,请根据有关物质的性质,设计实验将其区分开来。
溶液,请根据有关物质的性质,设计实验将其区分开来。
 、
、 、
、 、
、 溶液,请根据有关物质的性质,设计实验将其区分开来。
溶液,请根据有关物质的性质,设计实验将其区分开来。| 实验步骤 | 实验现象 | 结论 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】已知二氧化硫可使高锰酸钾溶液褪色反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4(已知MnSO4溶液为无色溶液)下图为验证浓硫酸与木炭在加热条件下,反应产物中是否含有SO2和CO2的部分装置。

(1)实验时,从_______ 端连接盛有澄清石灰水的实验装置(用a或b填空)。
(2)可观察到A瓶的溶液_______ 。
(3)C瓶溶液的作用是_______ 。
(4)验证有CO2的实验现象是_______ 。

(1)实验时,从
(2)可观察到A瓶的溶液
(3)C瓶溶液的作用是
(4)验证有CO2的实验现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】在编号为A、B、C、D的四支试管中分别盛有NaHSO4、NaHCO3、BaCl2、BaCO3固体,在只有蒸馏水和若干试管的条件下,将它们一一鉴别出来,在你设计的实验方案中:
(1)已知NaHSO4溶于水发生电离:NaHSO4=Na++H++SO ,根据物质的溶解性不同,最先检验出来的固体是
,根据物质的溶解性不同,最先检验出来的固体是_______ ,随后枪验出的第二种物质是_______ ;
(2)后两种固体被检验出来时发生反应的离子方程式分别是___________ 、__________ 。
(1)已知NaHSO4溶于水发生电离:NaHSO4=Na++H++SO
 ,根据物质的溶解性不同,最先检验出来的固体是
,根据物质的溶解性不同,最先检验出来的固体是(2)后两种固体被检验出来时发生反应的离子方程式分别是
您最近一年使用:0次



