已知A和B两支试管的溶液中共含有 K+、Ag+、Mg2+、Cl-、OH-、NO3—六种离子,向试管A的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
(1)试管A的溶液中所含的上述离子有_______________________
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是________ (填化学式)。
(3)若试管A和试管B中共有四种物质按等物质的量溶解于试管中,再将A和B中的溶液混合过滤,所得滤液中各种离子的物质的量之比 为_________________________ (要求标注出离子种类)。
(4)若向由试管A的溶液中阳离子组成的碳酸氢盐溶液中,滴入少量Ba(OH)2溶液,则发生反应的离子方程式为____________ 。
(1)试管A的溶液中所含的上述离子有
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(3)若试管A和试管B中共有四种物质按等物质的量溶解于试管中,再将A和B中的溶液混合过滤,所得滤液中各种离子的
(4)若向由试管A的溶液中阳离子组成的碳酸氢盐溶液中,滴入少量Ba(OH)2溶液,则发生反应的离子方程式为
更新时间:2019-09-23 23:29:35
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)物质的量相等的 CO 和 CO2 中,同温同压下所占的体积比为____ ,原子个数之比为______ ;
(2)1.8g水与_______ mol硫酸所含的分子数相等,它们所含氧原子数之比是________ ,其中氢原子数之比是___________ 。
(3)3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为________ 。
(4)可用于分离或提纯物质的方法有:
A 过滤 B 萃取 C 渗析 D 蒸馏 E 灼热氧化 F 分液.
如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
①除去淀粉溶液中的少量碘化钠________ ; ②提取溴水中的溴单质______ ;
③除去水中的Na+、 、Cl-等杂质
、Cl-等杂质________ ; ④除去CuO中的Cu ______ ;
(2)1.8g水与
(3)3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为
(4)可用于分离或提纯物质的方法有:
A 过滤 B 萃取 C 渗析 D 蒸馏 E 灼热氧化 F 分液.
如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
①除去淀粉溶液中的少量碘化钠
③除去水中的Na+、
 、Cl-等杂质
、Cl-等杂质
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有_______ (填序号)。
a.单质 b.氧化物 c.电解质 d.盐 e.化合物
Ⅱ.有一瓶无色溶液只含 五种离子中的某几种。通过实验:
五种离子中的某几种。通过实验:
①原溶液中加足量 溶液产生白色沉淀;
溶液产生白色沉淀;
②原溶液中加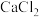 溶液不产生沉淀;
溶液不产生沉淀;
③原溶液中加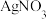 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
(2)原溶液中一定含有的离子是_______ ,一定不含有的离子是_______ ,可能含有的离子是_______ 。
(3)实验③说明原溶液中含有_______ 。有的同学认为实验③可以省略,你认为是否正确(填“是”或“否”)_______ ,理由是_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在有
a.单质 b.氧化物 c.电解质 d.盐 e.化合物
Ⅱ.有一瓶无色溶液只含
 五种离子中的某几种。通过实验:
五种离子中的某几种。通过实验:①原溶液中加足量
 溶液产生白色沉淀;
溶液产生白色沉淀;②原溶液中加
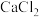 溶液不产生沉淀;
溶液不产生沉淀;③原溶液中加
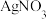 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。(2)原溶液中一定含有的离子是
(3)实验③说明原溶液中含有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白。
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________ 。
(2)取少量原溶液,加入过量稀盐酸、有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________ 。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有___________ ,该过程产生白色沉淀的离子方程式为___________ 。
(4)原溶液可能大量共存的阴离子是___________(选填字母编号)。
(5)写出NaHSO4在水溶液中的电离方程式___________ 。12gNaHSO4中含有___________ 个O原子,将其溶于水配成500mL溶液,则溶液的物质的量浓度为___________ mol/L,从中取出l00mL可以消耗1mol/L的NaOH溶液___________ mL。
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸、有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是___________(选填字母编号)。
| A.OH- | B. | C. | D.Cl- |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】亚硝酸钠(NaNO2)是肉制品加工中常用的发色剂。有毒,使用时必须严格控制用量。请按要求回答下列各小题。
(1)若要预测NaNO2的化学性质和变化,依据所学知识我们一般先从_______ 和_______ 两个角度进行预测。
(2)NaNO2中N元素的化合价为_______ 。在酸性条件下,可将KI转变为I2,自身转化为NO,该过程的离子反应方程式为______ ,该实验事实证明NaNO2具有_____ 性。
(3)已知NaNO2在空气中暴露会生成硝酸钠,反应的化学方程式为_______ ,该事实证明NaNO2具有________ 性。
(4)实验室常用NaNO2溶液与NH4Cl溶液反应来制取N2。反应原理为:NaNO2+NH4Cl NaCl+N2↑+2H2O,请选择合适的制气装置
NaCl+N2↑+2H2O,请选择合适的制气装置________ (填序号)。
A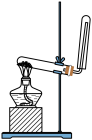 B
B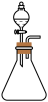 C
C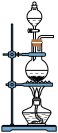 D
D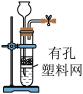
(5)误食NaNO2会导致血红蛋白中Fe2+转化为Fe3+而中毒,依据所学化学知识,写出一条合理的解毒方案______ 。
(1)若要预测NaNO2的化学性质和变化,依据所学知识我们一般先从
(2)NaNO2中N元素的化合价为
(3)已知NaNO2在空气中暴露会生成硝酸钠,反应的化学方程式为
(4)实验室常用NaNO2溶液与NH4Cl溶液反应来制取N2。反应原理为:NaNO2+NH4Cl
 NaCl+N2↑+2H2O,请选择合适的制气装置
NaCl+N2↑+2H2O,请选择合适的制气装置A
 B
B C
C D
D
(5)误食NaNO2会导致血红蛋白中Fe2+转化为Fe3+而中毒,依据所学化学知识,写出一条合理的解毒方案
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】为了达到下表中的实验要求,请选择合适的试剂及实验方法,将其标号填入对应的空格.
A.加硝酸酸化的硝酸银溶液 B.用试纸测定溶液的pH
C. 加入新制氢氧化铜悬浊液,加热 D. 加入食醋,加热
实验要求 | 试剂及方法 |
除去热水瓶的水垢 | |
鉴别蔗糖和葡萄糖 | |
区分蒸馏水和自来水 | |
证明某地雨水呈酸性 |
A.加硝酸酸化的硝酸银溶液 B.用试纸测定溶液的pH
C. 加入新制氢氧化铜悬浊液,加热 D. 加入食醋,加热
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)写出NaHSO4在水中的电离方程式 ___________ 。
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序是___________ 。
(3)实验证明铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液的。铜屑在此状态下被溶解的化学方程式为___________ 。
(4)利用铜制备CuSO4的另一种方法可用化学方程式表示为___________ 。
(5)以上两种方法___________ (填“前”或“后”)者好,原因是___________ 。
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序是
(3)实验证明铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液的。铜屑在此状态下被溶解的化学方程式为
(4)利用铜制备CuSO4的另一种方法可用化学方程式表示为
(5)以上两种方法
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有A、B、C、D四种可溶性盐溶液,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别是 、
、 、Cl-、
、Cl-、 中的某一种。
中的某一种。
(1)根据已知条件分析,将同一种盐溶液中的阳离子与阴离子用短线连接。__________
(2)四种盐溶液中,B溶液呈蓝色。则B中溶质的化学式为___________ 。
(3)向另外三种无色溶液中分别加入盐酸,A溶液变浑浊,C溶液有气泡产生。则A中溶质的化学式为___________ ,C溶液与D溶液混合的离子方程式为___________ 。
 、
、 、Cl-、
、Cl-、 中的某一种。
中的某一种。(1)根据已知条件分析,将同一种盐溶液中的阳离子与阴离子用短线连接。
| Ba2+ | Ag+ | Na+ | Cu2+ |
 |  | Cl- |  |
(3)向另外三种无色溶液中分别加入盐酸,A溶液变浑浊,C溶液有气泡产生。则A中溶质的化学式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
I.现有物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是_______ (填序号,下同),属于电解质的是_______ 。
(2)向④中逐滴滴加⑦,可观察到的现象是_______ 。
II.某白色粉末中可能含有 、
、 、
、 ,现进行以下实验:
,现进行以下实验:
i.将部分粉末加入水中,振荡,有白色沉淀生成;
ii.向i的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
iii.取少量ii的溶液滴入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
(3)根据上述实验现象,判断原白色粉末中肯定含有_______ ,可能含有_______ ,并写出有关反应的离子方程式_______ 。(写两个即可)
I.现有物质:①H2O ②Cu ③BaCO3 ④Fe(OH)3胶体 ⑤酒精 ⑥CO2 ⑦稀硫酸
(1)以上物质中属于混合物的是
(2)向④中逐滴滴加⑦,可观察到的现象是
II.某白色粉末中可能含有
 、
、 、
、 ,现进行以下实验:
,现进行以下实验:i.将部分粉末加入水中,振荡,有白色沉淀生成;
ii.向i的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
iii.取少量ii的溶液滴入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。(3)根据上述实验现象,判断原白色粉末中肯定含有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有一混合溶液,只可能含有以下离子中的若干种:K+、NH 、Cl-、Mg2+、Ba2+、CO
、Cl-、Mg2+、Ba2+、CO 、SO
、SO ,现取三份100mL该混合溶液进行如下实验。
,现取三份100mL该混合溶液进行如下实验。
实验①:向第一份混合溶液中加入AgNO3溶液,有沉淀产生;
实验②:向第二份混合溶液中加入足量NaOH溶液,加热,收集到0.08mol气体;
实验③:向第三份混合溶液中加入足量BaCl2溶液后,得到干燥的沉淀12.54g,经足量稀盐酸洗涤、干燥后,沉淀质量为4.66g。
(已知:NH +OH-
+OH- H2O+NH3↑)
H2O+NH3↑)
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液___ (填“一定”或“不一定”)含有Cl-。
(2)由实验②推断该混合溶液中应含有__ (填离子符号),其物质的量浓度为__ 。
(3)由实验③可知12.54g沉淀的成分为___ (填化学式)。
(4)综合上述实验,你认为以下结论正确的是__ (填标号)。
A.该混合溶液中一定含有K+、NH 、CO
、CO 、SO
、SO ,可能含Cl-,且n(K+)≥0.04mol
,可能含Cl-,且n(K+)≥0.04mol
B.该混合溶液中一定含有NH 、CO
、CO 、SO
、SO ,可能含K+、Cl-
,可能含K+、Cl-
C.该混合溶液中一定含有NH 、CO
、CO 、SO
、SO ,可能含Mg2+、K+、Cl-
,可能含Mg2+、K+、Cl-
D.该混合溶液中一定含有NH 、SO
、SO ,可能含Mg2+、K+、Cl-
,可能含Mg2+、K+、Cl-
 、Cl-、Mg2+、Ba2+、CO
、Cl-、Mg2+、Ba2+、CO 、SO
、SO ,现取三份100mL该混合溶液进行如下实验。
,现取三份100mL该混合溶液进行如下实验。实验①:向第一份混合溶液中加入AgNO3溶液,有沉淀产生;
实验②:向第二份混合溶液中加入足量NaOH溶液,加热,收集到0.08mol气体;
实验③:向第三份混合溶液中加入足量BaCl2溶液后,得到干燥的沉淀12.54g,经足量稀盐酸洗涤、干燥后,沉淀质量为4.66g。
(已知:NH
 +OH-
+OH- H2O+NH3↑)
H2O+NH3↑)根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液
(2)由实验②推断该混合溶液中应含有
(3)由实验③可知12.54g沉淀的成分为
(4)综合上述实验,你认为以下结论正确的是
A.该混合溶液中一定含有K+、NH
 、CO
、CO 、SO
、SO ,可能含Cl-,且n(K+)≥0.04mol
,可能含Cl-,且n(K+)≥0.04molB.该混合溶液中一定含有NH
 、CO
、CO 、SO
、SO ,可能含K+、Cl-
,可能含K+、Cl-C.该混合溶液中一定含有NH
 、CO
、CO 、SO
、SO ,可能含Mg2+、K+、Cl-
,可能含Mg2+、K+、Cl-D.该混合溶液中一定含有NH
 、SO
、SO ,可能含Mg2+、K+、Cl-
,可能含Mg2+、K+、Cl-
您最近半年使用:0次



