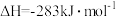下列热化学方程式中的∣△H∣能表示可燃物的燃烧热的是( )
A.H2(g)+ O2(g)=H2O(1)△H=-285.8kJ/mol-1 O2(g)=H2O(1)△H=-285.8kJ/mol-1 |
| B.H2(g)+C12(g)=2HCl(g)△H=-184.6kJ/mol-1 |
| C.2CO(g)+O2(g)=2CO2(g)△H= 一566kJ/mol-1 |
| D.CH4(g)+2O2(g)=2H2O(g)+CO2(g)△H= 一802.3kJ/mol-1 |
更新时间:2019-09-27 13:38:27
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列热化学方程式或离子方程式中,正确的是
| A.25℃、101kPa时,碳的燃烧热为-393.5kJ/mol |
B.一定条件下,将0.5mol 和1.5mol 和1.5mol 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,热化学方程式为: ,放热19.3kJ,热化学方程式为:  |
C.1mol 完全燃烧生成 完全燃烧生成 放出的热量叫 放出的热量叫 的燃烧热 的燃烧热 |
D. 的燃烧热是 的燃烧热是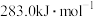 , , 分解的热化学方程式为: 分解的热化学方程式为:  |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】对于:2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJ/mol的叙述错误的是( )
| A.该反应的反应热为△H=﹣571.6kJ/mol,是放热反应 |
| B.该反应的△H与各物质的状态有关,与化学计量数也有关 |
| C.该式的含义为:25℃、101kPa下,2mol氢气完全燃烧生成液态水时放出热量571.6kJ |
| D.该反应为氢气燃烧的热化学方程式,由此可知氢气的燃烧热为571.6kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】下列有关说法正确的是
| A.已知2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2 |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH=-571.6kJ·mol-1,则H2的燃烧热为285.8kJ·mol-1 |
C.已知HI(g) 1/2H2(g)+1/2I2(s) ΔH=-26.5kJ·mol-1,由此可知,在密闭容器中充入1mol HI气体,充分分解后可以放出26.5kJ的热量 1/2H2(g)+1/2I2(s) ΔH=-26.5kJ·mol-1,由此可知,在密闭容器中充入1mol HI气体,充分分解后可以放出26.5kJ的热量 |
| D.HCl和NaOH反应中和热ΔH=-57.3kJ·mol-1,H2SO4(aq)+Ca(OH)2(aq)=CaSO4(s)+2H2O(l) ΔH=-114.6kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】查表得焓变数据(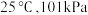 ),下列能正确表示物质燃烧热的热化学方程式是
),下列能正确表示物质燃烧热的热化学方程式是
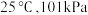 ),下列能正确表示物质燃烧热的热化学方程式是
),下列能正确表示物质燃烧热的热化学方程式是A.石墨: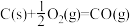  |
B. : :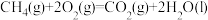 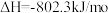 |
C. : :  |
D. : :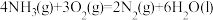 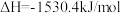 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列热化学方程式,正确 的是( )
| A.甲烷的燃烧热ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
D.500 ℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)  2NH3(g) ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 kJ·mol-1 |
您最近一年使用:0次

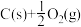 ═CO(g)
═CO(g)
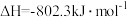
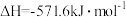
 O2(g)=CO2(g)
O2(g)=CO2(g)