I.铅蓄电池是典型的可充型电池,电池总反应为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O。
2PbSO4+2H2O。
请回答下列问题:
(1)放电时,负极材料是___ ;电解液中H2SO4的浓度将变___ (选“变大”“变小”或“不变”);
(2)充电时,阳极的电极反应式是___ 。
II.如图是一个化学过程的示意图。
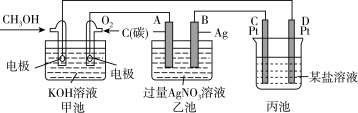
(1)图中甲池是___ 装置(填“电解池”或“原电池”),其中K+移向___ 极(选“正”或“负”)
(2)乙池中石墨电极A上发生的电极反应式:___ 。
(3)若丙内为足量NaCl溶液,当甲池内通入11.2LO2(标准状况下),则丙池中产生的气体的体积为____ L(标准状况下)。
 2PbSO4+2H2O。
2PbSO4+2H2O。请回答下列问题:
(1)放电时,负极材料是
(2)充电时,阳极的电极反应式是
II.如图是一个化学过程的示意图。

(1)图中甲池是
(2)乙池中石墨电极A上发生的电极反应式:
(3)若丙内为足量NaCl溶液,当甲池内通入11.2LO2(标准状况下),则丙池中产生的气体的体积为
更新时间:2019-11-17 19:18:23
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】要求完成下列问题。
(1)请根据图示回答:
①在Ⅰ中,Zn为_____________ 极(填“正”或“负”)。
②在Ⅱ中,负极反应式为_____________ ;电子由________ 极移向_____________ 极(填“Fe”或“Cu”),溶液中Na+移向_____________ 极(填“Fe”或“Cu”)。
③在Ⅱ中,酸是足量的。若产生了标准状况下5.6 L的气体,则转移_________ mol e-。
(2)铅蓄电池的总反应为:Pb+PbO2+2H2SO4 2PbSO4+2H2O。该电池的负极材料是
2PbSO4+2H2O。该电池的负极材料是_________ 。(填化学式)
(3)用32 g Cu与300 mL 12 mol/L的浓硝酸反应,当铜全部溶解后,共收集到标准状况下的气体11.2 L(不考虑NO2转化为N2O4),反应消耗的硝酸的物质的量是_____ mol。
(1)请根据图示回答:

①在Ⅰ中,Zn为
②在Ⅱ中,负极反应式为
③在Ⅱ中,酸是足量的。若产生了标准状况下5.6 L的气体,则转移
(2)铅蓄电池的总反应为:Pb+PbO2+2H2SO4
 2PbSO4+2H2O。该电池的负极材料是
2PbSO4+2H2O。该电池的负极材料是(3)用32 g Cu与300 mL 12 mol/L的浓硝酸反应,当铜全部溶解后,共收集到标准状况下的气体11.2 L(不考虑NO2转化为N2O4),反应消耗的硝酸的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图为原电池装置示意图:
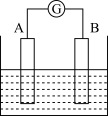
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,做负极的分别是__________ 。
a.铝片 铜片 b.铜片 铝片 c.铝片 铝片 d.铜片 铜片
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:______________________________ ;该电池工作时,A电极的质量将__________ (填“增加”、“减小”或“不变”)。若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为__________ 。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池为甲烷燃料电池,写出A电极反应式:______________________________ 。该电池工作一段时间后,溶液的碱性将__________ (填“增强”、“减弱”或“不变”)。

(1)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,做负极的分别是
a.铝片 铜片 b.铜片 铝片 c.铝片 铝片 d.铜片 铜片
(2)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入CH4和O2,该电池为甲烷燃料电池,写出A电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能设计成原电池_______
A.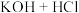 =
= B.
B.  =
=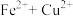
C.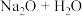 =
=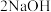 D.
D.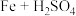 =
=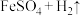
(2)为了探究化学反应中的能量变化,某同学设计了如图两个实验。有关实验现象,下列说法正确的是:_______ 。

A.图I中温度计的示数高于图II的示数
B.B.图I和图II中温度计的示数相等,且均高于室温
C.图I和图II的气泡均产生于锌棒表面
D.图II中产生气体的速度比I慢
(3)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解质溶液。放电时总反应为: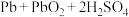 =
=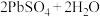
①写出放电时正极的电极反应式:_______ ;
②铅蓄电池放电时,负极质量将_______ (填“增大”、“减小”或“不变”)。当外电路上有2mol电子通过时,溶液中消耗H2SO4的物质的量为_______ 。
(1)根据构成原电池的本质判断,下列化学反应方程式正确且能设计成原电池
A.
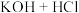 =
= B.
B.  =
=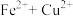
C.
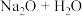 =
=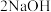 D.
D.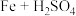 =
=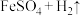
(2)为了探究化学反应中的能量变化,某同学设计了如图两个实验。有关实验现象,下列说法正确的是:

A.图I中温度计的示数高于图II的示数
B.B.图I和图II中温度计的示数相等,且均高于室温
C.图I和图II的气泡均产生于锌棒表面
D.图II中产生气体的速度比I慢
(3)电动汽车上用的铅蓄电池是以一组充满海绵状态铜的铅板和另一组结构相似的充满二氧化铅的铅板组成,用H2SO4作电解质溶液。放电时总反应为:
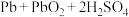 =
=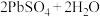
①写出放电时正极的电极反应式:
②铅蓄电池放电时,负极质量将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I、如图所示,X是一种生活中常见的金属元素,A、B、C、D为石墨电极,E、F分别为短周期相邻两种活泼金属中的一种,且E能与NaOH溶液反应。按图示接通线路,反应一段 时间(实验中所有溶液均足量)。

(1)甲池是___ (填“原电池”或“电解池”,下同]装置;乙池是___ 装置。
(2)D极为___ (填“阴极”或“阳极”)。
(3)烧杯中溶液会变蓝的是_______ (填“a”或“b”);C极上的电极反应式为____ 。
(4)F极上的电极反应式为:____ 。
(5)当电路中通过0.02mol电子时,B电极上沉积0.64g金属X,则X为___ (填元素符号),甲池中反应的化学方程式为___ 。
II、(1)从辉铜矿中浸取铜元素,可用FeCl3作浸取剂。
①反应Cu2S+4FeCl3=2CuCl2+4FeCl2+S,每生成1molCuCl2,反应中转移电子的数目为____ ;浸取时,在有氧环境下可维持Fe3+较高浓度。有关反应的离子方程式是___ 。
②浸取过程中加入洗涤剂溶解硫时,铜元素的浸取率的变化见如图1。其原因是___ 。

③353K时,向FeCl3浸取液中加入CuCl2,能加快铜元素的浸取速率,其反应原理可用化学方程式表示为:___ ,CuCl+FeCl3=CuCl2+FeCl2。
(2)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见如图2。转化时正极的电极反应式为___ 。


(1)甲池是
(2)D极为
(3)烧杯中溶液会变蓝的是
(4)F极上的电极反应式为:
(5)当电路中通过0.02mol电子时,B电极上沉积0.64g金属X,则X为
II、(1)从辉铜矿中浸取铜元素,可用FeCl3作浸取剂。
①反应Cu2S+4FeCl3=2CuCl2+4FeCl2+S,每生成1molCuCl2,反应中转移电子的数目为
②浸取过程中加入洗涤剂溶解硫时,铜元素的浸取率的变化见如图1。其原因是

③353K时,向FeCl3浸取液中加入CuCl2,能加快铜元素的浸取速率,其反应原理可用化学方程式表示为:
(2)辉铜矿可由黄铜矿(主要成分为CuFeS2)通过电化学反应转变而成,有关转化见如图2。转化时正极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知铅蓄电池的工作原理为:Pb+PbO2+2H2SO4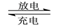 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
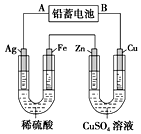
(1)A是铅蓄电池的________ 极,Cu电极是________ 极,放电过程中电解液的密度________ (填“减小”“增大”或“不变”)。
(2)Ag电极的电极反应式是______________________________ ,该电极的电极产物共________ g。
(3)Cu电极的电极反应式是______________________________ ,CuSO4溶液的浓度________ (填“减小”“增大”或“不变”)
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示________ 。
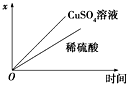
a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
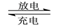 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol电子时铁电极的质量减少11.2 g。请回答下列问题。
(1)A是铅蓄电池的
(2)Ag电极的电极反应式是
(3)Cu电极的电极反应式是
(4)如图表示电解进行过程中某个量(纵坐标x)随时间的变化曲线,则x表示

a.各U形管中产生的气体的体积
b.各U形管中阳极质量的减少量
c.各U形管中阴极质量的增加量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_________ (填字母)。

a.金块 b.锌板 c.铜板 d.钠块
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是_______ 。
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的总反应式相同
(3)如下图,装置I为CO燃料电池(电解质溶液为KOH涛液),通过装置II实现铁棒上镀铜。
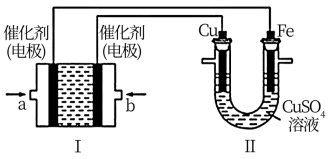
①b处应通入_______ (填“CO”或“O2”),a处电极上发生的电极反应式是_________ 。
②电镀结束后,装置I中溶液的pH______ (填写“变大”“变小”或“不变”);装置II中Cu2+的物质的量浓度________ (填写“变大”“变小”或“不变")。
③在此过程中若完全反应,装置II中阴极质量变化12.8 g,则装置I中理论上消耗CO______ L(标准状况下)。
(4)用惰性电极电解1000mL浓度均为1mol/L的CuSO4、HCl、AlCl3组成的混合溶液,一段时间后,阴、阳极收集到的气体体积相等,则阴、阳极收集到气体的总体积为______ L (假设产生的气体均在标况下测定,且所有气体均不考虑溶于水)。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择

a.金块 b.锌板 c.铜板 d.钠块
(2)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH溶液为介质的氢氧燃料电池的总反应式相同
(3)如下图,装置I为CO燃料电池(电解质溶液为KOH涛液),通过装置II实现铁棒上镀铜。

①b处应通入
②电镀结束后,装置I中溶液的pH
③在此过程中若完全反应,装置II中阴极质量变化12.8 g,则装置I中理论上消耗CO
(4)用惰性电极电解1000mL浓度均为1mol/L的CuSO4、HCl、AlCl3组成的混合溶液,一段时间后,阴、阳极收集到的气体体积相等,则阴、阳极收集到气体的总体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现用蓄电池Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾(K2FeO4)。反应装置如图所示:
Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾(K2FeO4)。反应装置如图所示:

(1)电解时,石墨电极连接的a极上放电的物质为__________ (填“Fe”或“NiO2”)。
(2)写出电解池中铁电极发生的电极反应式__________ 。
(3)当消耗掉0.1 mol NiO2时,生成高铁酸钾__________ g。
(4)Mg和Fe都是生产生活中的常用金属。加热锅炉时,水中的MgCO3可以先转化为Mg(HCO3)2,然后转化为Mg(OH)2,求MgCO3+H2O⇌Mg2++ +OH-在80℃时的平衡常数
+OH-在80℃时的平衡常数__________ 。(已知:80℃时H2O的Kw=2.5×10−13,Ksp(MgCO3)=8.4×10−6,Ka1(H2CO3)=4.2×10−7、Ka2(H2CO3)=5.6×10−11)。
 Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾(K2FeO4)。反应装置如图所示:
Fe(OH)2+Ni(OH)2为电源,制取少量高铁酸钾(K2FeO4)。反应装置如图所示:
(1)电解时,石墨电极连接的a极上放电的物质为
(2)写出电解池中铁电极发生的电极反应式
(3)当消耗掉0.1 mol NiO2时,生成高铁酸钾
(4)Mg和Fe都是生产生活中的常用金属。加热锅炉时,水中的MgCO3可以先转化为Mg(HCO3)2,然后转化为Mg(OH)2,求MgCO3+H2O⇌Mg2++
 +OH-在80℃时的平衡常数
+OH-在80℃时的平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】运用化学反应原理研究碳、氮、硫的化合物的反应对缓解环境污染、能源危机具有重要意义。
(1)汽车尾气脱硝脱碳主要原理为2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0。
N2(g)+2CO2(g) △H<0。
①该反应在一定条件下可自发反应的原因是__________ 。
②一定条件下的密闭容器中,充入CO和NO发生上述反应,该反应达到平衡后,为提高反应速率及NO的转化率,可采取的措施有_______ (填字母序号)。
a.缩小容器的体积 b.改用高效催化剂 c.升高温度 d.增加CO的浓度
(2)工业上实际处理废气时,常用活性炭作催化剂,用NH3还原NO,同时通入一定量的O2以提高处理效果。当n(NH3)=n(NO)时,写出体系中总反应的化学方程式:_______ 。
(3)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图1、图2所示。

①由图1知,当废气中的NO含量增加时,宜选用_______ 法提高脱氮的效率。
②图2中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为________ 。
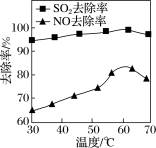
③研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。下图所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。温度高于60℃后,NO去除率下降的原因为_______ 。
(4)以连二亚硫酸盐(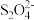 )为还原剂脱除烟气中的NO,并通过电解再生,装置如下图,阴极的电极反应式为
)为还原剂脱除烟气中的NO,并通过电解再生,装置如下图,阴极的电极反应式为_______ 。

(1)汽车尾气脱硝脱碳主要原理为2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H<0。
N2(g)+2CO2(g) △H<0。①该反应在一定条件下可自发反应的原因是
②一定条件下的密闭容器中,充入CO和NO发生上述反应,该反应达到平衡后,为提高反应速率及NO的转化率,可采取的措施有
a.缩小容器的体积 b.改用高效催化剂 c.升高温度 d.增加CO的浓度
(2)工业上实际处理废气时,常用活性炭作催化剂,用NH3还原NO,同时通入一定量的O2以提高处理效果。当n(NH3)=n(NO)时,写出体系中总反应的化学方程式:
(3)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图1、图2所示。

①由图1知,当废气中的NO含量增加时,宜选用
②图2中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为
③研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。下图所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。温度高于60℃后,NO去除率下降的原因为

(4)以连二亚硫酸盐(
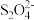 )为还原剂脱除烟气中的NO,并通过电解再生,装置如下图,阴极的电极反应式为
)为还原剂脱除烟气中的NO,并通过电解再生,装置如下图,阴极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某同学用铅蓄电池作电源,用石墨做电极电解500 mL某浓度的CuSO4溶液,观察到A电极表面有红色固体物质生成,当溶液中原有溶质完全电解后,停止通电,取出A电极,洗涤、干燥、称量,电极增重1.6 g。已知铅蓄电池的工作原理为:
Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
请按要求回答下列问题:
(1)电解CuSO4溶液的化学方程式_____________________________________ ,
(2)当反应过程中转移的电子为0.02mol时,铅蓄电池内消耗硫酸的物质的量为_____ mol。
(3)电解前CuSO4溶液的物质的量浓度为_____________ 。
(4)若电解前后溶液的体积不变,电解后溶液的pH=____
(5)写出铅蓄电池负极的电极反应式:__________________
Pb+PbO2+2H2SO4
 2PbSO4+2H2O
2PbSO4+2H2O请按要求回答下列问题:
(1)电解CuSO4溶液的化学方程式
(2)当反应过程中转移的电子为0.02mol时,铅蓄电池内消耗硫酸的物质的量为
(3)电解前CuSO4溶液的物质的量浓度为
(4)若电解前后溶液的体积不变,电解后溶液的pH=
(5)写出铅蓄电池负极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
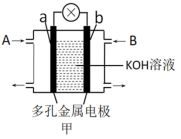
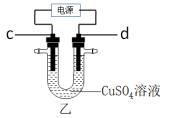
【推荐1】如图,甲是氢氧燃料电池示意图,a为正极;乙是惰性电极电解足量CuSO4溶液的示意图,电解时c电极上有红色固体物质析出。
回答下列问题:
(1)图甲中,从A口通入的气体是___ ,b电极的电极反应式为___ 。
(2)图乙中,c电极通过导线与电源的___ 极相连;理论上当c电极析出3.20g红色固体时,则d电极表面产生的气体在标准状况下的体积为___ mL。


回答下列问题:
(1)图甲中,从A口通入的气体是
(2)图乙中,c电极通过导线与电源的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】乙烷(C2H6)作为一种新能源在化学领域应用广泛,请回答下列问题:(如图所示,装置I为乙烷燃料电池(电解质溶液为KOH溶液),通过装置II实现铁棒上镀铜。

①a处应通入______ (填“C2H6”或“O2”),a处电极上发生的电极反应式是____________________________________ 。
②电镀结束后,装置I中溶液的pH______ (填写“变大”“变小”或“不变”,下同),装置II中Cu2+的物质的量浓度______ 。
③电镀结束后,装置I溶液中的阴离子除了OH-以外还含有___________ (忽略水解);在此过程中若完全反应,装置II中阴极质量变化12.8 g,则装置I中理论上消耗乙烷________ L(标准状况下)。

①a处应通入
②电镀结束后,装置I中溶液的pH
③电镀结束后,装置I溶液中的阴离子除了OH-以外还含有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】右图是一个化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O。

(1)请回答图中甲、乙两池的名称。甲池是________ 装置,乙池是________ 装置。
(2)请回答下列电极的名称:通入CH3OH的电极名称是__________________ ,B(石墨)电极的名称是______________________ 。
(3)写出电极反应式:通入O2的电极的电极反应式是__________________ 。A(Fe)电极的电极反应式为_______________________________________ 。
(4)乙池中反应的化学方程式为________________________________________ 。
(5)当乙池中A(Fe)极的质量增加4.32g时,甲池中理论上消耗O2__________ mL(标准状况下)。

(1)请回答图中甲、乙两池的名称。甲池是
(2)请回答下列电极的名称:通入CH3OH的电极名称是
(3)写出电极反应式:通入O2的电极的电极反应式是
(4)乙池中反应的化学方程式为
(5)当乙池中A(Fe)极的质量增加4.32g时,甲池中理论上消耗O2
您最近一年使用:0次



