已知A元素的一种原子没有中子;B元素的原子得1个电子后形成的离子与氩原子电子数相同;C元素的原子第三层电子数比第二层少2个;D元素的原子与A原子构成的分子A2D有10个电子。则A的元素符号为_____ ;B的离子结构示意图为_________________ ;C的原子结构示意图为_____________ ;D的元素名称为______________ 。
更新时间:2019-11-19 19:18:33
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D、E、F 六种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6 L H2,E的阳离子与A的阴离子核外电子层结构完全相同,F原子半径在短周期元素中最大,回答下列问题:
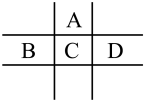
(1)元素的名称:B_____________ ;
(2)画出C离子的结构示意图:______________ ;
(3)写出D元素在周期表中的位置:__________ ;D元素的单质可用于制漂白液和漂白粉,写出制漂白液的离子方程式:____________ ,漂白粉的有效成分是______________ ;
(4)B的同族上一周期元素的氢化物为__________ (化学式) ,实验室制取该物质的方程式为_________ ,制取该气体时用______________ 做干燥剂。

(1)元素的名称:B
(2)画出C离子的结构示意图:
(3)写出D元素在周期表中的位置:
(4)B的同族上一周期元素的氢化物为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为: ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个未成对电子,E的价电子排布式为3d64s2。写出元素符号:A
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个未成对电子,E的价电子排布式为3d64s2。写出元素符号:A_______ B_______ C_______ D_______ 。
 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个未成对电子,E的价电子排布式为3d64s2。写出元素符号:A
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个未成对电子,E的价电子排布式为3d64s2。写出元素符号:A
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、4种元素,已知A— 核外有18个电子;B原子最外层电子数比D原子核外电子数多2个,B原子比D原子多2个电子层;D+ 核外没有电子,C元素原子核外电子数比B元素原子核外电子数多5个。(1)、写出四种元素的名称 ;
(1)A_________ 、B_________ 、C___________ 、D___________
(2)画出C和D原子的结构示意图
_________ 、_________
(1)A
(2)画出C和D原子的结构示意图
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】W、X、Y、Z是汽车尾气中含有的4种主要元素。W元素原子核外只有1个电子;X是金刚石的组成元素;X、Y、Z是原子序数依次递增的同一短周期元素,这三种元素原子最外层电子数之和为15。
(1)W在元素周期表中的位置为____ 。
(2)X的最高价氧化物对应的水化物的化学式为____ 。
(3)Y与Z的原子半径大小关系为:Y____ Z(填“>”或“<”)。
(4)Y的气态氢化物稳定性比Z的气态氢化物稳定性____ (填“强”或“弱”)。
(1)W在元素周期表中的位置为
(2)X的最高价氧化物对应的水化物的化学式为
(3)Y与Z的原子半径大小关系为:Y
(4)Y的气态氢化物稳定性比Z的气态氢化物稳定性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】I.回答下列问题:
(1)Cd与Zn同族且相邻,写出基态Cd原子的价层电子排布式:______ 。
(2)基态C原子中电子占据最高能级的符号是______ ,核外电子的空间运动状态有_____ 种,成对电子数与未成对电子数之比为_____ 。
(3)Mn在周期表中的位置为______ ,其基态原子价层电子轨道表示式为______ 。
II.有六种前四周期元素U、V、W、X、Y、Z,其原子序数依次增大,其部分信息如表所示。请用相应的化学用语回答下列问题:
(4)V、X分别与U形成的简单氢化物的稳定大的是_____ (填化学式);基态Z原子的电子排布式为______ 。
(5)U、V、W三种元素中第一电离能最大的是_____ (填物质名称)。
(6)U、V、W、X、Y、Z六种元素位于周期表中d区的元素是______ (填元素符号,下同);Y(VW3)2中各元素的电负性由大到小的顺序为______ 。
(1)Cd与Zn同族且相邻,写出基态Cd原子的价层电子排布式:
(2)基态C原子中电子占据最高能级的符号是
(3)Mn在周期表中的位置为
II.有六种前四周期元素U、V、W、X、Y、Z,其原子序数依次增大,其部分信息如表所示。请用相应的化学用语回答下列问题:
| U | 原子核外电子只存在一种运动状态 |
| V | 简单氢化物能与最高价氧化物对应的水合物反应生成盐 |
| W | 基态原子的价电子排布为nsnnp2n |
| X | 有同素异形体,其中白色单质需要保存在水中 |
| Y | 主族金属元素;各能层s能级上电子总数与各能层p能级上电子总数之比为2:3 |
| Z | 前四周期的基态原子中核外未成对电子数最多 |
(5)U、V、W三种元素中第一电离能最大的是
(6)U、V、W、X、Y、Z六种元素位于周期表中d区的元素是
您最近一年使用:0次
【推荐3】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表
回答下列问题:
(1)Y的氢化物空间构型是_________
(2)XY2是一种常用的溶剂,XY2的分子中存在_________ 个σ键,_________ 个π键。在H-Y,H-Z两种共价键中,键的极性较强的是_________ ,键长较长的是在_________ 。
(3)XZ4分子中X以______ 方式杂化。
(4)写出W元素简化的原子核外电子排布式_________ ,Z的价电子排布图_________
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下。Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(1)Y的氢化物空间构型是
(2)XY2是一种常用的溶剂,XY2的分子中存在
(3)XZ4分子中X以
(4)写出W元素简化的原子核外电子排布式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C、D、E五种短周期主族元素,原子序数A由到E逐渐增大。
①A元素最外层电子数是次外层电子数2的倍;
②B的阴离子和C的阳离子与氖原子的电子层结构相同;
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移;
④C的单质与B的单质在加热条件下反应,生成淡黄色固体,该淡黄色固体能与AB2反应生成B的单质;
⑤D的气态氢化物的化学式为H2D。回答下列问题:
(1)A元素在周期表中的位置是___ 。
(2)B、C、D三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)___ 。
(3)④中淡黄色固体中所含化学键类型有___ 。
(4)D的最高价氧化物对应水化物的浓溶液与铜单质在加热条件下发生反应的化学方程式为___ ,D、E的最高价氧化物对应水化物的酸性强弱关系为___ (用化学式表示)。
(5)下列叙述正确的是___ (填字母。)
a.D的简单气态氢化物比E的稳定
b.高温灼烧C、E形成的化合物,火焰呈紫色
c.物质AB2的结构式为O=C=O
①A元素最外层电子数是次外层电子数2的倍;
②B的阴离子和C的阳离子与氖原子的电子层结构相同;
③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移;
④C的单质与B的单质在加热条件下反应,生成淡黄色固体,该淡黄色固体能与AB2反应生成B的单质;
⑤D的气态氢化物的化学式为H2D。回答下列问题:
(1)A元素在周期表中的位置是
(2)B、C、D三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)④中淡黄色固体中所含化学键类型有
(4)D的最高价氧化物对应水化物的浓溶液与铜单质在加热条件下发生反应的化学方程式为
(5)下列叙述正确的是
a.D的简单气态氢化物比E的稳定
b.高温灼烧C、E形成的化合物,火焰呈紫色
c.物质AB2的结构式为O=C=O
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题。
(1)元素D在周期表中的位置________ 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)____ 。
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有________ 。用电子式表示当C、D按1:1所组成化合物的形成过程________ 。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:________________________________________________________________________ 。
(5)若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:_______________________________________________________ 。
(1)元素D在周期表中的位置
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:
(5)若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】W、X、Y、Z、M、G五种短周期元素,原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性。请回答下列问题:
(1)Y在元素周期表中的位置为___________ ;
(2) W、Y、Z、G形成的简单离子的半径大小顺序是___________ (用化学符号表示)
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有________ (任写两个)
(4)ZW的电子式为___________ ,W2Y2的电子式为______
(5)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,请用相关离子方程式解释原因________ 。
(6)已知
工业制镁时,电解MgCl2而不电解MgO的原因是是___________ ;制铝时,电解Al2O3而不电解AlCl3的原因是___________ 。
(7)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N≡N放出942kJ热量。根据以上信息和数据,下列说法正确的是___________ 。

A.N4属于一种新型化合物 B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2 D.1molN4转变为N2将吸收882kJ的能量
(1)Y在元素周期表中的位置为
(2) W、Y、Z、G形成的简单离子的半径大小顺序是
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有
(4)ZW的电子式为
(5)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,请用相关离子方程式解释原因
(6)已知
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(7)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N≡N放出942kJ热量。根据以上信息和数据,下列说法正确的是

A.N4属于一种新型化合物 B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2 D.1molN4转变为N2将吸收882kJ的能量
您最近一年使用:0次



