将V1 mL 1.00 mol·L-1HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
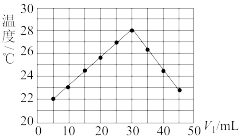

| A.做该实验时环境温度为22℃ | B.该实验表明化学能可以转化为热能 |
| C.NaOH溶液的浓度约是0.67 mol·L-1 | D.该实验表明有水生成的反应都是放热反应 |
更新时间:2019-11-18 22:30:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ/mol
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H=-1452 kJ/mol
H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ/mol
下列说法正确的是
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H=-1452 kJ/mol
H+(aq)+OH-(aq)=H2O(l) △H=-57.3 kJ/mol
下列说法正确的是
| A.H2(g)的标准燃烧热△H=-571.6 kJ/mol |
| B.醋酸溶液和氢氧化钠溶液反应生成1 mol水时,放出热量大于57.3 kJ |
C. H2SO4(aq)+ H2SO4(aq)+ Ba(OH)2(aq)= Ba(OH)2(aq)= BaSO4(s)+H2O(l) △H=-57.3 kJ/mol BaSO4(s)+H2O(l) △H=-57.3 kJ/mol |
| D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) △H=-131.4 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中正确的是
A.若 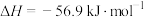 ,则1 mol ,则1 mol 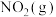 置于密闭容器中充分反应放出的热量为28.45kJ 置于密闭容器中充分反应放出的热量为28.45kJ |
B.若31 g白磷的能量比31 g红磷多b kJ,则白磷转化为红磷的热化学方程式为 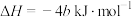 |
C.在稀溶液中,强酸与强碱反应的中和热为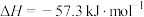 ,若将含有0.5 mol ,若将含有0.5 mol  的浓硫酸和含有1 mol NaOH的溶液混合,放出的热量等于57.3kJ 的浓硫酸和含有1 mol NaOH的溶液混合,放出的热量等于57.3kJ |
D. 的摩尔燃烧焓是 的摩尔燃烧焓是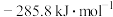 ,则 ,则 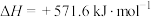 |
您最近一年使用:0次

 ,则甲烷燃烧的热化学方程式可表示为:
,则甲烷燃烧的热化学方程式可表示为:
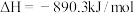
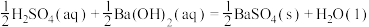

 在光照和点燃条件下的
在光照和点燃条件下的 不同
不同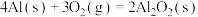
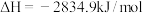 ,
,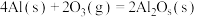
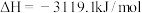 ,则
,则 比
比 稳定
稳定

