某无色溶液中可能大量含有K+、Cu2+、CO32-、Cl-、SO42-中的若干种,依据已有知识回答下列问题:
(1)不用检验就可知该溶液中一定不含有的离子是___ ;
(2)不用检验就可知该溶液中一定含有的离子是___ ;
(3)当溶液中存在大量H+时,则溶液中还可能含有的阴离子是___ ;
(4)若向该溶液中加入大量Ba2+后,则溶液中还可能含有的阴离子是___ 。
(1)不用检验就可知该溶液中一定不含有的离子是
(2)不用检验就可知该溶液中一定含有的离子是
(3)当溶液中存在大量H+时,则溶液中还可能含有的阴离子是
(4)若向该溶液中加入大量Ba2+后,则溶液中还可能含有的阴离子是
更新时间:2019-11-20 05:53:49
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】已知:NH4++OH- NH3↑+H2O,有一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl-中的几种,取该溶液进行如下实验:
NH3↑+H2O,有一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl-中的几种,取该溶液进行如下实验:
(1)填表(在表中的空白处填写离子符号)
(2)根据以上事实,在上述离子中,该溶液肯定存在的离子有________________ 。
(3)气体A溶于水可配成溶液A (该溶液的密度比水小),把50g浓度为c1的浓A溶液(溶质质量分数为ω1)与V mL水混合,得到浓度为c2的稀A溶液(溶质质量分数为ω2)。若ω1=2ω2,则:
①c1_____ c2,②V_________ 50mL(填“>”“<”或“=”)。
 NH3↑+H2O,有一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl-中的几种,取该溶液进行如下实验:
NH3↑+H2O,有一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl-中的几种,取该溶液进行如下实验:(1)填表(在表中的空白处填写离子符号)
| 步骤 | 实验步骤 | 肯定不存在的离子 |
| ① | 用pH试纸测得该溶液呈酸性 | |
| ② | 另取l0mL该溶液逐滴加入稀NaOH溶液,使溶液从酸性逐渐变为碱性,此过程中无沉淀生成 | |
| ③ | 向②所得的溶液中加入足量Na2CO3溶液,过滤、洗涤、干燥,得到1.97g白色固体 | |
| ④ | 另取l0mL该溶液,加入浓NaOH溶液并加热,收集到224mL气体A(标准状况下) | |
| ⑤ | 另取l0mL该溶液,加入足量稀硝酸和AgNO3溶液,产生2.87g白色沉淀 |
(2)根据以上事实,在上述离子中,该溶液肯定存在的离子有
(3)气体A溶于水可配成溶液A (该溶液的密度比水小),把50g浓度为c1的浓A溶液(溶质质量分数为ω1)与V mL水混合,得到浓度为c2的稀A溶液(溶质质量分数为ω2)。若ω1=2ω2,则:
①c1
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】【离子推断】某混合溶液中,只可能大量含有下表所列离子中的某几种:
将Na2O2逐渐加入到上述混合溶液中,产生沉淀的物质的量与加入Na2O2的物质的量的关系如图所示。
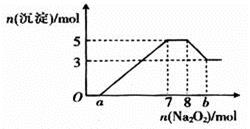
(1)将上述混合溶液中一定大量含有的阴、阳离子及其物质的量填入下表(可以不填满,也可以增加)。
(2)图中a=____________, b=____________。
| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | OH-、SO42-、CO32-、AlO2-、S2- |
将Na2O2逐渐加入到上述混合溶液中,产生沉淀的物质的量与加入Na2O2的物质的量的关系如图所示。

(1)将上述混合溶液中一定大量含有的阴、阳离子及其物质的量填入下表(可以不填满,也可以增加)。
| 离子种类 | ||||||
| 物质的量(mol) |
(2)图中a=____________, b=____________。
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】1L某混合溶液,可能含有的离子如下表:
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(v)的关系如下图所示。
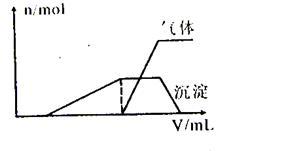
则该溶液中确定含有的离子有_________ ;肯定不含有的离子有________ ,滴加氢氧化钠过程中发生反应的先后顺序为(用离子方程式表示)_______ 。
(2)若经检测,该溶液中含有大量的Cl—、Br—、I—,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl—、Br—、I—的物质的量与通入Cl2的体积(标准状况下)的关系如下图所示,回答下列问题:
①当通入的Cl2的体积为2.8L时,溶液中发生反应的离子方程式为:_________ ,a=_________ 。
②原溶液中Cl—、Br—、I—的物质的量浓度之比为____________ 。
| 可能大量含有的阳离子 | H+  Al3+ K+ Al3+ K+ |
| 可能大量含有的阴离子 | Cl- Br- I- ClO-  |
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(v)的关系如下图所示。

则该溶液中确定含有的离子有
(2)若经检测,该溶液中含有大量的Cl—、Br—、I—,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl—、Br—、I—的物质的量与通入Cl2的体积(标准状况下)的关系如下图所示,回答下列问题:
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n (Cl-) | 1.25mol | 1.5mol | 2mol |
| n (Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(I-) | a mol | 0 | 0 |
①当通入的Cl2的体积为2.8L时,溶液中发生反应的离子方程式为:
②原溶液中Cl—、Br—、I—的物质的量浓度之比为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去):
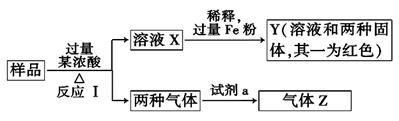
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填写化学式)___________ 。
(2)Z为一种或两种气体
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是_________ 。
②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是_____________ 。
(3)向Y中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)_____________ 。
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2 mol I- 时,共转移3 mol电子,该反应的离子方程式是_______________ 。

(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填写化学式)
(2)Z为一种或两种气体
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是
②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是
(3)向Y中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2 mol I- 时,共转移3 mol电子,该反应的离子方程式是
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】A、B、C、D、E 5瓶透明溶液。分别是HCl、BaCl2、NaHSO4、Na2CO3和AgNO3中的一种。已知:
①A与B反应有气体生成
②B与C反应有沉淀生成
③C与D反应有沉淀生成
④D与E反应有沉淀生成
⑤A与E反应有气体生成
⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在反应②和③中,生成的沉淀物质的化学式是_____ 。
(2)A是_____ ,D是_____ (填化学式)。
(3)A与E反应的离子方程式是_______________ 。
①A与B反应有气体生成
②B与C反应有沉淀生成
③C与D反应有沉淀生成
④D与E反应有沉淀生成
⑤A与E反应有气体生成
⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在反应②和③中,生成的沉淀物质的化学式是
(2)A是
(3)A与E反应的离子方程式是
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】以下是25℃时几种难溶电解质的溶解度:
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子,例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,现将混合物溶于水,再加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,再加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可;
请回答下列问题:
(1).上述三个除杂方案都能够达到很好的效果,Fe3+、Fe2+都被转化为__________ (填名称)而除去
(2).①中加入的试剂应该选择__________ 为宜。
(3).②中除去Fe3+时所发生的总反应的离子方程式为__________
(4).下列与方案③相关的叙述中,正确的是( )
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+—定不能大量存在
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子,例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,现将混合物溶于水,再加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,再加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可;
请回答下列问题:
(1).上述三个除杂方案都能够达到很好的效果,Fe3+、Fe2+都被转化为
(2).①中加入的试剂应该选择
(3).②中除去Fe3+时所发生的总反应的离子方程式为
(4).下列与方案③相关的叙述中,正确的是
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+—定不能大量存在
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】一瓶未知溶液,其中可能含有H+、NH4+、K+、Na+、Mg2+、Ba2+、Fe3+、SO42-、CO32-、Cl-和I-。取该溶液进行了以下实验:
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入数滴氯水及2 mL CCl4,经振荡后CCl4层呈紫红色;
(3)另取部分溶液,加入NaOH 溶液使其变为碱性,无沉淀生成;
(4)取部分上述碱性溶液,加Na2CO3溶液,有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
根据上述实验事实,可知原溶液中肯定含有的离子是_________ ;肯定没有的离子是_______________ 。
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入数滴氯水及2 mL CCl4,经振荡后CCl4层呈紫红色;
(3)另取部分溶液,加入NaOH 溶液使其变为碱性,无沉淀生成;
(4)取部分上述碱性溶液,加Na2CO3溶液,有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
根据上述实验事实,可知原溶液中肯定含有的离子是
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+中的两种或多种。取该溶液100mL,加入过量NaOH溶液,加热,得到448mL(标况)气体,同时产生红褐色沉淀,经过滤、洗涤、灼烧,得到1.6g固体;将上述滤液平均分成两份,一份中加足量BaCl2溶液,得到2.33g不溶于盐酸的沉淀;另一份中通入过量CO2得到1.56g白色沉淀。由此可推断原溶液一定含有的离子种类及其浓度,将结果填入下表(可不填满)。
| 一定含有的离子种类 | |||||||
| 物质的量浓度(mol/L) |
您最近半年使用:0次
【推荐3】在Cl-浓度为0.5 mol·L-1的某无色澄清溶液中,还可能含有下表中的若干种离子。
提示:SiO32-+2H+=H2SiO3↓(H2SiO3是白色沉淀)、H2SiO3 SiO2+H2O
SiO2+H2O
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
请回答下列问题。
(1)通过以上实验能确定一定不存在的阳离子是______ ,一定不存在的阴离子是________ 。
(2)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子及其浓度(不一定要填满)
(3)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:_______________ 。
| 阳离子 | K+ Ag+ Mg2+ Ba2+ Fe3+ |
| 阴离子 | NO3- CO32- SiO32- SO42- |
提示:SiO32-+2H+=H2SiO3↓(H2SiO3是白色沉淀)、H2SiO3
 SiO2+H2O
SiO2+H2O现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色沉淀并放出标准状况下0.56 L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4 g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
请回答下列问题。
(1)通过以上实验能确定一定不存在的阳离子是
(2)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子及其浓度(不一定要填满)
| 阴离子 | ① | ② | ||
| c/mol·L-1 |
(3)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:
您最近半年使用:0次



