在Cl-浓度为0.5 mol·L-1的某无色澄清溶液中,还可能含有下表中的若干种离子。
提示:SiO32-+2H+=H2SiO3↓(H2SiO3是白色沉淀)、H2SiO3 SiO2+H2O
SiO2+H2O
现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
请回答下列问题。
(1)通过以上实验能确定一定不存在的阳离子是______ ,一定不存在的阴离子是________ 。
(2)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子及其浓度(不一定要填满)
(3)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:_______________ 。
| 阳离子 | K+ Ag+ Mg2+ Ba2+ Fe3+ |
| 阴离子 | NO3- CO32- SiO32- SO42- |
提示:SiO32-+2H+=H2SiO3↓(H2SiO3是白色沉淀)、H2SiO3
 SiO2+H2O
SiO2+H2O现取该溶液100 mL进行如下实验(气体体积均在标准状况下测定)。
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 产生白色沉淀并放出标准状况下0.56 L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4 g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
请回答下列问题。
(1)通过以上实验能确定一定不存在的阳离子是
(2)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,请写出一定存在的阴离子及其浓度(不一定要填满)
| 阴离子 | ① | ② | ||
| c/mol·L-1 |
(3)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:
更新时间:2020-02-06 15:36:14
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】1 000 mL某待测溶液中除含有0.2 mol·L-1的Na+外,还可能含有下列离子中的一种或多种:
现进行如下实验操作(每次实验所加试剂均过量):
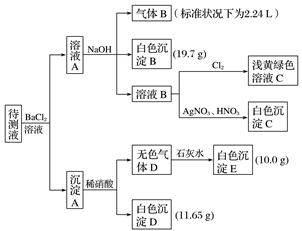
(1)写出生成白色沉淀B的离子方程式:__________________________________ 。
(2)待测液中肯定不存在的阳离子是________________ 。
(3)若无色气体D是单一气体:判断原溶液中K+是否存在____ (填“是”或“否”),若存在,求其物质的量浓度的最小值,若不存在,请说明理由:________________________ 。
(4)若无色气体D是混合气体:
①待测液中一定含有的阴离子是________________ 。
②沉淀A中能与稀硝酸反应的成分是____________ (写化学式)。
| 阳离子 | K+、NH 、Fe3+、Ba2+ 、Fe3+、Ba2+ |
| 阴离子 | Cl-、Br-、CO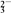 、HCO 、HCO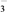 、SO 、SO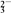 、SO 、SO |
现进行如下实验操作(每次实验所加试剂均过量):

(1)写出生成白色沉淀B的离子方程式:
(2)待测液中肯定不存在的阳离子是
(3)若无色气体D是单一气体:判断原溶液中K+是否存在
(4)若无色气体D是混合气体:
①待测液中一定含有的阴离子是
②沉淀A中能与稀硝酸反应的成分是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】某混合物的水溶液中,只可能含有以下离子中的若干种:K+、Ca2+、Fe3+、NH4+、Cl-、CO32- 和SO42-。现每次取100mL溶液进行实验:(已知:NH4++OH - = NH3↑ +H2O )
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体0.896 L(标准状况下)
③第三份加入足量BaCl2溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g。
请回答:
(1)c(CO32-) =_____________ mol/L;
(2)K+ 是否存在____________ ;若存在,浓度范围是__________________ (若不存在,则不必回答)。
(3)根据以上实验,不能判断是否存在的离子是____________ (填离子符号)。若存在此离子,请描述检验步骤__________________________________________________ 。
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体0.896 L(标准状况下)
③第三份加入足量BaCl2溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g。
请回答:
(1)c(CO32-) =
(2)K+ 是否存在
(3)根据以上实验,不能判断是否存在的离子是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】(1)当前频繁出现的雾霾天气与汽车尾气的排放有一定的关系,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。

写出净化过程中的总化学方程式:_______________________________________________ 。
(2)目前科学家也在尝试用Cu+作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:

①该过程中,还原剂是________ (填物质名称)。
②若某辆汽车的NO排放量为0.09 g·km-1,则该车行驶100 km,完成上述转化时,理论上需消耗乙烯的质量为________ g。
(3)为探究本地区雾霾中的可溶性颗粒的成分,某化学研究性小组进行了实验探究。
[查阅资料]雾霾颗粒样品中可能含有SO42-、CO32-、SO32-、HCO3-、NO3-、Cl-、Br-及一种常见阳离子(Mn+),现进行如下实验:

请回答下列问题:
①根据上述实验,雾霾浸取液中一定含有的离子为________ ,肯定没有的离子为________ 。
②若气体D遇空气会变成红棕色,则沉淀A中一定含有________ (填化学式)。

写出净化过程中的总化学方程式:
(2)目前科学家也在尝试用Cu+作催化剂,将汽车尾气中NO转化为无毒的N2。其原理如下图所示:

①该过程中,还原剂是
②若某辆汽车的NO排放量为0.09 g·km-1,则该车行驶100 km,完成上述转化时,理论上需消耗乙烯的质量为
(3)为探究本地区雾霾中的可溶性颗粒的成分,某化学研究性小组进行了实验探究。
[查阅资料]雾霾颗粒样品中可能含有SO42-、CO32-、SO32-、HCO3-、NO3-、Cl-、Br-及一种常见阳离子(Mn+),现进行如下实验:

请回答下列问题:
①根据上述实验,雾霾浸取液中一定含有的离子为
②若气体D遇空气会变成红棕色,则沉淀A中一定含有
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】铁是目前人类使用量最大的金属,它能形成多种化合物。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集了的气体体积均小于2.24 L(标准状况),最主要的原因是__________ ,所得溶液在长时间放置过程中会慢慢出现浅黄色,试用离子方程式解释这一变化的原因____________ 。
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox 和用于除去废气的转化关系如图 。若上述转化反应中消耗的
。若上述转化反应中消耗的 ,x的值为
,x的值为_________________ 。请写出 ZnFe2Ox与NO2反应的化学方程式______________ (x用前一问求出的具体值)。
(3)LiFePO4(难溶干水)材料被视为最有前途的锂离子电池材料之一。
①以 FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4 ,,该反应还生成一种可燃性气体,则反应方程式为____________ .
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负桩隔开)工作原理为 。则放电时正极上的电极反应式为
。则放电时正极上的电极反应式为___________ .
(4)已知25℃时, ,此温度下若在实验室中配制5 mol/L 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2 mol/L的盐酸
,此温度下若在实验室中配制5 mol/L 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2 mol/L的盐酸__________ ml(忽略加入盐酸体积)。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集了的气体体积均小于2.24 L(标准状况),最主要的原因是
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox 和用于除去废气的转化关系如图
 。若上述转化反应中消耗的
。若上述转化反应中消耗的 ,x的值为
,x的值为(3)LiFePO4(难溶干水)材料被视为最有前途的锂离子电池材料之一。
①以 FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4 ,,该反应还生成一种可燃性气体,则反应方程式为
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负桩隔开)工作原理为
 。则放电时正极上的电极反应式为
。则放电时正极上的电极反应式为(4)已知25℃时,
 ,此温度下若在实验室中配制5 mol/L 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2 mol/L的盐酸
,此温度下若在实验室中配制5 mol/L 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2 mol/L的盐酸
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】二元化合物X可由单质硫和Ca(OH)2浊液共热制得。取一定量X与100 mL 0.2 mol·L−1稀硫酸恰好完全反应,生成0.08 mol淡黄色沉淀和0.448 L气体甲(已折算为标准状况)。请回答:
(1) 甲的电子式为________ 。
(2) X的化学式为________ 。
(3) X与稀硫酸反应的化学方程式为________ 。
(4) 单质硫和Ca(OH)2浊液制X时,还生成另一种含氧酸盐(M<160 g·mol −1),该盐与稀硫酸反应也有淡黄色沉淀生成并放出刺激性气味气体,则单质硫与Ca(OH)2浊液反应制X的化学方程式为________ 。
(5) 气体甲通入硫酸铁溶液中能发生反应。请设计实验方案验证反应后溶液中除H+之外的阳离子________ 。
(1) 甲的电子式为
(2) X的化学式为
(3) X与稀硫酸反应的化学方程式为
(4) 单质硫和Ca(OH)2浊液制X时,还生成另一种含氧酸盐(M<160 g·mol −1),该盐与稀硫酸反应也有淡黄色沉淀生成并放出刺激性气味气体,则单质硫与Ca(OH)2浊液反应制X的化学方程式为
(5) 气体甲通入硫酸铁溶液中能发生反应。请设计实验方案验证反应后溶液中除H+之外的阳离子
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】常温下将一块钠露置在空气中一段时间后,甲、乙两位同学把固体分成两份,各取一份同时进行实验,欲探究其组成和含量。请根据要求回答下列问题。
甲同学:将一份放入烧瓶中,加入稀硫酸后,生成无色无味的气体,据分析推理可能有二氧化碳和氢气,然后进行气体成份的验证实验。
(1)为验证气体产物中是否含有二氧化碳和氢气,需从下图中选择必要的仪器和药品,设计一套装置验证气体成份。装置的连接顺序为:d→ _____ → _____ → _____ →
→ _____ → _____ 。(填下列装置的接口字母)________
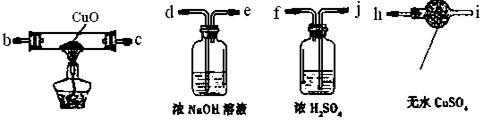
(2)实验过程中观察到石灰水变浑浊,由此可判断原固体中含有的物质是________
(填化学式)。
乙同学将另一份进行以下实验。
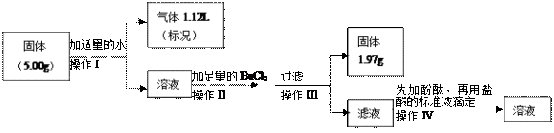
(3)用浓盐酸配制500mL 3.00mol·L-1的稀盐酸时,需要使用的玻璃仪器除了量筒、烧杯、胶头滴管、玻璃棒以外,还有________ 。
(4)在操作II中,发生反应的离子方程式为________ 。
(5)操作IV中用盐酸标准液滴定滤液时,滴定终点的现象是________ 。
(6)若操作IV中,消耗3.00mol·L-1的盐酸标准液50.00 mL,通过计算判断,5.00g固体中是否含有NaOH________ (填有或无),质量是________ g
(若你认为无NaOH,则此空不用答)。
甲同学:将一份放入烧瓶中,加入稀硫酸后,生成无色无味的气体,据分析推理可能有二氧化碳和氢气,然后进行气体成份的验证实验。
(1)为验证气体产物中是否含有二氧化碳和氢气,需从下图中选择必要的仪器和药品,设计一套装置验证气体成份。装置的连接顺序为:d→ _____ → _____ → _____ →
→ _____ → _____ 。(填下列装置的接口字母)

(2)实验过程中观察到石灰水变浑浊,由此可判断原固体中含有的物质是
(填化学式)。
乙同学将另一份进行以下实验。

(3)用浓盐酸配制500mL 3.00mol·L-1的稀盐酸时,需要使用的玻璃仪器除了量筒、烧杯、胶头滴管、玻璃棒以外,还有
(4)在操作II中,发生反应的离子方程式为
(5)操作IV中用盐酸标准液滴定滤液时,滴定终点的现象是
(6)若操作IV中,消耗3.00mol·L-1的盐酸标准液50.00 mL,通过计算判断,5.00g固体中是否含有NaOH
(若你认为无NaOH,则此空不用答)。
您最近一年使用:0次



