某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是____ 。
A.冷水B.沸水C.NaOH浓溶液D.NaCl浓溶液
(2)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备实验:
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。请评价该操作是否正确____ 。
②乙同学直接加热饱和FeCl3溶液,请评价是否正确____ 。
③丙同学向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确__ 。
(3)写出制备Fe(OH)3胶体的化学方程式:_____ 。证明有Fe(OH)3胶体生成的实验操作是________ 。利用的胶体性质是___ 。
(4)Fe(OH)3胶体稳定存在的主要原因是___ 。
A.胶粒直径小于1 nm B.胶粒带正电荷
C.胶粒作布朗运动D.胶粒能透过滤纸
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是
A.冷水B.沸水C.NaOH浓溶液D.NaCl浓溶液
(2)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备实验:
①甲同学的操作是:取一小烧杯,加入25 mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2 mL FeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。请评价该操作是否正确
②乙同学直接加热饱和FeCl3溶液,请评价是否正确
③丙同学向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟,请评价是否正确
(3)写出制备Fe(OH)3胶体的化学方程式:
(4)Fe(OH)3胶体稳定存在的主要原因是
A.胶粒直径小于1 nm B.胶粒带正电荷
C.胶粒作布朗运动D.胶粒能透过滤纸
更新时间:2019-11-22 14:47:57
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】将少量FeCl3饱和溶液分别滴加到下列物质中,得到三种分散系
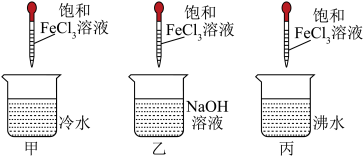
(1)将丙继续加热煮沸至液体呈红褐色,反应的化学方程式为__________
(2)用最简单判断丙中是否成功制备胶体的方法叫____ ;具体操作:______
(3)向经过检验后的丙中逐滴加入盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因是_____________
②随后发生变化得到和甲相同的溶液,此反应的离子方程式是______

(1)将丙继续加热煮沸至液体呈红褐色,反应的化学方程式为
(2)用最简单判断丙中是否成功制备胶体的方法叫
(3)向经过检验后的丙中逐滴加入盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因是
②随后发生变化得到和甲相同的溶液,此反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
甲同学:向 的氯化铁溶液中加入少量的NaOH溶液。
的氯化铁溶液中加入少量的NaOH溶液。
乙同学:直接加热饱和 溶液。
溶液。
丙同学:向25mL沸水中逐滴加入5~6滴 饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是_______ (填“甲”“乙”或“丙”)。
(2)证明有 胶体生成的实验操作是
胶体生成的实验操作是_______ 利用的胶体性质是_______ 。
(3)在胶体中加入电解质溶液或带有相反电荷的胶体粒子能使胶体粒子沉淀出来。丁同学利用制得的 胶体进行下列实验:
胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的液体颜色逐渐变深,这表明 胶体微粒带
胶体微粒带_______ (带“正”或“负”)电荷。
②实验证明,电解质的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝聚力越大。向 胶体加入下列电解质时,其凝聚能力最强的为
胶体加入下列电解质时,其凝聚能力最强的为_______ 。
A.NaCl B. C.
C. D.
D.
(4)写出实验室制备 胶体的化学方程式:
胶体的化学方程式:_______ 。
 胶体的制备实验。
胶体的制备实验。甲同学:向
 的氯化铁溶液中加入少量的NaOH溶液。
的氯化铁溶液中加入少量的NaOH溶液。乙同学:直接加热饱和
 溶液。
溶液。丙同学:向25mL沸水中逐滴加入5~6滴
 饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
饱和溶液;继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是
(2)证明有
 胶体生成的实验操作是
胶体生成的实验操作是(3)在胶体中加入电解质溶液或带有相反电荷的胶体粒子能使胶体粒子沉淀出来。丁同学利用制得的
 胶体进行下列实验:
胶体进行下列实验:①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的液体颜色逐渐变深,这表明
 胶体微粒带
胶体微粒带②实验证明,电解质的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝聚力越大。向
 胶体加入下列电解质时,其凝聚能力最强的为
胶体加入下列电解质时,其凝聚能力最强的为A.NaCl B.
 C.
C. D.
D.
(4)写出实验室制备
 胶体的化学方程式:
胶体的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】现有A、B、C三种气体,常温下,A是密度最小的气体,B是黄绿色单质气体,纯净的A可以在B中安静地燃烧,生成C。
(1)写出A在B中燃烧的化学方程式________ 。
(2)把A、B、C三种气体分别通入硝酸酸化的硝酸银溶液中,出现白色沉淀的气体是___________ (用字母表示)。
(3)气体B通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合液,经测定Cl-与 的个数比为11∶2,则所得溶液中ClO-与
的个数比为11∶2,则所得溶液中ClO-与 的个数比为
的个数比为___________ 。
(4)金属Fe在B中燃烧的产物溶于水可以得到棕黄色溶液,某同学想利用该溶液来制备Fe(OH)3胶体:
①判断胶体制备成功的方法是_______ 。
②向制得的Fe(OH)3胶体中逐滴滴加稀盐酸,开始产生红褐色沉淀,这是因为______ ,继续滴加,沉淀减少最终消失,写出离子反应方程式______ 。
(1)写出A在B中燃烧的化学方程式
(2)把A、B、C三种气体分别通入硝酸酸化的硝酸银溶液中,出现白色沉淀的气体是
(3)气体B通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合液,经测定Cl-与
 的个数比为11∶2,则所得溶液中ClO-与
的个数比为11∶2,则所得溶液中ClO-与 的个数比为
的个数比为(4)金属Fe在B中燃烧的产物溶于水可以得到棕黄色溶液,某同学想利用该溶液来制备Fe(OH)3胶体:
①判断胶体制备成功的方法是
②向制得的Fe(OH)3胶体中逐滴滴加稀盐酸,开始产生红褐色沉淀,这是因为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】将少量FeCl3饱和溶液分别滴加到下列物质中,得到三种分散系

(1)将丙继续加热煮沸至液体呈红褐色,反应的化学方程式为__________
(2)用最简单判断丙中是否成功制备胶体的方法叫____ ;具体操作:______
(3)向经过检验后的丙中逐滴加入盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因是_____________
②随后发生变化得到和甲相同的溶液,此反应的离子方程式是______

(1)将丙继续加热煮沸至液体呈红褐色,反应的化学方程式为
(2)用最简单判断丙中是否成功制备胶体的方法叫
(3)向经过检验后的丙中逐滴加入盐酸,会出现一系列变化:
①先出现和乙中相同的现象,原因是
②随后发生变化得到和甲相同的溶液,此反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
甲同学:向 的氯化铁溶液中加入少量的NaOH溶液。
的氯化铁溶液中加入少量的NaOH溶液。
乙同学:直接加热饱和 溶液。
溶液。
丙同学:向25mL沸水中逐滴加入5~6滴 饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(1)其中操作正确的同学是_______ (填“甲”“乙”或“丙”)。
(2)证明有 胶体生成的实验操作是
胶体生成的实验操作是_______ 利用的胶体性质是_______ 。
(3)在胶体中加入电解质溶液或带有相反电荷的胶体粒子能使胶体粒子沉淀出来。丁同学利用制得的 胶体进行下列实验:
胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的液体颜色逐渐变深,这表明 胶体微粒带
胶体微粒带_______ (带“正”或“负”)电荷。
②实验证明,电解质的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝聚力越大。向 胶体加入下列电解质时,其凝聚能力最强的为
胶体加入下列电解质时,其凝聚能力最强的为_______ 。
A.NaCl B. C.
C. D.
D.
(4)写出实验室制备 胶体的化学方程式:
胶体的化学方程式:_______ 。
 胶体的制备实验。
胶体的制备实验。甲同学:向
 的氯化铁溶液中加入少量的NaOH溶液。
的氯化铁溶液中加入少量的NaOH溶液。乙同学:直接加热饱和
 溶液。
溶液。丙同学:向25mL沸水中逐滴加入5~6滴
 饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
饱和溶液;继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是
(2)证明有
 胶体生成的实验操作是
胶体生成的实验操作是(3)在胶体中加入电解质溶液或带有相反电荷的胶体粒子能使胶体粒子沉淀出来。丁同学利用制得的
 胶体进行下列实验:
胶体进行下列实验:①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的液体颜色逐渐变深,这表明
 胶体微粒带
胶体微粒带②实验证明,电解质的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝聚力越大。向
 胶体加入下列电解质时,其凝聚能力最强的为
胶体加入下列电解质时,其凝聚能力最强的为A.NaCl B.
 C.
C. D.
D.
(4)写出实验室制备
 胶体的化学方程式:
胶体的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】将少量饱和 溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
甲:饱和 溶液滴加到冷水中;乙:饱和
溶液滴加到冷水中;乙:饱和 溶液滴加到
溶液滴加到 溶液中;
溶液中;
丙:饱和 溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
(1)以上三种操作得到的分散系中,分散质粒子直径最大的是_______ (填甲、乙、丙),名称是_______ ,乙中实验现象是:_______ 。
(2)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为_______ 。
(3)判断丙中成功制备胶体的操作方法是_______ (描述操作过程)。
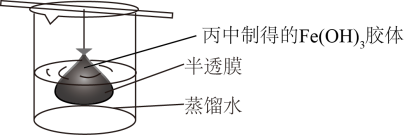
(4)可用如图所示的装置除去 胶体中的杂质离子来提纯
胶体中的杂质离子来提纯 胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入
胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入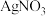 溶液,若
溶液,若_______ (填实验现象),则说明该 胶体中的杂质离子已经完全除去。
胶体中的杂质离子已经完全除去。
 溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:甲:饱和
 溶液滴加到冷水中;乙:饱和
溶液滴加到冷水中;乙:饱和 溶液滴加到
溶液滴加到 溶液中;
溶液中;丙:饱和
 溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。(1)以上三种操作得到的分散系中,分散质粒子直径最大的是
(2)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为
(3)判断丙中成功制备胶体的操作方法是
(4)可用如图所示的装置除去
 胶体中的杂质离子来提纯
胶体中的杂质离子来提纯 胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入
胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入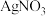 溶液,若
溶液,若 胶体中的杂质离子已经完全除去。
胶体中的杂质离子已经完全除去。
您最近一年使用:0次



