写出下列离子方程式
(1)氯化亚铁溶液和氯气反应生成氯化铁_________________________________ 。
(2)澄清石灰水通入氯气的反应___________________________ 。
(3)实验室制取二氧化碳____________________________ 。
(4)澄清石灰水通入二氧化碳变浑浊___________________________ 。
(5)纯碱溶液与氯化钡溶液混合____________________________ 。
(1)氯化亚铁溶液和氯气反应生成氯化铁
(2)澄清石灰水通入氯气的反应
(3)实验室制取二氧化碳
(4)澄清石灰水通入二氧化碳变浑浊
(5)纯碱溶液与氯化钡溶液混合
更新时间:2019-12-03 18:38:37
|
【知识点】 离子反应的发生及书写
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)现有以下物质:a.NaOH溶液,b.液氨,c. 固体,d.
固体,d. ,e.
,e. 胶体,f.铜,g.
胶体,f.铜,g. ,h.
,h. 。
。
①以上物质中属于非电解质的是___________ (填字母)。
②写出d在水溶液中电离方程式:___________ 。
③在足量d的水溶液中加入少量c的水溶液,发生反应的离子方程式为___________ 。
(2)三氟化氮( )是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有HF、NO和
)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有HF、NO和 写出该反应的化学方程式:
写出该反应的化学方程式:___________ ,若反应中生成0.2 mol  ,转移的电子数为
,转移的电子数为___________ 。反应过程中,被氧化与被还原的元素原子的物质的量之比为___________ 。
(3) 与NaOH和NaClO的混合液作用,是制备理想的绿色水处理剂(
与NaOH和NaClO的混合液作用,是制备理想的绿色水处理剂( )的一种方法。试写出此反应的方程式
)的一种方法。试写出此反应的方程式___________
(4)我国科学家设计协同转化装置处理尾气 。为避免硫磺沉积在Y极,将氧化吸收和电解过程分开进行,装置如图所示(电解反应器中,以石墨为电极)。
。为避免硫磺沉积在Y极,将氧化吸收和电解过程分开进行,装置如图所示(电解反应器中,以石墨为电极)。

① 通过质子交换膜移向
通过质子交换膜移向___________ (填“X”或“Y”)极区。
②协同转化装置实现物质转化的总反应方程式为___________ 。
(1)现有以下物质:a.NaOH溶液,b.液氨,c.
 固体,d.
固体,d. ,e.
,e. 胶体,f.铜,g.
胶体,f.铜,g. ,h.
,h. 。
。①以上物质中属于非电解质的是
②写出d在水溶液中电离方程式:
③在足量d的水溶液中加入少量c的水溶液,发生反应的离子方程式为
(2)三氟化氮(
 )是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有HF、NO和
)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有HF、NO和 写出该反应的化学方程式:
写出该反应的化学方程式: ,转移的电子数为
,转移的电子数为(3)
 与NaOH和NaClO的混合液作用,是制备理想的绿色水处理剂(
与NaOH和NaClO的混合液作用,是制备理想的绿色水处理剂( )的一种方法。试写出此反应的方程式
)的一种方法。试写出此反应的方程式(4)我国科学家设计协同转化装置处理尾气
 。为避免硫磺沉积在Y极,将氧化吸收和电解过程分开进行,装置如图所示(电解反应器中,以石墨为电极)。
。为避免硫磺沉积在Y极,将氧化吸收和电解过程分开进行,装置如图所示(电解反应器中,以石墨为电极)。
①
 通过质子交换膜移向
通过质子交换膜移向②协同转化装置实现物质转化的总反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组对NaHSO4的性质进行了如下探究。
(1)下列关于NaHSO4的说法中正确的是___________。
(2)取少量的NaHSO4溶液,滴加2-3滴石蕊试液,现象是___________ 。
(3)向NaHSO4溶液中滴加NaHCO3溶液,反应的离子方程式为___________ 。在两份相同的Ba(OH)2溶液中,分别滴入相同浓度的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
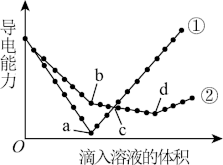
(4)图中①代表滴加___________ (填化学式)溶液的曲线,导电能力变化的原因是___________ 。
(5)b点溶液中大量存在的离子是___________ 。
(6)___________ 点对应的溶液呈中性(填a、b、c、d,下同);___________ 点对应的溶液中Ba2+恰好沉淀完全。
(7)写出bd段发生的离子方程式___________ 。
(1)下列关于NaHSO4的说法中正确的是___________。
| A.因为NaHSO4是离子化合物,所以NaHSO4固体能够导电 |
| B.NaHSO4固体中正离子和负离子的个数比是2∶1 |
| C.NaHSO4固体熔化时破坏的是离子键和共价键 |
| D.NaHSO4固体溶于水时破坏的是离子键和共价键 |
(3)向NaHSO4溶液中滴加NaHCO3溶液,反应的离子方程式为

(4)图中①代表滴加
(5)b点溶液中大量存在的离子是
(6)
(7)写出bd段发生的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)在盛有淀粉KI溶液(用H2SO4酸化)的试管中,滴加少量的次氯酸钠溶液,会立即看到溶液变成蓝色,相应的离子方程式为______________________________ 。在盛有淀粉和碘形成的蓝色溶液中,滴加Na2SO3溶液,又发现蓝色溶液逐渐消失,相应的离子方程式为_______________________ 。对比上述两组实验所得结果,可得出ClO-、I2、SO42-的氧化性由强到弱的顺序为 _____________________ 。
(2)氯酸是一种强酸,氯酸的浓度超过40%,就会迅速分解,产生比它的酸性更强的酸,同时放出气体,该气体混合物经干燥后,平均分子量为47.6,它可以使带火星的木条复燃,并可使润湿的淀粉一碘化钾试纸变蓝。试完成下列各题:
(a)该气体的组成是__________ ,气体混合物中各成分的物质的量比为_________ 。
(b)写出氯酸分解的化学反应方程式____________________________________________ ,该反应的氧化产物是____________ (写化学式)。
(2)氯酸是一种强酸,氯酸的浓度超过40%,就会迅速分解,产生比它的酸性更强的酸,同时放出气体,该气体混合物经干燥后,平均分子量为47.6,它可以使带火星的木条复燃,并可使润湿的淀粉一碘化钾试纸变蓝。试完成下列各题:
(a)该气体的组成是
(b)写出氯酸分解的化学反应方程式
您最近一年使用:0次



