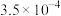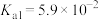某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、量筒、0.5mol·L-1盐酸、0.55mol·L-1NaOH溶液,实验尚缺少的玻璃用品是__ 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒__ (填“能”或“否”),其原因是__ 。
(3)他们记录的实验数据如下:
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18kJ·℃-1·kg-1,各物质的密度均为1g·cm-3。
①计算完成上表。___
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:__ 。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、量筒、0.5mol·L-1盐酸、0.55mol·L-1NaOH溶液,实验尚缺少的玻璃用品是
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | ΔH | |||
| ① | 50mL0.55mol·L-1NaOH溶液 | 50mL0.5mol·L-1溶液 | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol·L-1NaOH溶液 | 50mL0.5mol·L-1HCl溶液 | 20℃ | 23.5℃ | |
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18kJ·℃-1·kg-1,各物质的密度均为1g·cm-3。
①计算完成上表。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:
19-20高二上·四川遂宁·阶段练习 查看更多[2]
更新时间:2019-12-20 19:18:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求填空。
Ⅰ.已知:298K时,1mol相关物质的相对能量如图所示。

(1)写出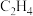 完全燃烧生成气态水的热化学方程式:
完全燃烧生成气态水的热化学方程式:__________ 。
(2)由甲烷制取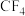 的原理为
的原理为
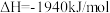 ,断裂1mol化学键所吸收的能量如下表所示:
,断裂1mol化学键所吸收的能量如下表所示:
则形成1molF-F键所释放的能量为__________ kJ。
Ⅱ.实验室用 盐酸、
盐酸、 溶液和如图所示装置进行中和反应反应热测定实验,得到如表所示数据:
溶液和如图所示装置进行中和反应反应热测定实验,得到如表所示数据:

(3)根据表中所测数据进行计算,则该实验测得的中和热△H=__________  [假设盐酸和NaOH溶液的密度按
[假设盐酸和NaOH溶液的密度按 计算,反应后混合溶液的比热容(c)按
计算,反应后混合溶液的比热容(c)按 计算,结果保留1位小数]。
计算,结果保留1位小数]。
(4)下列说法正确的是__________。
Ⅰ.已知:298K时,1mol相关物质的相对能量如图所示。

(1)写出
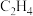 完全燃烧生成气态水的热化学方程式:
完全燃烧生成气态水的热化学方程式:(2)由甲烷制取
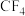 的原理为
的原理为
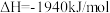 ,断裂1mol化学键所吸收的能量如下表所示:
,断裂1mol化学键所吸收的能量如下表所示:| 化学键 |  |  |  |
| 能量/kJ | 414 | 489 | 565 |
Ⅱ.实验室用
 盐酸、
盐酸、 溶液和如图所示装置进行中和反应反应热测定实验,得到如表所示数据:
溶液和如图所示装置进行中和反应反应热测定实验,得到如表所示数据:
| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
(3)根据表中所测数据进行计算,则该实验测得的中和热△H=
 [假设盐酸和NaOH溶液的密度按
[假设盐酸和NaOH溶液的密度按 计算,反应后混合溶液的比热容(c)按
计算,反应后混合溶液的比热容(c)按 计算,结果保留1位小数]。
计算,结果保留1位小数]。(4)下列说法正确的是__________。
| A.在实验操作时,若未用水把温度计上的酸冲洗干净,实验测得的“中和热”数值将偏小 |
| B.用玻璃搅拌器搅拌时应围绕温度计旋转做圆周运动 |
C.将一定量的浓氢氧化钠溶液、稀氢氧化钙溶液分别和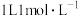 的稀盐酸恰好完全反应,其反应热分别为 的稀盐酸恰好完全反应,其反应热分别为 、 、 ,则 ,则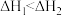 |
| D.可用耐酸碱的塑料材质的搅拌器代替玻璃搅拌器 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.25℃时,三种酸的电离平衡常数如下表所示。
(1)三种酸的酸性由强到弱的顺序为____________________ (填化学式)。
(2)将pH和体积均相同的 溶液和HF溶液分别稀释,其pH随加水体积的变化如图所示。
溶液和HF溶液分别稀释,其pH随加水体积的变化如图所示。

①稀释前
__________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
②a、b两点:
__________ 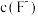 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(3)在NaF溶液中滴加少量的草酸溶液,发生反应的离子反应方程式为____________________ 。
II.分别取40mL的 盐酸与40mL的
盐酸与40mL的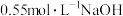 溶液进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
溶液进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
某学生实验记录数据如下:
(4)近似认为 的NaOH溶液和
的NaOH溶液和 的盐酸的密度都是
的盐酸的密度都是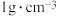 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 ,则中和热
,则中和热
__________ (取小数点后一位)。
(5)用相同浓度和体积的醋酸代替盐酸溶液进行上述实验,测得的中和热数值(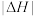 )会
)会__________ (填“偏大”“偏小”或“无影响”)。
| 名称 | 醋酸 | 氢氟酸 | 草酸 |
| 化学式 |
| HF |
|
| 电离平衡常数 |
|
|
|
(2)将pH和体积均相同的
 溶液和HF溶液分别稀释,其pH随加水体积的变化如图所示。
溶液和HF溶液分别稀释,其pH随加水体积的变化如图所示。
①稀释前

 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。②a、b两点:

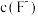 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(3)在NaF溶液中滴加少量的草酸溶液,发生反应的离子反应方程式为
II.分别取40mL的
 盐酸与40mL的
盐酸与40mL的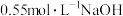 溶液进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
溶液进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:某学生实验记录数据如下:
| 实验序号 | 起始温度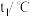 | 终止温度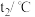 | |
| 盐酸 | NaOH | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
 的NaOH溶液和
的NaOH溶液和 的盐酸的密度都是
的盐酸的密度都是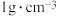 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 ,则中和热
,则中和热
(5)用相同浓度和体积的醋酸代替盐酸溶液进行上述实验,测得的中和热数值(
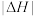 )会
)会
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
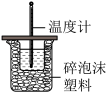
(1)从实验装置上看,图中尚缺少的一种玻璃用品是____________ ;
(2)用相同浓度和体积的醋酸代替稀盐酸溶液进行实验,求得的中和热数值__________ (填“偏大”、“偏小”或“无影响”);
(3)实验中改用60mL 0.50mol/L 盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”),所求中和热_______ (填“相等”或“不相等”)

(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)用相同浓度和体积的醋酸代替稀盐酸溶液进行实验,求得的中和热数值
(3)实验中改用60mL 0.50mol/L 盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】下图是用0.1000mol/L的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前、后盛放盐酸的滴定管中液面的位置。
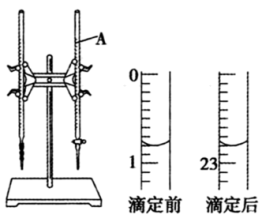
请回答下列问题;
(1)仪器A的名称是___________ 。
(2)盐酸的体积读数:滴定前读数为___________ mL。
(3)某实验小组同学的三次实验的实验数据如下表所示。根据表中数据计算出标准溶液盐酸的平均体积为___________ ,待测NaOH溶液的平均浓度是___________ mol/L(保留四位有效数字)
(4)对下列几种假定情况进行讨论(填“无影响”“偏高”或“偏低”):
①取待测液的滴定管,取液前滴定管尖端有气泡,取液后气泡消失,对测定结果的影响是___________ ;
②若滴定前前锥形瓶未用待测液润洗,对测定结果的影响是___________ ;
③标准液读数时,若滴定前俯视,滴定后仰视,对测定结果的影响是___________ 。

请回答下列问题;
(1)仪器A的名称是
(2)盐酸的体积读数:滴定前读数为
(3)某实验小组同学的三次实验的实验数据如下表所示。根据表中数据计算出标准溶液盐酸的平均体积为
| 实验编号 | 待测NaOH溶液的体积/mL | 滴定前盐酸的体积读数/mL | 滴定后盐酸的体积读数/mL |
| 1 | 20.00 | 1.20 | 23.22 |
| 2 | 20.00 | 1.21 | 29.21 |
| 3 | 20.00 | 1.50 | 23.48 |
①取待测液的滴定管,取液前滴定管尖端有气泡,取液后气泡消失,对测定结果的影响是
②若滴定前前锥形瓶未用待测液润洗,对测定结果的影响是
③标准液读数时,若滴定前俯视,滴定后仰视,对测定结果的影响是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷能形成多种含氧酸,请回答下列问题:
(1)工业上常用磷精矿[ ]与硫酸反应制备磷酸。已知25℃,101kPa时。
]与硫酸反应制备磷酸。已知25℃,101kPa时。

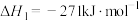
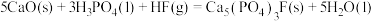

则 与硫酸反应生成磷酸的热化学方程式为
与硫酸反应生成磷酸的热化学方程式为___________ 。
(2)次磷酸( )是一种精细化工产品,向
)是一种精细化工产品,向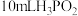 溶液中加入30mL等物质的量浓度的NaOH溶液后,所得到的溶液中只有
溶液中加入30mL等物质的量浓度的NaOH溶液后,所得到的溶液中只有 、
、 两种阴离子。
两种阴离子。
①写出 溶液与足量NaOH溶液反应后所形成的正盐的化学式:
溶液与足量NaOH溶液反应后所形成的正盐的化学式:___________ 。
②常温下, 的
的 溶液在加水稀释过程中,下列表达式的数值一定减小的是
溶液在加水稀释过程中,下列表达式的数值一定减小的是___________ (填字母)。
A. B.
B. C.
C.
(3)亚磷酸( )是二元中强酸,25℃时其电离常数为
)是二元中强酸,25℃时其电离常数为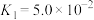 、
、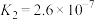 。
。
①试从电离平衡移动的角度解释 、
、 数据的差异:
数据的差异:___________ 。
② 是
是___________ (填“酸式盐”“碱式盐”或“正盐”)。
(4)已知25℃时,HF的电离常数为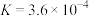 ;
; 的电离常数为
的电离常数为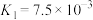 ,
,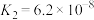 ,
,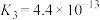 。
。
①足量NaF溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
②已知:
 ,则
,则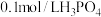 溶液与足量0.1mol/LNaOH溶液反应生成
溶液与足量0.1mol/LNaOH溶液反应生成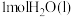 放出的热量
放出的热量___________ (填字母)。
A.等于57.3kJ B.小于57.3kJ C.大于57.3kJ D.无法确定
(1)工业上常用磷精矿[
 ]与硫酸反应制备磷酸。已知25℃,101kPa时。
]与硫酸反应制备磷酸。已知25℃,101kPa时。
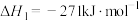
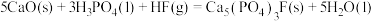

则
 与硫酸反应生成磷酸的热化学方程式为
与硫酸反应生成磷酸的热化学方程式为(2)次磷酸(
 )是一种精细化工产品,向
)是一种精细化工产品,向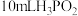 溶液中加入30mL等物质的量浓度的NaOH溶液后,所得到的溶液中只有
溶液中加入30mL等物质的量浓度的NaOH溶液后,所得到的溶液中只有 、
、 两种阴离子。
两种阴离子。①写出
 溶液与足量NaOH溶液反应后所形成的正盐的化学式:
溶液与足量NaOH溶液反应后所形成的正盐的化学式:②常温下,
 的
的 溶液在加水稀释过程中,下列表达式的数值一定减小的是
溶液在加水稀释过程中,下列表达式的数值一定减小的是A.
 B.
B. C.
C.
(3)亚磷酸(
 )是二元中强酸,25℃时其电离常数为
)是二元中强酸,25℃时其电离常数为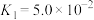 、
、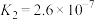 。
。①试从电离平衡移动的角度解释
 、
、 数据的差异:
数据的差异:②
 是
是(4)已知25℃时,HF的电离常数为
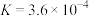 ;
; 的电离常数为
的电离常数为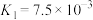 ,
,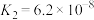 ,
,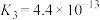 。
。①足量NaF溶液与
 溶液反应的离子方程式为
溶液反应的离子方程式为②已知:

 ,则
,则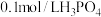 溶液与足量0.1mol/LNaOH溶液反应生成
溶液与足量0.1mol/LNaOH溶液反应生成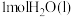 放出的热量
放出的热量A.等于57.3kJ B.小于57.3kJ C.大于57.3kJ D.无法确定
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)终点的判断:溶液由_______ 。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是( )
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
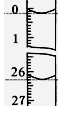
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为_______ mL。
(4)某学生根据3次实验分别记录有关数据如表:
②依据上表数据列式计算该NaOH溶液的物质的量浓度_______ (计算结果取4位有效数)。
(1)终点的判断:溶液由
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸溶液的体积为

(4)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.1000 mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 平均耗用盐酸 体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.15 | ①V= |
| 第二次 | 25.00 | 0.56 | 30.30 | |
| 第三次 | 25.00 | 0.20 | 26.45 | |
②依据上表数据列式计算该NaOH溶液的物质的量浓度
您最近半年使用:0次