今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各100mL该溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.08mol;
③第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,回答下列问题:
(1)由第二份进行的实验得知混合物中应含有___________ 离子,其物质的量浓度为________ 。
(2)由第三份进行的实验可知12.54克沉淀的成分是______________ (写沉淀化学式),其物质的量分别为______________________ 。
(3)原溶液中是否存在K+_______ 填“是”或“否)若存在则K+的浓度的取值范围是____________________ (若不存在此空可不填)
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.08mol;
③第三份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,回答下列问题:
(1)由第二份进行的实验得知混合物中应含有
(2)由第三份进行的实验可知12.54克沉淀的成分是
(3)原溶液中是否存在K+
更新时间:2020-01-12 22:06:59
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有一混合溶液,只可能含有以下离子中的若干种:H+、Na+、K+、Cl-、Ca2+、 、
、 ,取少量该混合溶液进行如下实验。
,取少量该混合溶液进行如下实验。
实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,火焰为黄色;
实验②:向混合溶液中加入足量BaCl2溶液后,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解,产生气泡;
实验④:向②过滤后的溶液加入硝酸银,产生白色沉淀。
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液中一定含有___________ (填离子符号,下同)
(2)由实验②③推断该混合溶液中一定含有___________ ,一定不含有___________ 。请写出实验③中反应的离子方程式:___________
(3)综合上述实验,是否能确定该混合溶液中含有Cl-:___________ (填“是”或“否”)。若“是”本空无需作答,若“否”请写出检验该混合溶液中Cl-的实验操作及现象:___________ 。
 、
、 ,取少量该混合溶液进行如下实验。
,取少量该混合溶液进行如下实验。实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,火焰为黄色;
实验②:向混合溶液中加入足量BaCl2溶液后,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解,产生气泡;
实验④:向②过滤后的溶液加入硝酸银,产生白色沉淀。
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液中一定含有
(2)由实验②③推断该混合溶液中一定含有
(3)综合上述实验,是否能确定该混合溶液中含有Cl-:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】现有含NaCl、MgCl2和Na2SO4的混合溶液,某兴趣小组的同学欲提取纯净的NaCl晶体,设计了如下实验:

请回答下列问题:
(1)写出沉淀Ⅰ和沉淀Ⅱ所含物质的化学式。沉淀Ⅰ:_________ 、沉淀Ⅱ:_______ 。
(2)上述流程中,加入过量稀盐酸的目的是______________ 。
(3)操作Ⅲ中需使用的玻璃仪器是________________________ 。

请回答下列问题:
(1)写出沉淀Ⅰ和沉淀Ⅱ所含物质的化学式。沉淀Ⅰ:
(2)上述流程中,加入过量稀盐酸的目的是
(3)操作Ⅲ中需使用的玻璃仪器是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氢氧化钴[Co(OH)2]是锂电池正极材料钴酸锂(LiCoO2)的前驱体。以CoSO4溶液、NaOH溶液、氨水和水合肼为原料可制得微米级Co(OH)2。
已知:①Co2+、Co3+易与NH3形成络合物, 的还原性强于Co(OH)2和Co2+;
的还原性强于Co(OH)2和Co2+;
②水合肼(N2H4·H2O)为无色油状液体,具有强还原性,氧化产物为N2;
③沉淀的生成速率越快,颗粒越小,呈凝乳状或胶体,不易过滤。
(1)60℃时在搅拌下向CoSO4溶液中加入氨水,调节pH至6后,再加入NaOH溶液,调节pH至9.5左右,一段时间后,过滤、洗涤,真空烘干得微米级Co(OH)2。
①制备时,在加入NaOH溶液前必须先加氨水的原因是_______ 。
②洗涤时,使用热水除去产品表面杂质,检验产品是否洗净的实验操作是_______ 。
(2)经仪器分析,测得按题(1)步骤制得的Co(OH)2晶体结构中含有Co(Ⅲ),进一步用碘量法测得Co(Ⅱ)的氧化程度为8%。因此制备时必须加入一定量的还原剂。
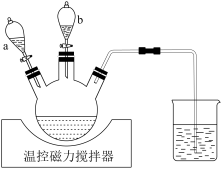
①将500 mL1 mol/L的CoSO4溶液与氨水配成pH为6的溶液,加入三颈烧瓶中(装置见如图),滴液漏斗a装有NaOH溶液、b中装有水合肼。60℃时依次将两种溶液加入三颈烧瓶,充分反应后,过滤。实验时应先打开滴液漏斗_______ (填“a”或“b”)。
②为确保制得的Co(OH)2产品中不含Co(Ⅲ),制备时至少需加入水合肼的质量为_______ g。
(3)以废旧锂电池正极材料(含LiCoO2,以及少量Al、Fe等)为原料制备微米级氢氧化钴。已知:酸性条件下的氧化性强弱顺序为:Co3+>H2O2>Cl2>Fe3+;LiOH可溶于水;下表是部分金属离子生成氢氧化物沉淀的pH。
请补充完整实验方案:取一定量废旧锂电池正极材料,粉碎后与Na2SO3溶液配成悬浊液,在搅拌下_______ ,调节pH至9.5,过滤、洗涤,真空烘干得到微米级Co(OH)2。实验中可选用的试剂:1 mol/LH2SO4溶液、2 mol/L HCl溶液、5 mol/LNaOH溶液、5 mol/L氨水、30%H2O2溶液。
已知:①Co2+、Co3+易与NH3形成络合物,
 的还原性强于Co(OH)2和Co2+;
的还原性强于Co(OH)2和Co2+;②水合肼(N2H4·H2O)为无色油状液体,具有强还原性,氧化产物为N2;
③沉淀的生成速率越快,颗粒越小,呈凝乳状或胶体,不易过滤。
(1)60℃时在搅拌下向CoSO4溶液中加入氨水,调节pH至6后,再加入NaOH溶液,调节pH至9.5左右,一段时间后,过滤、洗涤,真空烘干得微米级Co(OH)2。
①制备时,在加入NaOH溶液前必须先加氨水的原因是
②洗涤时,使用热水除去产品表面杂质,检验产品是否洗净的实验操作是
(2)经仪器分析,测得按题(1)步骤制得的Co(OH)2晶体结构中含有Co(Ⅲ),进一步用碘量法测得Co(Ⅱ)的氧化程度为8%。因此制备时必须加入一定量的还原剂。

①将500 mL1 mol/L的CoSO4溶液与氨水配成pH为6的溶液,加入三颈烧瓶中(装置见如图),滴液漏斗a装有NaOH溶液、b中装有水合肼。60℃时依次将两种溶液加入三颈烧瓶,充分反应后,过滤。实验时应先打开滴液漏斗
②为确保制得的Co(OH)2产品中不含Co(Ⅲ),制备时至少需加入水合肼的质量为
(3)以废旧锂电池正极材料(含LiCoO2,以及少量Al、Fe等)为原料制备微米级氢氧化钴。已知:酸性条件下的氧化性强弱顺序为:Co3+>H2O2>Cl2>Fe3+;LiOH可溶于水;下表是部分金属离子生成氢氧化物沉淀的pH。
| 金属离子 | Co2+ | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀的pH | 7.6 | 7.6 | 2.7 | 4.0 |
| 沉淀完全的pH | 9.2 | 9.6 | 3.7 | 5.2 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某地区的雾霾中含有含有K+、Ca2+、Na+、Mg2+、Cl−、SO 、CO
、CO 离子中的若干种。某同学收集雾霾样品,经必要预处理配成试样溶液,为确定其溶液的组成,进行如下实验探究:
离子中的若干种。某同学收集雾霾样品,经必要预处理配成试样溶液,为确定其溶液的组成,进行如下实验探究:
①向一定体积的试样溶液中加入1.00 mol/L的BaCl2溶液300 mL,恰好可以将溶液中的某种或某些离子完全沉淀,过滤得62.7 g沉淀及滤液。
②向上述沉淀中加入过量的盐酸,产生的气体通入足量澄清的石灰水中,得到一定量的沉淀X。
③向上述滤液中加入 AgNO3溶液,产生白色沉淀。
据此,请回答下列问题(用相应的离子符号表示):
(1)上述实验②中得到沉淀X的质量为_______ g;生成沉淀X的离子方程式为_______ 。
(2)试样溶液中一定不存在的离子是_______ ;肯定存在的离子是_______ ;不能确定是否存在的阴离子是_______ ,为确定该离子是否存在,可以向该试样溶液中加入足量_______ 溶液。
(3)为确定试样溶液中存在的阳离子,可采用的方法为_______ (填操作名称即可)。
 、CO
、CO 离子中的若干种。某同学收集雾霾样品,经必要预处理配成试样溶液,为确定其溶液的组成,进行如下实验探究:
离子中的若干种。某同学收集雾霾样品,经必要预处理配成试样溶液,为确定其溶液的组成,进行如下实验探究:①向一定体积的试样溶液中加入1.00 mol/L的BaCl2溶液300 mL,恰好可以将溶液中的某种或某些离子完全沉淀,过滤得62.7 g沉淀及滤液。
②向上述沉淀中加入过量的盐酸,产生的气体通入足量澄清的石灰水中,得到一定量的沉淀X。
③向上述滤液中加入 AgNO3溶液,产生白色沉淀。
据此,请回答下列问题(用相应的离子符号表示):
(1)上述实验②中得到沉淀X的质量为
(2)试样溶液中一定不存在的离子是
(3)为确定试样溶液中存在的阳离子,可采用的方法为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某学习小组进行“铁与水反应所得固体物质的成分、性质及再利用”的实验探究。
【探究一】设计下图所示装置进行“铁与水反应”的实验。

(1)反应前A中投放碎瓷片的目的是__________________ 。
(2)硬质玻璃管B中发生反应的化学方程式为_______________ 。
(3)装置E中的现象是__________________ 。
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
待硬质玻璃管B冷却后,取少许其中的固体物质溶于硫酸后,将所得溶液分成两份。
(4)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同)为_______ ;若溶液未变红色,推断硬质玻璃管B中固体物质的成分为_______ 。
①只有有Fe ②只有Fe3O4 ③Fe3O4和Fe ④一定有Fe3O4,可能有Fe
(5)若要检测溶液中是否存在Fe 2+,则另一份溶液中需要加入______ (填试剂)来检验。
【探究三】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(6)计算反应后B装置中铁元素的质量分数为_______ 。
【探究一】设计下图所示装置进行“铁与水反应”的实验。

(1)反应前A中投放碎瓷片的目的是
(2)硬质玻璃管B中发生反应的化学方程式为
(3)装置E中的现象是
【探究二】设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
待硬质玻璃管B冷却后,取少许其中的固体物质溶于硫酸后,将所得溶液分成两份。
(4)一份滴加几滴KSCN溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分(选填序号,下同)为
①只有有Fe ②只有Fe3O4 ③Fe3O4和Fe ④一定有Fe3O4,可能有Fe
(5)若要检测溶液中是否存在Fe 2+,则另一份溶液中需要加入
【探究三】设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(6)计算反应后B装置中铁元素的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】(CH3COO)2Mn·4H2O主要用于纺织染色催化剂和分析试剂,其制备过程如图。回答下列问题:
步骤一:以MnO2为原料制备MnSO4
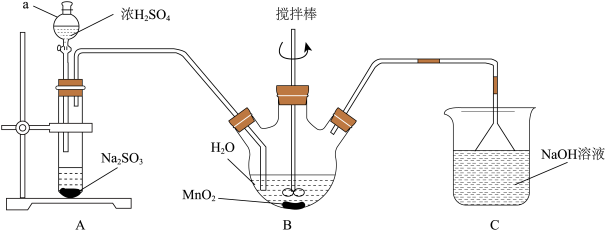
(1)仪器a的名称是___ ,C装置中NaOH溶液的作用是___________ 。
(2)B装置中发生反应的化学方程式是___________ 。
步骤二:制备MnCO3沉淀
充分反应后将B装置中的混合物过滤,向滤液中加入饱和NH4HCO3溶液,反应生成MnCO3沉淀。过滤,洗涤,干燥。
(3)①生成MnCO3的离子方程式_____________ 。
②判断沉淀已洗净的操作和现象是___________ 。
步骤三:制备(CH3COO)2Mn·4H2O固体
向11.5 g MnCO3固体中加入醋酸水溶液,反应一段时间后,过滤、洗涤,控制温度不超过55℃干燥,得(CH3COO)2Mn·4H2O固体。探究生成(CH3COO)2Mn·4H2O最佳实验条件的数据如下:
(4)产品干燥温度不宜超过55℃的原因可能是___________ 。
(5)上述实验探究了___________ 和___________ 对产品质量的影响,实验l中(CH3COO)2Mn·4H2O产率为___________ 。
步骤一:以MnO2为原料制备MnSO4

(1)仪器a的名称是
(2)B装置中发生反应的化学方程式是
步骤二:制备MnCO3沉淀
充分反应后将B装置中的混合物过滤,向滤液中加入饱和NH4HCO3溶液,反应生成MnCO3沉淀。过滤,洗涤,干燥。
(3)①生成MnCO3的离子方程式
②判断沉淀已洗净的操作和现象是
步骤三:制备(CH3COO)2Mn·4H2O固体
向11.5 g MnCO3固体中加入醋酸水溶液,反应一段时间后,过滤、洗涤,控制温度不超过55℃干燥,得(CH3COO)2Mn·4H2O固体。探究生成(CH3COO)2Mn·4H2O最佳实验条件的数据如下:
| 实验组别 | 醋酸质量分数 | 温度/℃ | 产品质量/g |
| 1 | 3% | 50 | 22.05 |
| 2 | 3% | 60 | 22.24 |
| 3 | 4% | 50 | 22.13 |
| 4 | 4$ | 60 | 23.27 |
(5)上述实验探究了
您最近一年使用:0次



