Fe2O3又称铁红,请根据要求完成下列问题.
(1)Fe2O3固体(红棕色)属于_____ (填纯净物或者混合物).将其加入适量盐酸,反应的化学方程式_____
(2)用上述所得溶液进行下列实验,取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式_____
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴FeCl3溶液,继续煮沸至出现_____ 色,即可制得Fe(OH)3胶体.
(4)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到_____ 烧杯的液体中产生了丁达尔效应.
(1)Fe2O3固体(红棕色)属于
(2)用上述所得溶液进行下列实验,取少量溶液置于试管中,滴入NaOH溶液,可观察到有红褐色沉淀产生,反应的离子方程式
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向烧杯中加入几滴FeCl3溶液,继续煮沸至出现
(4)另取一小烧杯也加入20mL蒸馏水,向烧杯中加入1mL FeCl3溶液,振荡摇匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到
14-15高一上·吉林长春·期中 查看更多[15]
(已下线)课时2 铁的重要化合物四川省广元市八二一中学2021-2022学年高一上学期期中考试化学试题河北省石家庄藁城新冀明中学2021-2022学年高一上学期第一次月考化学试题吉林省长春市第二十九中学2021-2022学年高一上学期第二学程考试化学(理)试题贵州省毕节市威宁第四中学2021-2022学年高一上学期第一次月考化学试题江苏省海安市南莫中学2021-2022学年高一上学期第一次月考备考金卷A卷化学试题湖南省湘阴县知源学校2020-2021学年高一上学期10月月考化学试题安徽安庆宿松县第二中学2019-2020学年高一11月月考化学试题云南省绥江县第三中学2019-2020学年高一上学期期末考试化学试题人教版高一化学必修1第二章《化学物质及其变化》测试卷人教版高中化学必修1第二章《化学物质及其变化》测试卷2安徽省滁州市定远县重点中学2018-2019学年高一上学期期末考试化学试题安徽省滁州市定远县育才学校2019-2020学年高一上学期期中考试(普通班)化学试题云南省玉溪市通海县第二中学2019-2020学年高一上学期12月月考化学试题(已下线)2014-2015学年吉林省长春外国语学校高一上学期期中化学试卷
更新时间:2020-01-12 09:03:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下图为一个五圆环,每个环中的物质依次为 、NaCl、
、NaCl、 、
、 、
、 ,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
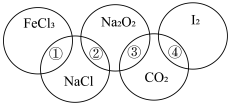
(1)关于上述相交部分的说法不正确的是______(填选项),
(2)上述五种物质中,有两种物质可以发生氧化还原反应,其化学方程式为____________ ;
(3)用洁净的烧杯取少量蒸馏水。用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol/L上图中某物质M的溶液,继续煮沸得到红褐色透明液体。
①物质M的化学式为______ ,向上述所得红褐色透明液体中加入电极通电后, 胶体粒子移向
胶体粒子移向______ 极;(填“阴极”或“阳极”)
②检验该红褐色透明液体是胶体的方法为__________________ ;
③往该红褐色透明液体中逐滴加入稀硫酸溶液至过量,现象是________________ ,此反应的离子反应方程式为____________
 、NaCl、
、NaCl、 、
、 、
、 ,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
(1)关于上述相交部分的说法不正确的是______(填选项),
| A.①表示盐类 | B.②表示钠的化合物 | C.③表示氧化物 | D.④表示单质 |
(3)用洁净的烧杯取少量蒸馏水。用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol/L上图中某物质M的溶液,继续煮沸得到红褐色透明液体。
①物质M的化学式为
 胶体粒子移向
胶体粒子移向②检验该红褐色透明液体是胶体的方法为
③往该红褐色透明液体中逐滴加入稀硫酸溶液至过量,现象是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高铁酸钾( ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
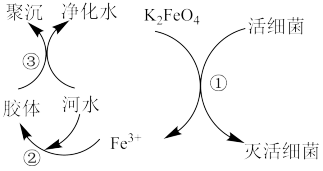
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 价。
(2)过程①中活性菌表现了_______ (填“氧化”或“还原”)性,该过程的还原产物是_______ (填离子符号);过程③属于_______ (填“物理”或“化学”)变化。
(3)根据上述原理分析,作水处理剂时, 的作用有
的作用有_______ (填两个)。
(4)制备高铁酸钾常用的反应原理为 (反应未配平)。
(反应未配平)。
①该反应中,Cl元素的化合价由_______ 价变为_______ 价;通过该反应说明:在碱性条件下,氧化性
_______ (填“>”、“=”或“<”) 。
。
②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:_______ ,将该反应改写为离子方程式:_______ 。
 ,极易溶于水)是常见的水处理剂,其原理如图所示。
,极易溶于水)是常见的水处理剂,其原理如图所示。
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
请回答下列问题:
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活性菌表现了
(3)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(4)制备高铁酸钾常用的反应原理为
 (反应未配平)。
(反应未配平)。①该反应中,Cl元素的化合价由

 。
。②配平该反应的化学方程式,并用双线桥法表示电子转移的方向和数目:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.回答下列问题:
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是_______ ,只有还原性的是_______ ,既有氧化性又有还原性的是_______ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O ②N2O4+H2O→HNO3+HNO2 ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是_______ (填序号)。
Ⅱ.根据胶体制备和性质完成以下问题
(3)某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加几滴饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。反应原理为FeCl3+3H2O=Fe(OH)3(胶体)+3HCl。
(a)判断胶体制备是否成功,可利用胶体的_______ 。
(b)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到_______ ,其原因是_______ 。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会_______ ,原因是_______ 。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会_______ ,原因是_______ 。
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O ②N2O4+H2O→HNO3+HNO2 ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是
Ⅱ.根据胶体制备和性质完成以下问题
(3)某化学兴趣小组的同学按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加几滴饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。反应原理为FeCl3+3H2O=Fe(OH)3(胶体)+3HCl。
(a)判断胶体制备是否成功,可利用胶体的
(b)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】以下12种物质为中学化学常见的物质。
①水银 ②NaCl ③NaHCO3 ④干冰 ⑤H2SO4 ⑥C2H5OH ⑦熔融的CaCO3 ⑧大理石⑨Cu(OH)2 ⑩Fe(OH)3胶体 ⑪ S ⑫氨水请按下列分类标准回答问题:
(1)属于非电解质的是________________ :(填序号,下同)能导电的是_____________ 。
(2)制备Fe(OH)3胶体的化学方程式为______________ ,当看到溶液呈________ 色时,则代表胶体已经制备完成。Fe(OH)3胶体中常混有FeCl3和HCl,将其装入半透膜袋,浸入蒸馏水中进行分离,该分离方法称为________ ;面粉厂静电除尘利用的原理是胶体的_____________ 。
(3)写出③NaHCO3在水溶液中的电离方程式_____________ ;将干冰升华过后的少量气体通入NaOH溶液中,试写出反应的离子方程式_________ 。
①水银 ②NaCl ③NaHCO3 ④干冰 ⑤H2SO4 ⑥C2H5OH ⑦熔融的CaCO3 ⑧大理石⑨Cu(OH)2 ⑩Fe(OH)3胶体 ⑪ S ⑫氨水请按下列分类标准回答问题:
(1)属于非电解质的是
(2)制备Fe(OH)3胶体的化学方程式为
(3)写出③NaHCO3在水溶液中的电离方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。回答下列问题。
(1)按照物质的分类方法,FeCl3应属于_________ (填序号)。
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为______________ ;判断胶体制备是否成功可利用胶体的____________ ;某同学在实验中没有使用蒸馏水,而是用自来水,结果生成了红褐色沉淀,原因是________________ 。
(3)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),青色来自蓝铜矿颜料(主要成分为Cu(OH)2·2CuCO3)。 其中孔雀石颜料属于_________ (填“纯净物”或"混合物”),请写出Cu(OH)2·CuCO3与盐酸反应的化学方程式________________ 。
(1)按照物质的分类方法,FeCl3应属于
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为
(3)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),青色来自蓝铜矿颜料(主要成分为Cu(OH)2·2CuCO3)。 其中孔雀石颜料属于
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】向一定量的Fe和Fe2O3的混合物中加入80mL 的盐酸溶液,使固体混合物恰好完全溶解,放出标准状况下的气体224mL,在溶液中加入KSCN溶液无血红色出现。请回答下列问题:
的盐酸溶液,使固体混合物恰好完全溶解,放出标准状况下的气体224mL,在溶液中加入KSCN溶液无血红色出现。请回答下列问题:
(1)请写出上述反应中所有属于氧化还原反应的化学方程式______ 。
(2)若忽略反应前后溶液体积变化,则最终所得溶液中溶质的物质的量浓度为______  。
。
(3)原固体混合物的总质量为______ g。
 的盐酸溶液,使固体混合物恰好完全溶解,放出标准状况下的气体224mL,在溶液中加入KSCN溶液无血红色出现。请回答下列问题:
的盐酸溶液,使固体混合物恰好完全溶解,放出标准状况下的气体224mL,在溶液中加入KSCN溶液无血红色出现。请回答下列问题:(1)请写出上述反应中所有属于氧化还原反应的化学方程式
(2)若忽略反应前后溶液体积变化,则最终所得溶液中溶质的物质的量浓度为
 。
。(3)原固体混合物的总质量为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学与环境密切相关.近年来雾霾问题已成为百姓所关注的主要问题,今年入秋以来,我国大部分地区更是“霾伏”四起,部分地区持续出现中度至重度霾,环境治理刻不容缓。回答下列问题:
(1)下列有关说法正确的是______________
(2)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
①工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是:____________ ;__________ (两个);不采用铜跟浓硫酸反应来制取硫酸铜的原因是________ (答两点)
②在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积____________ (填“大于”、“等于”或“小于”)180 mL。
③若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为__________
④将8 g Fe2O3投入到150 mL某浓度的稀硫酸中,再投入7 g铁粉,充分反应后,收集到1.68 L H2(标准状况),同时,Fe和Fe2O3均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗4 mol·L-1的NaOH溶液150 mL。则原硫酸的物质的量浓度为__________
(1)下列有关说法正确的是______________
| A.光化学烟雾是氮氧化物与碳氢化合物受紫外线作用后产生的有毒烟雾 |
| B.PH小于7的雨水都是酸雨 |
| C.PM2.5含量的增加是形成雾霾天气的重要原因之一 |
| D.大气中CO2含量的增加会导致臭氧空洞的加剧 |
①工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是:
②在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积
③若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
④将8 g Fe2O3投入到150 mL某浓度的稀硫酸中,再投入7 g铁粉,充分反应后,收集到1.68 L H2(标准状况),同时,Fe和Fe2O3均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗4 mol·L-1的NaOH溶液150 mL。则原硫酸的物质的量浓度为
您最近半年使用:0次



