某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出C、D、的化学式:C_______ ,D______ 。
(2)将含1 mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,请写出A与E反应的离子方程式:_______________ 。
(3)在A溶液中加入少量澄清石灰水,其离子方程式为_____________________ 。
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理______________________ 。
(5)若向含溶质0.5 mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为__________ g。
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 |    OH- OH- |
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出C、D、的化学式:C
(2)将含1 mol A的溶液与含l mol E的溶液反应后蒸干,仅得到一种化合物,请写出A与E反应的离子方程式:
(3)在A溶液中加入少量澄清石灰水,其离子方程式为
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理
(5)若向含溶质0.5 mol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为
更新时间:2017-02-23 18:39:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某溶液中只含有以下离子中的全部或部分: Ag+、Fe3+、Al3+、H+、SO42-、CO32-、OH-、Cl-,取该溶液做以下实验:
①观察溶液外观, 溶液有颜色;
②取少量该溶液加入Ba(NO3)2溶液, 无现象;
③取该溶液 100 mL,向其中逐滴滴加 1 mol/L的NaOH溶液至过量,生成沉淀物质的量与所加入的 NaOH 溶液的体积关系如图所示。根据实验回答以下问题:
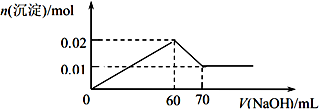
(1)检验溶液中阴离子的离子方程式为________________________________ 。
(2)根据以上实验推断,溶液中各离子的物质的量浓度分别为________________________________ 。
(3)若取以上溶液 100 mL,加入足量氨水后过滤,再将所得沉淀洗涤、灼烧,所得固体残留物的物质的量为_____________ mol。
①观察溶液外观, 溶液有颜色;
②取少量该溶液加入Ba(NO3)2溶液, 无现象;
③取该溶液 100 mL,向其中逐滴滴加 1 mol/L的NaOH溶液至过量,生成沉淀物质的量与所加入的 NaOH 溶液的体积关系如图所示。根据实验回答以下问题:

(1)检验溶液中阴离子的离子方程式为
(2)根据以上实验推断,溶液中各离子的物质的量浓度分别为
(3)若取以上溶液 100 mL,加入足量氨水后过滤,再将所得沉淀洗涤、灼烧,所得固体残留物的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D四种可溶性盐,它们的阳离子可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子可能是NO3-、SO42-、Cl-、CO32-的某一种。
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向⑴的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据⑴⑵实验事实可推断它们的化学式为:
⑴A、______ ;B、______ ;C、______ ;D、______ ;
⑵写出D与盐酸反应的离子方程式:_____________________________________ ;
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向⑴的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据⑴⑵实验事实可推断它们的化学式为:
⑴A、
⑵写出D与盐酸反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】无色溶液甲可能含有K+、Ca2+、NH 、Cu2+、NO
、Cu2+、NO 、Cl−、SO
、Cl−、SO 、CO
、CO 八种离子中的若干种。为确定甲溶液的组成,将其分成两等份,进行如下实验:
八种离子中的若干种。为确定甲溶液的组成,将其分成两等份,进行如下实验:
①向一份溶液中加入足量的NaOH浓溶液并加热,产生气体在标准状况下体积为4.48L。
②向另一份溶液中加入含有0.3molBaCl2的溶液,恰好可以与溶液中的离子完全反应,过滤得66.3g沉淀及滤液。
③向上述沉淀中加入过量的盐酸,得到沉淀X的质量为46.6g。
④向上述滤液中加入含有0.65mol的 AgNO3溶液,恰好可完全反应。据此,请回答下列问题(用相应的离子符号表示):
(l)上述实验③中得到沉淀X的物质的量为___________ mol;
(2)实验③过程中发生的反应,用离子方程式表示为___________ 。实验①过程中发生的反应,用离子方程式表示为 ___________ 。
(3)甲溶液中一定不存在的离子是______ ;可能存在的离子是 ________ 。
(4)甲溶液一定存在的离子中,物质的量最大的离子是_______ ;物质的量最小的离子是 ______ ,该离子的物质的量为 _______ mol。
 、Cu2+、NO
、Cu2+、NO 、Cl−、SO
、Cl−、SO 、CO
、CO 八种离子中的若干种。为确定甲溶液的组成,将其分成两等份,进行如下实验:
八种离子中的若干种。为确定甲溶液的组成,将其分成两等份,进行如下实验:①向一份溶液中加入足量的NaOH浓溶液并加热,产生气体在标准状况下体积为4.48L。
②向另一份溶液中加入含有0.3molBaCl2的溶液,恰好可以与溶液中的离子完全反应,过滤得66.3g沉淀及滤液。
③向上述沉淀中加入过量的盐酸,得到沉淀X的质量为46.6g。
④向上述滤液中加入含有0.65mol的 AgNO3溶液,恰好可完全反应。据此,请回答下列问题(用相应的离子符号表示):
(l)上述实验③中得到沉淀X的物质的量为
(2)实验③过程中发生的反应,用离子方程式表示为
(3)甲溶液中一定不存在的离子是
(4)甲溶液一定存在的离子中,物质的量最大的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。相互间能发生反应的是___________ 。(填序号)
(2)检验Na2O2其组成中所含阳离子的方法是___________ 。
(3)FeSO4·7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式简述其原因___________ 。
(4)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式___________ ,若生成6.72L气体(标准状况),则消耗铝的质量为___________ g。
(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。相互间能发生反应的是
(2)检验Na2O2其组成中所含阳离子的方法是
(3)FeSO4·7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式简述其原因
(4)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮是生命体重要的组成元素,自然界中氮的循环对生命活动有重要意义。
(1)汽车尾气主要含有 、CO、
、CO、 、
、 等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、
等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为______ 。
(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。______ ;丙为钠盐,其化学式为______ 。
②甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为______ 。实验室用该反应原理制取并收集一瓶干燥的甲气体,从下图中选择合适的装置,其连接顺序为______ 。(按从左到右的气流方向,用小写字母 和箭头表示)______ (填字母)。
A. B.
B. C.
C. D.
D.
④丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式______ 。
(1)汽车尾气主要含有
 、CO、
、CO、 、
、 等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、
等物质,这种尾气逐渐成为城市空气污染的主要来源之一。其中的CO、 ,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为
,在适宜条件下会转化为参与大气循环的两种无毒气体,该过程的化学反应方程式为(2)“价-类”二维图是学习元素化合物性质的重要方法,利用所学知识能更好地了解氮的循环。

②甲为常见的碱性气体,是制造氮肥、炸药等物质的化工原料。实验室制备甲的化学方程式为
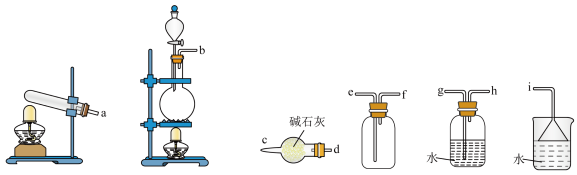
A.
 B.
B. C.
C. D.
D.
④丁主要用于染料、医药、印染、漂白等方面,且丁的焰色反应呈黄色。丁在酸性条件下,与KI按物质的量1:1恰好完全反应,生成能使淀粉变蓝的物质,写出该过程发生的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】生活离不开化学。家庭厨卫中有许多中学化学常见的物质,下列物质括号内为厨卫物品的主要成分:①食盐 ;②料酒(乙醇);③食醋(乙酸);④碱面
;②料酒(乙醇);③食醋(乙酸);④碱面 ;⑤发酵粉(
;⑤发酵粉( 和酒石酸);⑥“84”消毒液
和酒石酸);⑥“84”消毒液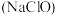 ;⑦洁厕灵
;⑦洁厕灵 。回答下列问题:
。回答下列问题:
(1)写出 在水中的电离方程式:
在水中的电离方程式:_______ 。
(2)当食盐不慎洒落在天然气的火焰上,观察到的现象是_______ 。
(3)②③的主要成分可以归为一类物质,其分类的依据是_______ (填标号)。
A.两种物质都是电解质
B.两种物质都是含碳化合物
C.两种物质都是氧化物
(4)⑥和⑦不能混合使用的原因是_______ (用离子方程式表示)。
(5)用面粉制作馒头的发酵过程中会产生有机酸(一种弱酸),导致口感变差,若在蒸馒头前加入适量④,可使蒸好的馒头松软可口无酸味,用化学方程式解释④的作用:_______ (设有机酸化学式为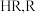 表示有机酸根)。
表示有机酸根)。
(6)欲用 固体配制
固体配制 质量分数为25%、密度为
质量分数为25%、密度为 的“84”消毒液。
的“84”消毒液。
①用电子天平(精确度为 )称量
)称量 的质量为
的质量为_______ g,若配制过程中发现液面超过了刻度线,处理方法为_______ 。
②该“84”消毒液的物质的量浓度约为_______  (保留小数点后一位)。
(保留小数点后一位)。
 ;②料酒(乙醇);③食醋(乙酸);④碱面
;②料酒(乙醇);③食醋(乙酸);④碱面 ;⑤发酵粉(
;⑤发酵粉( 和酒石酸);⑥“84”消毒液
和酒石酸);⑥“84”消毒液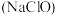 ;⑦洁厕灵
;⑦洁厕灵 。回答下列问题:
。回答下列问题:(1)写出
 在水中的电离方程式:
在水中的电离方程式:(2)当食盐不慎洒落在天然气的火焰上,观察到的现象是
(3)②③的主要成分可以归为一类物质,其分类的依据是
A.两种物质都是电解质
B.两种物质都是含碳化合物
C.两种物质都是氧化物
(4)⑥和⑦不能混合使用的原因是
(5)用面粉制作馒头的发酵过程中会产生有机酸(一种弱酸),导致口感变差,若在蒸馒头前加入适量④,可使蒸好的馒头松软可口无酸味,用化学方程式解释④的作用:
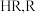 表示有机酸根)。
表示有机酸根)。(6)欲用
 固体配制
固体配制 质量分数为25%、密度为
质量分数为25%、密度为 的“84”消毒液。
的“84”消毒液。①用电子天平(精确度为
 )称量
)称量 的质量为
的质量为②该“84”消毒液的物质的量浓度约为
 (保留小数点后一位)。
(保留小数点后一位)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】将0.1molMg 、Al混合物溶于100mL3mol/LHCl中,再滴加1mol/LNaOH 溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V变化如图所示:
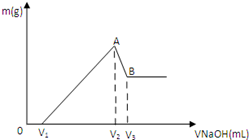
(1)写出A→B段反应的离子方程式__________________________________ 。
(2)A点沉淀的总物质的量n=________________________________ 。
(3)欲使Mg2+ 、Al3+刚好沉淀完全,则加入NaOH溶液的体积V2=_____ mL。
(4)若V1=60mL ,则混合物中Mg的物质的量n(Mg)=____________ ,V3点所加NaOH溶液的体积为V3=________ mL。

(1)写出A→B段反应的离子方程式
(2)A点沉淀的总物质的量n=
(3)欲使Mg2+ 、Al3+刚好沉淀完全,则加入NaOH溶液的体积V2=
(4)若V1=60mL ,则混合物中Mg的物质的量n(Mg)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】国际化学年的中国宣传口号是“化学-----我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
①若金属钠等活泼金属着火时,应该用________ 来灭火。
②经火焰灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)的元素是__________ 。
③使用漂白粉Ca(ClO)2漂白衣物原理的化学方程式是______________________ 。
④在自然界中,能实现氮的固定的化学方程式是____________________________ 。
⑤胃舒平(含有氢氧化铝)治疗胃酸(盐酸)过多的离子反应方程式:__________ 。
⑥过氧化钠在太空及潜水艇中作为供氧剂的两个化学方程式是________ 、________ 。
⑦明矾(KAl(SO4)2·12H2O)是具有净水作用的复盐,请你写出其在水中的电离方程式__ 。
①若金属钠等活泼金属着火时,应该用
②经火焰灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)的元素是
③使用漂白粉Ca(ClO)2漂白衣物原理的化学方程式是
④在自然界中,能实现氮的固定的化学方程式是
⑤胃舒平(含有氢氧化铝)治疗胃酸(盐酸)过多的离子反应方程式:
⑥过氧化钠在太空及潜水艇中作为供氧剂的两个化学方程式是
⑦明矾(KAl(SO4)2·12H2O)是具有净水作用的复盐,请你写出其在水中的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2010年上海世博会主题是“城市,让生活更美好”,试回答下列问题:
(1)为确保世博会期间申城空气质量优良率达到95%以上,世博会期间的空气质量状况监测中,不需要监测的指标是_____________ 。
a.可吸入颗粒物(PM10) b.NO2浓度 c.SO2浓度 d.CO2浓度;
(2)造成臭氧层空洞的主要物质是_______________ 。为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量。对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为__________ 。
(3)为2010年世博会期间提供科学有效的环境质量保障方案,白龙港污水处理厂升级改造,处理废水时加入K2SO4·Al2(SO4)3·24H2O或碱式氯化铝的作用是____________ ;通入臭氧或二氧化氯的作用是______________ 。某农村地区为获得饮用水,在将地表水取回家后,常使用漂白粉或漂白精片进行杀菌消毒,其原理可用化学方程式表示为_________________________ 。
(4)世博会中国馆——“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成。生产玻璃所用的工业设备是____________ ;石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是__________ 。
(1)为确保世博会期间申城空气质量优良率达到95%以上,世博会期间的空气质量状况监测中,不需要监测的指标是
a.可吸入颗粒物(PM10) b.NO2浓度 c.SO2浓度 d.CO2浓度;
(2)造成臭氧层空洞的主要物质是
(3)为2010年世博会期间提供科学有效的环境质量保障方案,白龙港污水处理厂升级改造,处理废水时加入K2SO4·Al2(SO4)3·24H2O或碱式氯化铝的作用是
(4)世博会中国馆——“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成。生产玻璃所用的工业设备是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列是五种物质的化学式,请按要求选择合适的序号填空:
A.NaHCO3 B.Na2CO3 C.Fe2O3 D.Ca(ClO)2 E. KAl(SO4)2·12H2O
(1)漂粉精的有效成分______ ;
(2)一种常见净水剂_________ ;
(3)常用于焙制糕点的小苏打___________ ;
(4)制普通玻璃的原料是石英、石灰石和______ 。
(5)常用做红色油漆和涂料的是__________
A.NaHCO3 B.Na2CO3 C.Fe2O3 D.Ca(ClO)2 E. KAl(SO4)2·12H2O
(1)漂粉精的有效成分
(2)一种常见净水剂
(3)常用于焙制糕点的小苏打
(4)制普通玻璃的原料是石英、石灰石和
(5)常用做红色油漆和涂料的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】把对应物质的字母代码填入括号内。
A水玻璃 B明矾 C浓硫酸 D硝酸铵 E新制氯水 F小苏打 G次氯酸钙
(1)漂白粉或漂粉精的有效成分_____
(2)常温下能使铝或铁钝化________
(3)能使紫色石蕊试液先变红后褪色______
(4)能做木材防火剂_________
(5)能做净水剂_________
(6)能做植物肥料___________
(7)能做处理胃酸过多的一种药剂_______
A水玻璃 B明矾 C浓硫酸 D硝酸铵 E新制氯水 F小苏打 G次氯酸钙
(1)漂白粉或漂粉精的有效成分
(2)常温下能使铝或铁钝化
(3)能使紫色石蕊试液先变红后褪色
(4)能做木材防火剂
(5)能做净水剂
(6)能做植物肥料
(7)能做处理胃酸过多的一种药剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请按要求完成下列各小题
(1)书写下列反应的离子方程式:
①向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀_____________________ 。
②过氧化钠溶于水中_________________________________________ 。
(2)已知反应:①Cl2+2KBr=2KCl+Br2 ②KClO3+6HCl=3Cl2+KCl+3H2O
③2KBrO3+Cl2 = Br2+2KClO3
A. Cl2 、KClO3 、KBrO3、 Br2的氧化性由强到弱的顺序为___________________ 。
B.反应②中还原剂与氧化剂的物质的量之比为__________ 。
C.③中若1mol Cl2参加反应,则氧化剂得电子的物质的量为________________ 。
(1)书写下列反应的离子方程式:
①向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀
②过氧化钠溶于水中
(2)已知反应:①Cl2+2KBr=2KCl+Br2 ②KClO3+6HCl=3Cl2+KCl+3H2O
③2KBrO3+Cl2 = Br2+2KClO3
A. Cl2 、KClO3 、KBrO3、 Br2的氧化性由强到弱的顺序为
B.反应②中还原剂与氧化剂的物质的量之比为
C.③中若1mol Cl2参加反应,则氧化剂得电子的物质的量为
您最近一年使用:0次



