①将质量分数为60%的稀硫酸与水等体积混合,混合后的质量分数为w;②将物质的量浓度为6mol/L的氨水加水等质量混合,混合后的物质的量浓度为C,则
| A.W<30% C>3 mol·L-1 | B.W<30% C<3 mol·L-11 |
| C.W>30% C>3 mol·L-1 | D.W>30% C<3 mol·L-1 |
更新时间:2020-03-28 20:08:16
|
【知识点】 物质的量浓度计算-溶液稀释的有关计算解读
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列说法中正确的是
| A.在一定温度和压强下,各种气态物质体积大小由分子间距离决定 |
| B.相同温度时,CO2和N2O若体积相同,则它们的质量一定相同 |
| C.100g浓度为18mol/L的浓硫酸中加入等质量的水稀释浓度大于9mol/L |
| D.14 mol/L的H2SO4溶液的溶质质量分数为80%,那么7 mol/L的H2SO4溶液的溶质质量分数将大于40% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】现有两种硫酸溶液,其中一种物质的量浓度为C1 mol/L、密度为ρ1 g/cm3,另一种物质的量浓度为C2 mol/L、密度为p2 g/cm3 ,当它们等体积混合后,溶液的密度为ρ3 g/cm3,则混合溶液的物质的量浓度为
A.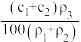 | B.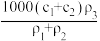 | C.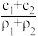 | D.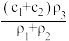 |
您最近一年使用:0次




