2016届浙江省义乌市稠州中学九年级上学期第一次月考科学试卷
浙江
九年级
阶段练习
2015-10-19
200次
整体难度:
适中
考查范围:
常见的物质、科学探究所需要的基本技能、物质的结构、物质的运动与相互作用
一、选择题 添加题型下试题
| A.食醋是一种酸 | B.食醋中含有氢离子 |
| C.食醋是一种混合物 | D.可以从酸中闻到酸味证明醋酸有挥发性 |
【知识点】 酸的化学性质
| A.偏低 | B.偏高 | C.不变 | D.无法判断 |
【知识点】 pH值的测量及方法
| A.Ag+和CO32— | B.Ag+或SO42— | C.SO42— | D.Ag+ |
【知识点】 物质的推断
A. | B. ; ; |
C. | D. |
【知识点】 常见实验操作
| A.KOH | B.Ca3(PO4)2 | C.K2CO3 | D.CO(NH2)2 |
【知识点】 盐与化肥

| A.氢氧化钠溶液和一氧化碳 |
| B.硫酸和氮气 |
| C.酒精和氧气 |
| D.氢氧化钠溶液和二氧化碳 |
| A.硫酸、火碱、纯碱、水 | B.醋酸、纯碱、火碱、干冰 |
| C.硝酸、苏打、碳酸钙、过氧化氢 | D.盐酸、苛性钠、生石灰、氧化镁 |
【知识点】 常见物质的分类 氧化物、酸、碱和盐的概念
| A.蓝色 | B.红色 | C.紫色 | D.无法判断 |
【知识点】 中和反应及其应用
| A.将铁片放入稀盐酸 | B.将铜片放入稀盐酸 |
| C.将铁片放入硝酸银溶液 | D.将铜片放入硝酸银溶液 |
【知识点】 金属活动性顺序及其应用
| A.取a克混合物溶于水通入足量二氧化碳反应,蒸发结晶,得b克固体 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物与足量稀硫酸充分反应,逸出气体直接通入碱石灰中,碱石灰增重b克 |
| D.取a克混合物溶于水与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |

| A.①和② | B.②和③ | C.①和③ | D.①②③ |
【知识点】 盐的性质及用途 置换反应及其应用 复分解反应及其应用 化合物之间的相互转化
| A.铁和铜 | B.铁和锌 | C.锌和铜 | D.铁和镁 |
【知识点】 金属的化学性质 根据化学反应方程式的计算

| A.图①是向一定量稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 |
| B.图②是用H2还原CuO来测定CuO中铜元素的含量 |
| C.图③是向饱和的NaCl溶液中不断加水 |
| D.图④是用适量的KClO3和MnO2混合物加热制O2 |

| A.图中Oa段表示生成的沉淀量 |
| B.c点表示碳酸钠恰好完全反应 |
| C.与50g废液恰好完全反应时消耗碳酸钠溶液的质量为30g |
| D.最终产生气体的质量为5g |
二、填空题 添加题型下试题
(1)由两种元素组成的一种燃料
(2)含氧元素质量分数最高的氧化物
(3)一种非金属单质
(4)一种含正三价元素的氧化物
【知识点】 化学式
A盐酸 B硫酸 C熟石灰 D硫酸铜 E纯碱 F食盐
请选择合适物质用化学式填空(物质不得重复使用)。
(1)用来清除铁锈的物质是
(2)改良酸性土壤结构的物质是
(3)在日常生活中用作调味剂的是
(4)存在于人的胃液中可帮助消化的物质是
(1)从上述叙述中找出镭的一点物理性质
(2)写出镭(Ra)与水反应的化学方程式
【知识点】 化学性质与物理性质的差别及应用 金属的物理性质及用途 金属的化学性质
三、解答题 添加题型下试题
(1)CaCl2溶液和NaHCO3,溶液反应生成CaCO3沉淀。为表示这个反应写出了下列两个反应方程式:
甲:CaCl2+NaHCO3=CaCO3+NaCl+HCl
乙:CaCl2+2NaHCO3=CaCO3↓+2NaCl+CO2↑+H2O
你认为哪一个反应的化学方程式不合理,并简述理由:
(2)某无色溶液中可能有Na+、Mg2+、Fe3+、Cl-、OH-、SO42-等离子中的一种或几种,经pH试纸测定,该溶液的pH为11。由此可知,该溶液中一定存在的阴离子有
【知识点】 盐的性质及用途 离子或物质的共存问题 常见离子的检验方法及现象
四、填空题 添加题型下试题
【知识点】 常见气体的检验与除杂方法 酸的化学性质
五、解答题 添加题型下试题
(1)在一个铜壶里发现了特殊的液体,闻起来有一股酒精味。为了检测这种液体是不是酒精,他提出了下面三种方法,你认为较哪种不科学?试选择其中的一种说明理由: 。
A.喝一口品尝 B.使用酒精测试仪测试 C.将其点燃
(2)区分纯铜和青铜的实验方法是 。
(3)小明发现从不同地点收集到的两个分别用纯铜和青铜制作的四喜娃娃中,青铜娃娃身上的锈斑比纯铜的多,他据此得出结论:青铜比纯铜更容易生锈。他的这种推理方法是否科学?说明理由: 。
六、填空题 添加题型下试题
步骤一:混合液中加入试剂A,过滤得到沉淀1和滤液1;
步骤二:滤液1中加入试剂B,过滤得到沉淀2和滤液2;
步骤三:滤液2中加入试剂C,过滤得到沉淀3和滤液3.
(1)同学们确认试剂A是NaCl溶液,写出步骤一中反应的化学方程式 。
(2)三种沉淀中,能溶于稀盐酸的是 。
(3)滤液3中,除NaNO3外还含有的盐是 。
【知识点】 初中科学综合库

(1)废液呈红色,说明废液显 性;
(2)写出废液中所含溶质的化学式 。
【知识点】 中和反应及其应用 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系
七、探究题 添加题型下试题
| 反应时间(秒) | 20 | 40 | 60 | 80 | 100 | 120 | 140 | |
| 收集到的气体体积(毫升) | 甲金属 | 25 | 60 | 95 | 130 | 160 | 170 | 170 |
| 乙金属 | 30 | 75 | 120 | 150 | 150 | 150 | 150 | |
(1)由实验结果可知:金属活动性较强的是
(2)为使得到的实验数据准确,小吴开始收集气体的时间点应该是
A.导管口一有气泡冒出时
B.冒出气泡连续且均匀时
C.检验产生的气体纯净时
(3)根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,还需知道
A.参加反应的硫酸质量
B.生成物中金属元素的化合价
【知识点】 金属活动性顺序及其应用 金属的化学性质
八、解答题 添加题型下试题

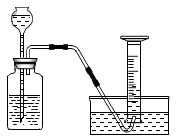
(1)打开A中的玻璃塞和活塞,C中反应的化学方程式为 。小聪认为通过B中的现象能说明二氧化碳与水反应生成了碳酸,你认为他的看法是否合理,并说明原因______ 。
(2)上述实验过程中,C中玻璃管K1的作用是_____ 。
【知识点】 实验室制取氧气的反应原理 二氧化碳的实验室制法 二氧化碳的化学性质
九、探究题 添加题型下试题
【提出问题】排污管道中的毒气有什么成分?
【查阅资料】
I.排污管道中的大部分有机物在一定条件下发酵会产生CO、CO2、H2S、CH4等。
II.H2S气体能与CuSO4溶液反应生成黑色沉淀。
【提出猜想】小组同学对排污管道气含有上述气体中最少3种成分的猜想如下:
猜想1:有CO、CO2、H2S;
猜想2:有CO、CO2、CH4;
猜想3:有CO、H2S、CH4;
猜想4:有CO2、H2S、;
猜想5:有CO、CO2、H2S、CH4。
【实验方案】小组同学共同设计了下图所示的装置并进行探究(夹持仪器已省略)。

【问题讨论】
(1)判断猜想2正确,最关键的观察对象是
(2)在验证猜想l的实验中,装置C中NaOH溶液的作用是
(3)要确证猜想5中是否有CH4,某同学认为图示装置有不足之处,需在装置C与D间加一个
【知识点】 常见气体的检验与除杂方法 二氧化碳的检验和验满 碱的化学性质

(1)取白色粉末A,向其中加入足量水,充分搅拌后过滤,得到白色沉淀B和无色滤液C。由此可判断,原白色粉末中一定不含有 。
(2)向白色沉淀B中加入足量稀盐酸,沉淀全部溶解,并产生无色气体。由此可判断,原白色粉末中一定含有 。
(3)向无色滤液C中通入一定量二氧化碳,充分反应后过滤,得到白色沉淀D和无色滤液E,由此可判断,原白色粉末中一定还含有 。
十、解答题 添加题型下试题
(1)废水中滴加紫色石蕊显
(2)80g氢氧化钠溶液中溶质的质量为
(3)废水中硫酸的质量分数为
【知识点】 碱的化学性质 根据化学反应方程式的计算
C2H6O + 3O2
 2CO2+3H2O
2CO2+3H2O (1)23g乙醇完全燃烧需消耗 克氧气。
乙醇不完全燃烧会产生二氧化碳和一氧化碳,某实验测得反应前后各物质的质量如下表:

①表中a的值为 。
②该实验发生反应的化学方程式为:4C2H5OH+11O2
 6CO2+12H2O+ CO。
6CO2+12H2O+ CO。
【知识点】 质量守恒定律及其应用 根据化学反应方程式的计算

(1)整个反应过程中,溶液中
(2)P点溶液中的溶质是
(3)M点溶液中的溶质质量分数是多少
【知识点】 盐的性质及用途 根据化学反应方程式的计算
十一、填空题 添加题型下试题
| 试验次数 | 氧化铜/g | 硫酸溶液/g | 硫酸铜/g |
| 1 | 2.0 | 120 | 4.0 |
| 2 | 4.0 | 120 | 8.0 |
| 3 | 6.0 | 120 | 9.6 |
| 4 | 8.0 | 200 | 16 |
| 5 | 10.0 | 200 | x |
根据实验结果填写下列空格:
(1)哪几次反应氧化铜有剩余?___________。
(2)表中x的值是_________。
(3)硫酸溶液中溶质的质量分数为________。
【知识点】 金属的化学性质
十二、探究题 添加题型下试题

①取研碎后的钙片4克,导入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量。
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量。
③整理相关数据如表所示,计算出钙片中碳酸钙的质量分数。
| 反应前总质量(克) | 275.58 |
| 反应后总质量(克) | 274.92 |
| 反应前后总质量差(克) | 0.66 |
| 容器内气体质量差(克) | m |
(1)该实验中,对装置中的固态干燥剂的性质有何要求?
(2)反应前容器内是空气(密度为ρ1),反应后全部是二氧化碳(密度为ρ2),则反应前后容器(容积为V)内的气体质量差为m为
(3)小明查阅有关数据后,计算出反应前后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数。
【知识点】 二氧化碳的实验室制法 根据化学反应方程式的计算
十三、解答题 添加题型下试题

【知识点】 金属的化学性质 影响化学反应速率的因素
试卷分析
试卷题型(共 33题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.65 | 酸的化学性质 | |
| 2 | 0.85 | pH值的测量及方法 | |
| 3 | 0.65 | 物质的推断 | |
| 4 | 0.65 | 常见实验操作 | |
| 5 | 0.94 | 盐与化肥 | |
| 6 | 0.65 | 酸的化学性质 碱的化学性质 | |
| 7 | 0.65 | 常见物质的分类 氧化物、酸、碱和盐的概念 | |
| 8 | 0.65 | 中和反应及其应用 | |
| 9 | 0.65 | 金属活动性顺序及其应用 | |
| 10 | 0.65 | 碱的化学性质 盐的性质及用途 | |
| 11 | 0.65 | 金属的化学性质 碱的化学性质 盐的性质及用途 | |
| 12 | 0.65 | 盐的性质及用途 置换反应及其应用 复分解反应及其应用 化合物之间的相互转化 | |
| 13 | 0.65 | 金属的化学性质 根据化学反应方程式的计算 | |
| 14 | 0.65 | 金属的化学性质 金属的冶炼 盐的性质及用途 | |
| 15 | 0.4 | 酸的化学性质 碱的化学性质 盐的性质及用途 | |
| 二、填空题 | |||
| 16 | 0.85 | 化学式 | |
| 17 | 0.85 | 碱的物理性质及用途 碱的化学性质 盐的性质及用途 | |
| 18 | 0.65 | 化学性质与物理性质的差别及应用 金属的物理性质及用途 金属的化学性质 | |
| 20 | 0.65 | 常见气体的检验与除杂方法 酸的化学性质 | |
| 22 | 0.64 | ||
| 23 | 0.85 | 中和反应及其应用 酸碱指示剂及其性质 溶液的酸碱性与pH值的关系 | |
| 31 | 0.4 | 金属的化学性质 | |
| 三、解答题 | |||
| 19 | 0.65 | 盐的性质及用途 离子或物质的共存问题 常见离子的检验方法及现象 | |
| 21 | 0.65 | 实验室的安全 金属的化学性质 | |
| 25 | 0.65 | 实验室制取氧气的反应原理 二氧化碳的实验室制法 二氧化碳的化学性质 | |
| 28 | 0.65 | 碱的化学性质 根据化学反应方程式的计算 | |
| 29 | 0.65 | 质量守恒定律及其应用 根据化学反应方程式的计算 | |
| 30 | 0.4 | 盐的性质及用途 根据化学反应方程式的计算 | |
| 33 | 0.65 | 金属的化学性质 影响化学反应速率的因素 | |
| 四、探究题 | |||
| 24 | 0.4 | 金属活动性顺序及其应用 金属的化学性质 | |
| 26 | 0.65 | 常见气体的检验与除杂方法 二氧化碳的检验和验满 碱的化学性质 | |
| 27 | 0.4 | 盐的性质及用途 常见物质的鉴定 | |
| 32 | 0.4 | 二氧化碳的实验室制法 根据化学反应方程式的计算 | |




