如图表示五种不同类别物质间的关系。A是铁锈的主要成分,C俗称苛性钠,请结合图示回答问题(图中“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质)。
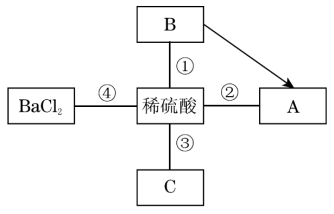
(1)B物质是__________ ;
(2)在①、②、③、④四个反应中,不能体现酸的化学通性的是________ (填序号)。

(1)B物质是
(2)在①、②、③、④四个反应中,不能体现酸的化学通性的是
更新时间:2020-05-07 13:56:48
|
相似题推荐
解答题
|
较难
(0.4)
【推荐1】小九同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取62.44 g该混合溶液于烧杯中,向烧杯中滴入溶质质量分数为13.8%的K2CO3溶液。滴入K2CO3溶液质量与生成沉淀质量的关系如图所示。求:

(1)所取盐酸和氯化钙混合溶液中HCl的质量;
(2)求恰好完全反应时,烧杯内所得溶液的溶质质量分数。

(1)所取盐酸和氯化钙混合溶液中HCl的质量;
(2)求恰好完全反应时,烧杯内所得溶液的溶质质量分数。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】亚氯酸盐在工业上有许多用途,常见的亚氯酸钠、亚氯酸镁、亚氯酸钡均易溶于水,亚氯酸盐在酸中不稳定,可生成Cl2、ClO2和H2O。用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠。
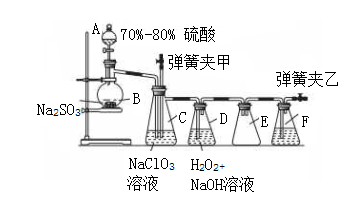
装置A中发生反应:Na2SO3+H2SO4=Na2SO4+H2O+SO2
装置C中发生反应:2 NaClO3+SO2=2ClO2+Na2SO4
装置D中发生反应:2ClO2+H2O2+2NaOH=2 NaClO2+2H2O+O2
(1)仪器组装完毕,关闭两个弹簧夹,打开A中活塞,向A中注入水可检验装置气密性,装置气密性良好的现象是__________ 。
(2)装置E的作用是________________ 。
(3)一次实验制备中,通过检验发现制备的 NaClO2中含有NaOH、Na2SO3,出现这些杂质的可能原因是____________________________________ 。

装置A中发生反应:Na2SO3+H2SO4=Na2SO4+H2O+SO2
装置C中发生反应:2 NaClO3+SO2=2ClO2+Na2SO4
装置D中发生反应:2ClO2+H2O2+2NaOH=2 NaClO2+2H2O+O2
(1)仪器组装完毕,关闭两个弹簧夹,打开A中活塞,向A中注入水可检验装置气密性,装置气密性良好的现象是
(2)装置E的作用是
(3)一次实验制备中,通过检验发现制备的 NaClO2中含有NaOH、Na2SO3,出现这些杂质的可能原因是
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】按要求写物质的化学式或反应的化学方程式:
(1)检验市场上销售的食盐中是否含有碘元素(元素符号为I) 的一种方法,是在酸性条件下,使食盐样品溶液跟一种试剂X反应(KIO3 +5X+6HCl═6KCl+3I2+3H2O)。这种试剂X是 ,要完成这种实验还需要的一种物质是 (填名称),它遇到 会变蓝。
(2)有一种浸液,其配方如下:NaOH 6g、NaCl 10g、Ca(OH)2 59g、茶叶5g、H2O 210mL,用该浸液浸泡鸭蛋可制无泥皮蛋。配制浸液时,是否可以用生石灰和纯碱代替NaOH和Ca(OH)2。请用化学方程式说明理由 ;
(3)调味用的食醋中含有醋酸(用HAc表示其组成),可以用来浸泡除去水垢(主要成分是碳酸钙和氢氧化镁),请写出有关反应的化学方程式 ;
(4)从含Cu2S的铜矿石中炼出铜的方法有多种:其中一种方法是:
①先将该矿石通空气高温煅烧,生成一种黑色固态氧化物和一种有刺激性气味的气态氧化物;
②将燃烧过的矿石上加适量的未经燃烧的铜矿石,混合均匀后隔绝空气再进行高温煅烧,结果得到金属铜和上述刺激性气味的气体。写出上述两步反应的化学方程式:
① ;② 。
(1)检验市场上销售的食盐中是否含有碘元素(元素符号为I) 的一种方法,是在酸性条件下,使食盐样品溶液跟一种试剂X反应(KIO3 +5X+6HCl═6KCl+3I2+3H2O)。这种试剂X是 ,要完成这种实验还需要的一种物质是 (填名称),它遇到 会变蓝。
(2)有一种浸液,其配方如下:NaOH 6g、NaCl 10g、Ca(OH)2 59g、茶叶5g、H2O 210mL,用该浸液浸泡鸭蛋可制无泥皮蛋。配制浸液时,是否可以用生石灰和纯碱代替NaOH和Ca(OH)2。请用化学方程式说明理由 ;
(3)调味用的食醋中含有醋酸(用HAc表示其组成),可以用来浸泡除去水垢(主要成分是碳酸钙和氢氧化镁),请写出有关反应的化学方程式 ;
(4)从含Cu2S的铜矿石中炼出铜的方法有多种:其中一种方法是:
①先将该矿石通空气高温煅烧,生成一种黑色固态氧化物和一种有刺激性气味的气态氧化物;
②将燃烧过的矿石上加适量的未经燃烧的铜矿石,混合均匀后隔绝空气再进行高温煅烧,结果得到金属铜和上述刺激性气味的气体。写出上述两步反应的化学方程式:
① ;② 。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】某科学兴趣小组在实验室发现一瓶敞口久置的氢氧化钠和一瓶未标浓度的稀盐酸,为测定氢氧化钠的变质情况和稀盐酸的浓度,他们取9.3g变质的氢氧化钠样品于锥形瓶中,加入50g水,充分溶解,再向锥形瓶中滴加未知浓度的稀盐酸,实验测得加入稀盐酸的质量与锥形瓶中物质的质量关系如图所示。

求:(1)生成的二氧化碳的质量________ 。
(2)9.3g样品中碳酸钠的质量是________ 。
(3)未知浓度的稀盐酸的溶质质量分数________ 。

求:(1)生成的二氧化碳的质量
(2)9.3g样品中碳酸钠的质量是
(3)未知浓度的稀盐酸的溶质质量分数
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如下图所示。试回答下列问题:

(1)完全反应后生成BaSO4沉淀____ 克。
(2)恰好完全反应时消耗Na2SO4溶液的质量是多少克?____
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?____ (写出计算步骤,计算结果精确到0.l%)

(1)完全反应后生成BaSO4沉淀
(2)恰好完全反应时消耗Na2SO4溶液的质量是多少克?
(3)恰好完全反应时所得溶液中溶质的质量分数是多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
真题
名校
【推荐3】兴趣小组的同学探究一瓶敞口放置的NaOH溶液(原质量分数为10%)是否变质,进行了下述实验:
(1)小江加入的“?”是 。
(2)小江认为小柯的实验和结论不正确,理由是 。
(3)小龙将沉淀过滤、洗涤、干燥,称量质量为1.97g。已知小龙所取的待测溶液质量为10g,请根据化学方程式计算,该待测溶液中变质生成物的质量分数。
| 同学 | 小柯 | 小江 | 小龙 |
| 操作 | 各取一支相同规格的试管,在试管中加入一定量的待测溶液 | ||
| 滴入无色酚酞 | 加入足量的 ? | 加入足量的BaCl2溶液 | |
| 现象 | 变红 | 产生气泡 | 产生白色沉淀 |
| 结论 | 没变质 | 变质 | 变质 |
(1)小江加入的“?”是 。
(2)小江认为小柯的实验和结论不正确,理由是 。
(3)小龙将沉淀过滤、洗涤、干燥,称量质量为1.97g。已知小龙所取的待测溶液质量为10g,请根据化学方程式计算,该待测溶液中变质生成物的质量分数。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】某化工厂有甲、乙两个车间,排出的污水澄清透明,经分析分别含有三种不同的离子,两厂废水中共有 Ba2+、K+、Cu2+、OH-、NO3-、CO32-六种离子
(1)甲车间的废水含有 3 种离子,明显呈碱性,则乙车间排放的污水中所含有的 3 种离子是________ (填离子符号)
(2)将甲、乙两车间的废水按适当的比例混合,可以变废为宝,既能使废水中的 Ba2+、Cu2+、OH-、CO32-等离子转化为沉淀除去,又可用上层清液来浇灌农田, 清液中含的溶质主要是________ (填化学式).
(1)甲车间的废水含有 3 种离子,明显呈碱性,则乙车间排放的污水中所含有的 3 种离子是
(2)将甲、乙两车间的废水按适当的比例混合,可以变废为宝,既能使废水中的 Ba2+、Cu2+、OH-、CO32-等离子转化为沉淀除去,又可用上层清液来浇灌农田, 清液中含的溶质主要是
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】A~G是初中所学的常见物质,其转化关系如图所示(部分反应物和生成物.反应条件已略去),A、B常温下为无色气体且组成元素相同,C 是大理石的主要成分,D为红色固体,E为黑色金属单质。请回答下列问题:
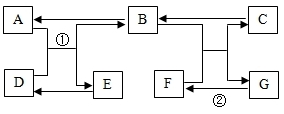
(1)B的化学式为__________________ ;
(2)反应②的基本反应类型是______________ 反应;
(3)写出反应①的化学方程式:____________________ 。

(1)B的化学式为
(2)反应②的基本反应类型是
(3)写出反应①的化学方程式:
您最近一年使用:0次




