小明利用稀硫酸与生锈的铁屑反应制取硫酸亚铁,实验流程如下:

资料:①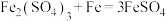 ;②硫酸亚铁容易被氧化为硫酸铁等物质。
;②硫酸亚铁容易被氧化为硫酸铁等物质。
(1)配制50克溶质质量分数为19.6%的稀硫酸,需溶质质量分数为98%的浓硫酸_______ 克。
(2)写出该实验中的一条化学方程式(除资料①中的反应外)。__________
(3)稀硫酸与生锈的铁屑充分反应后,要确保铁有少量剩余,其目的是_________ 。

资料:①
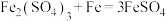 ;②硫酸亚铁容易被氧化为硫酸铁等物质。
;②硫酸亚铁容易被氧化为硫酸铁等物质。(1)配制50克溶质质量分数为19.6%的稀硫酸,需溶质质量分数为98%的浓硫酸
(2)写出该实验中的一条化学方程式(除资料①中的反应外)。
(3)稀硫酸与生锈的铁屑充分反应后,要确保铁有少量剩余,其目的是
2020·浙江·中考真题 查看更多[2]
更新时间:2020-07-05 07:18:15
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】下表是硫酸的密度和硫酸溶液中溶质的质量分数对照表(20℃)
实验室用溶质的质量分数为80%的浓硫酸配制200克溶质的质量分数为30%的稀硫酸。
(1)200克稀硫酸中含溶质_______ 克。
(2)需80%的浓硫酸_________ 毫升(保留一位小数)。
| 密度(克/厘米3) | 1.14 | 1.22 | 1.30 | 1.40 | 1.5O | 1.61 | 1.73 | 1.81 | 1.84 |
| 质量分数(%) | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 98 |
实验室用溶质的质量分数为80%的浓硫酸配制200克溶质的质量分数为30%的稀硫酸。
(1)200克稀硫酸中含溶质
(2)需80%的浓硫酸
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】小明测定一瓶稀盐酸的溶质质量分数,具体步骤如下:
步骤一:配制溶质质量分数为1%的氢氧化钠溶液
步骤二:向10克待测稀盐酸中逐渐滴入上述氢氧化钠溶液,并使用pH计记录溶液的pH变化情况,绘制图像如图。

(1)在步骤一中需要用到的玻璃仪器有____________ (写出两种)。
(2)请结合图,计算该稀盐酸的溶质质量分数为多少?(写出计算过程)____
(3)在往盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到2时,溶液中的溶质的__________________ 。(用化学式表示)
步骤一:配制溶质质量分数为1%的氢氧化钠溶液
步骤二:向10克待测稀盐酸中逐渐滴入上述氢氧化钠溶液,并使用pH计记录溶液的pH变化情况,绘制图像如图。

(1)在步骤一中需要用到的玻璃仪器有
(2)请结合图,计算该稀盐酸的溶质质量分数为多少?(写出计算过程)
(3)在往盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到2时,溶液中的溶质的
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】下表为硝酸钾和氯化钠在不同温度下的溶解度,请回答下列问题:
(1)若硝酸钾晶体中含少量的氯化钠晶体,可采用______ 的方法提纯硝酸钾。
(2)60℃时,将200克硝酸钾加入盛有100克水的烧杯中,充分搅棒后,形成溶液的质量为_____ 克。
(3)生产生活中,常常将一种物质的浓溶液加水稀释成稀溶液。要配制溶质质量分数为10%的硝酸钾溶液1000克,需要往溶质质量分数为20%的硝酸钾溶液中加__________ 克的水?
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 硝酸钾的溶解度/克 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| 氯化钠的溶解度/克 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(1)若硝酸钾晶体中含少量的氯化钠晶体,可采用
(2)60℃时,将200克硝酸钾加入盛有100克水的烧杯中,充分搅棒后,形成溶液的质量为
(3)生产生活中,常常将一种物质的浓溶液加水稀释成稀溶液。要配制溶质质量分数为10%的硝酸钾溶液1000克,需要往溶质质量分数为20%的硝酸钾溶液中加
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】铜镁合金具有优良的导电性,常用作飞机天等导电材料。科研小组欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金10克放入烧杯,将120克稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量,数据记录如下。请计算:
(1)合金中镁与铜的质量比为___________ 。
(2)第4次加入稀硫酸后,所得溶液中的含有的溶质是___________ 。
(3)所加稀硫酸溶质的质量分数___________ 。(写出计算过程)
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 30 | 30 | 30 | 30 |
| 剩余固体的质量/g | 9.1 | 8.2 | 7.3 | 6.5 |
(1)合金中镁与铜的质量比为
(2)第4次加入稀硫酸后,所得溶液中的含有的溶质是
(3)所加稀硫酸溶质的质量分数
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】下图甲是氢气和氧化铜反应的实验,下图乙是木炭和氧化铁反应的实验。
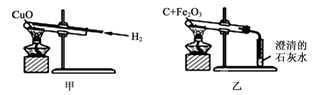
(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是 性。
(2)实验步骤的先后次序非常重要,比如甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生爆炸;反应结束后必须先 后 ,否则生成的红色的铜会变成黑色。
(3)某同学正确操作完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成 。
(4)该同学查阅资料,得到关于铁的氧化物如下信息:
根据以上信息,试写出乙实验大试管中反应的化学方程式: 。

(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是 性。
(2)实验步骤的先后次序非常重要,比如甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生爆炸;反应结束后必须先 后 ,否则生成的红色的铜会变成黑色。
(3)某同学正确操作完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成 。
(4)该同学查阅资料,得到关于铁的氧化物如下信息:
| 铁的氧化物化学式 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红色 | 黑色 | 黑色 |
| 化学性质 | 可溶于酸 | 常温下不可溶于酸 | 可溶于酸 |
根据以上信息,试写出乙实验大试管中反应的化学方程式: 。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】某科学兴趣小组同学取一定质量的铁粉,放到含少量硫酸的硫酸铜溶液中,完全反应后,最终得到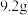 固体。为测定所得固体中各成分的含量,同学们将
固体。为测定所得固体中各成分的含量,同学们将 稀盐酸分五次加入到该固体中,得到数据如下表:
稀盐酸分五次加入到该固体中,得到数据如下表:
请分析计算:
(1)表中a的值是____________ 。
(2)稀盐酸的溶质质量分数是多少__________ ?(要有计算过程)
(3)与硫酸铜反应的铁的质量是多少_________ ?(要有计算过程)
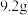 固体。为测定所得固体中各成分的含量,同学们将
固体。为测定所得固体中各成分的含量,同学们将 稀盐酸分五次加入到该固体中,得到数据如下表:
稀盐酸分五次加入到该固体中,得到数据如下表:次数 | 1 | 2 | 3 | 4 | 5 |
加入盐酸溶液质量/g | 12.5 | 12.5 | 12.5 | 12.5 | 12.5 |
剩余固体质量/g | 8.5 | 7.8 | a | 6.4 | 6.4 |
(1)表中a的值是
(2)稀盐酸的溶质质量分数是多少
(3)与硫酸铜反应的铁的质量是多少
您最近一年使用:0次
解答题
|
适中
(0.65)
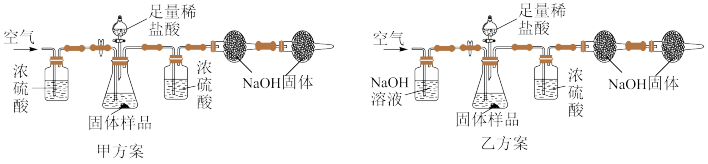
【推荐1】为测定某石灰石样品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶于水)。小嘉,小禾同学采用了不同的方案。
(1)小嘉的方法可用如下流程表示:______ 。
②计算稀盐酸的质量分数(计算结果保留0.1%),______
(2)小禾同学设计了甲、乙两种方案,(不考虑稀盐酸挥发)其中合理的是______ ,请说明理由______ 。
(1)小嘉的方法可用如下流程表示:

②计算稀盐酸的质量分数(计算结果保留0.1%),
(2)小禾同学设计了甲、乙两种方案,(不考虑稀盐酸挥发)其中合理的是
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】等质量的A、B两种物质分别与等质量的同浓度的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如图所示。请回答下列问题:

(1)若A、B为Mg、Zn中的一种,则A是________ 。
(2)若A、B为碳酸钠粉末和碳酸钙块状固体中的一种,B反应至a点时,所得溶液的溶质为________ (写化学式)。

(1)若A、B为Mg、Zn中的一种,则A是
(2)若A、B为碳酸钠粉末和碳酸钙块状固体中的一种,B反应至a点时,所得溶液的溶质为
您最近一年使用:0次
解答题
|
适中
(0.65)
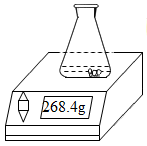
【推荐3】用久的热水瓶内胆有一层水垢[主要成分是CaCO3和Mg(OH)2],兴趣小组为了解具体成分进行了实验。他们取样品25克放入质量为100克的锥形瓶中,置于电子天平上,往瓶内加入150克稀盐酸时,恰好完全反应(样品中的杂质不与稀盐酸反应),此时天平示数如图为268.4克。对所得混合物进行过滤、洗涤、干燥、称量,得到固体4.2克。请回答下列问题:
(1)恰好完全反应时,溶液中的溶质为_______________ (填化学式)
(2)样品中CaCO3的质量分数是多少_______ ?
(3)反应结束时溶液中MgCl2的质量分数是多少_______ ?(精确到0.1%)
(1)恰好完全反应时,溶液中的溶质为
(2)样品中CaCO3的质量分数是多少
(3)反应结束时溶液中MgCl2的质量分数是多少

您最近一年使用:0次



