用化学方程式表示
(1)用含氢氧化镁的药物来治疗胃酸(含盐酸)过多________________
(2)用氢氧化钠中和石油中的硫酸________________
(3)硫酸厂排放的尾气中有二氧化硫,为避免大气污染,用氢氧化钠溶液来吸收二氧化硫,其化学方程式是_____________ 。
(1)用含氢氧化镁的药物来治疗胃酸(含盐酸)过多
(2)用氢氧化钠中和石油中的硫酸
(3)硫酸厂排放的尾气中有二氧化硫,为避免大气污染,用氢氧化钠溶液来吸收二氧化硫,其化学方程式是
更新时间:2018-10-19 19:08:37
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】氢氧化钠是一种重要的化工原料。工业上常用电解饱和食盐水的方法来制取烧碱,并生成氯气(Cl2)和氢气。
(1)请写出工业上用电解饱和食盐水制取烧碱的化学方程式:_____ 。
(2)氢氧化钠溶液中滴入酚酞试液会变红色,氢氧化钠溶液中主要含有Na+、OHˉ、水分子。某探究小组为探究氢氧化钠溶液中的哪种微粒能使酚酞试液变红,设计了如下实验方案,得出了初步结论。
①请填写下表中的实验结论:
②是否需要做“向水中滴加酚酞试液”的对比实验?为什么?_____
(3)某化学兴趣小组同学在实验室用氢氧化钠与稀盐酸做探究实验。将两种溶液混合后,对溶液中溶质的可能组成作出如下猜想:
甲同学的猜想是:溶液中只有NaCl。
乙同学的猜想是:溶液中可能含有NaCl、NaOH、和HCl。
①你认为甲乙两位同学的猜想都合理吗?并说明理由_____ 。
(4)有一瓶因保存不当而部分变质的氢氧化钠固体,为测其成分,称取10g样品配制成溶液,向其中滴加一定质量分数的稀盐酸,充分反应,共放出0.88g气体,试求样品中氢氧化钠的质量分数是多少?_____
(1)请写出工业上用电解饱和食盐水制取烧碱的化学方程式:
(2)氢氧化钠溶液中滴入酚酞试液会变红色,氢氧化钠溶液中主要含有Na+、OHˉ、水分子。某探究小组为探究氢氧化钠溶液中的哪种微粒能使酚酞试液变红,设计了如下实验方案,得出了初步结论。
①请填写下表中的实验结论:
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有少量NaCl溶液的试管中滴入酚酞试液,振荡 | 溶液无明显变化 |
②是否需要做“向水中滴加酚酞试液”的对比实验?为什么?
(3)某化学兴趣小组同学在实验室用氢氧化钠与稀盐酸做探究实验。将两种溶液混合后,对溶液中溶质的可能组成作出如下猜想:
甲同学的猜想是:溶液中只有NaCl。
乙同学的猜想是:溶液中可能含有NaCl、NaOH、和HCl。
①你认为甲乙两位同学的猜想都合理吗?并说明理由
(4)有一瓶因保存不当而部分变质的氢氧化钠固体,为测其成分,称取10g样品配制成溶液,向其中滴加一定质量分数的稀盐酸,充分反应,共放出0.88g气体,试求样品中氢氧化钠的质量分数是多少?
您最近一年使用:0次
解答题
|
适中
(0.65)
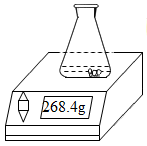
【推荐2】用久的热水瓶内胆有一层水垢[主要成分是CaCO3和Mg(OH)2],兴趣小组为了解具体成分进行了实验。他们取样品25克放入质量为100克的锥形瓶中,置于电子天平上,往瓶内加入150克稀盐酸时,恰好完全反应(样品中的杂质不与稀盐酸反应),此时天平示数如图为268.4克。对所得混合物进行过滤、洗涤、干燥、称量,得到固体4.2克。请回答下列问题:
(1)恰好完全反应时,溶液中的溶质为_______________ (填化学式)
(2)样品中CaCO3的质量分数是多少_______ ?
(3)反应结束时溶液中MgCl2的质量分数是多少_______ ?(精确到0.1%)
(1)恰好完全反应时,溶液中的溶质为
(2)样品中CaCO3的质量分数是多少
(3)反应结束时溶液中MgCl2的质量分数是多少

您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
(1)配制200g质量分数为8%的氢氧化钠溶液,需要水的体积为_________ mL。
(2)称量时:调节托盘天平平衡,将一个烧杯放在托盘天平的左盘,称量其质量。然后_________ (按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中
B.按需要添加砝码、移动游码。
(3)右图表示用上述配制的氢氧化钠溶液与20g某稀盐酸发生反应后溶液温度的变化情况。

①根据曲线判断,当加入氢氧化钠溶液的质量为____________ 时,反应恰好完全进行。
②当加入15 g氢氧化钠溶液时,所得溶液中的溶质为___________ (写化学式)。
(1)配制200g质量分数为8%的氢氧化钠溶液,需要水的体积为
(2)称量时:调节托盘天平平衡,将一个烧杯放在托盘天平的左盘,称量其质量。然后
A.将氢氧化钠固体加入烧杯中
B.按需要添加砝码、移动游码。
(3)右图表示用上述配制的氢氧化钠溶液与20g某稀盐酸发生反应后溶液温度的变化情况。

①根据曲线判断,当加入氢氧化钠溶液的质量为
②当加入15 g氢氧化钠溶液时,所得溶液中的溶质为
您最近一年使用:0次
解答题
|
适中
(0.65)
真题
【推荐1】食用碱的主要成分是 (含有少量
(含有少量 ),研究小组为测定市售食用碱中
),研究小组为测定市售食用碱中 的含量,设计了如图所示实验装置。
的含量,设计了如图所示实验装置。

取12克食用碱样品放入锥形瓶进行实验。按定量测定实验的正确步骤,进行规范操作,并用电子天平对某一装置进行连续称重,直至该装置质量不再改变时停止实验,此时该装置质量增加了4.4克。(假设每步吸收都完全, 装置中试剂均过量)
装置中试剂均过量)
回答下列问题:
(1)装置A的作用是________ ;
(2)根据某装置质量不再改变时,作为停止实验的依据,则该装置应该是_______ ;
(3)计算食用碱中 的质量分数。(要求根据化学方程式计算)
的质量分数。(要求根据化学方程式计算)_______
 (含有少量
(含有少量 ),研究小组为测定市售食用碱中
),研究小组为测定市售食用碱中 的含量,设计了如图所示实验装置。
的含量,设计了如图所示实验装置。
取12克食用碱样品放入锥形瓶进行实验。按定量测定实验的正确步骤,进行规范操作,并用电子天平对某一装置进行连续称重,直至该装置质量不再改变时停止实验,此时该装置质量增加了4.4克。(假设每步吸收都完全,
 装置中试剂均过量)
装置中试剂均过量)回答下列问题:
(1)装置A的作用是
(2)根据某装置质量不再改变时,作为停止实验的依据,则该装置应该是
(3)计算食用碱中
 的质量分数。(要求根据化学方程式计算)
的质量分数。(要求根据化学方程式计算)
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】牙膏中常用碳酸钙、二氧化硅等物质作为摩擦剂。某同学对牙膏中摩擦剂碳酸钙的含量进行探究。
【实验原理】测定C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。
【查阅资料】CO2+Ba(OH)2===BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生。
【实验装置】

根据探究过程回答下列问题:
(1)装置B中发生反应的化学方程式_____ ;
(2)实验过程中需持续缓缓通入空气,其作用有:①搅拌B、C中的反应物,使其充分反应;②____ ;
(3)从C中过滤出BaCO3沉淀所需的玻璃仪器有烧杯、____ 和玻璃棒;
(4)若没有A装置,直接通入空气,则测得CaCO3的质量分数______ (填“偏大”、“偏小”或“不变”)。
【实验原理】测定C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。
【查阅资料】CO2+Ba(OH)2===BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生。
【实验装置】

根据探究过程回答下列问题:
(1)装置B中发生反应的化学方程式
(2)实验过程中需持续缓缓通入空气,其作用有:①搅拌B、C中的反应物,使其充分反应;②
(3)从C中过滤出BaCO3沉淀所需的玻璃仪器有烧杯、
(4)若没有A装置,直接通入空气,则测得CaCO3的质量分数
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】已知:(1)向氯化铝溶液中滴加氢氧化钠溶液,有白色沉淀[Al(OH)3]生成。当继续滴加氢氧化钠溶液时,白色沉淀逐渐减少,直至消失,生成一种可溶性盐。此反应的化学方程式是:Al(OH)3+NaOH=NaAlO2(偏铝酸钠)+2H2O;(2)氢氧化铁固体不溶于氢氧化钠溶液.现欲除去氯化铁溶液中混有的少量氯化铝杂质,得到较为纯净的氯化铁溶液,某同学设计了如下提纯方案:

试回答:
(1)B溶液的名称是_________ ;
(2)滤液中的溶质有_________ 、_________ 、_________ 。(填化学式)

试回答:
(1)B溶液的名称是
(2)滤液中的溶质有
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】酸奶作为世界公认的长寿食品之一,正愈来愈受到人们的喜爱,酸奶中的酸味来自乳酸(化学式为C3H6O3)。
(1)青少年要多喝牛奶,因为牛奶中含有构成人体细胞的基本物质______ ;
(2)乳酸中C、H、O三种元素的质量比为______ ;
(3)乳酸在人体内消化吸收后,最终完全氧化为CO2和H2O,4.5g乳酸完全氧化,生成H2O多少克______ ?(乳酸氧化反应方程式:2C3H6O3+3O2==6CO2+6H2O)
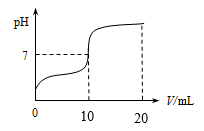
(4)为了测定某品牌酸奶中乳酸的含量,某同学取100mL酸奶和100mL蒸馏水于烧杯中,慢慢滴入0.2%的NaOH溶液并不断搅拌,用传感器测得溶液pH随加入NaOH体积V的变化关系如图所示。计算该酸奶中乳酸的含量为多少克每升______ (已知乳酸和氢氧化钠的反应方程式表示为:C3H6O3+NaOH==C3H5O3Na+H2O,测定所用NaOH溶液的密度为1.0g/mL)。
(1)青少年要多喝牛奶,因为牛奶中含有构成人体细胞的基本物质
(2)乳酸中C、H、O三种元素的质量比为
(3)乳酸在人体内消化吸收后,最终完全氧化为CO2和H2O,4.5g乳酸完全氧化,生成H2O多少克
(4)为了测定某品牌酸奶中乳酸的含量,某同学取100mL酸奶和100mL蒸馏水于烧杯中,慢慢滴入0.2%的NaOH溶液并不断搅拌,用传感器测得溶液pH随加入NaOH体积V的变化关系如图所示。计算该酸奶中乳酸的含量为多少克每升

您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】将m1g 7.3% HCl溶液和m2g未知浓度的NaOH溶液混合均匀,测量并记录溶液温度,实验结果如图所示(实验中始终保持m1+m2=50g)。

(1)做该实验时环境温度为_______ ℃左右。
(2)实验过程中溶液温度升高的原因是_______ 。
(3)图中A点所得溶液中的两种溶质是_______ 。
(4)通过计算确定NaOH溶液的溶质质量分数为多少?________

(1)做该实验时环境温度为
(2)实验过程中溶液温度升高的原因是
(3)图中A点所得溶液中的两种溶质是
(4)通过计算确定NaOH溶液的溶质质量分数为多少?
您最近一年使用:0次
解答题
|
适中
(0.65)
名校
【推荐3】小明在实验室发现一瓶未知浓度的氢氧化钠溶液,为方便以后使用,他对其浓度进行了测定.取20.0g此氢氧化钠溶液于烧杯中,逐滴滴加溶质质量分数为7.3%的稀盐酸,并随时对反应后的溶液用pH计(一种测定溶液pH的仪器)测定溶液的pH,所得数据如表:
试回答:
(1)当滴加稀盐酸的质量为9.8g时,溶液中的溶质是_____ ;当滴加稀盐酸的质量为10.0g时,溶液中的溶质是________ ;当滴加稀盐酸的质量为10.1g时,溶液中的溶质是________ 。
(2)计算所测氢氧化钠溶液中溶质的质量分数___ .
加入稀盐酸的质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
试回答:
(1)当滴加稀盐酸的质量为9.8g时,溶液中的溶质是
(2)计算所测氢氧化钠溶液中溶质的质量分数
您最近一年使用:0次



