为保护绿水青山,可将工业残留的钡渣(主要成分为碳酸钡)进行无害化处理,制取化工原料硫酸钡(BaSO4)。主要流程如下图,则:
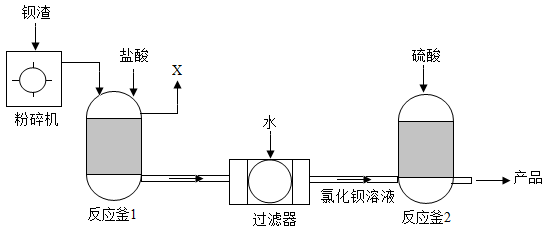
(1)粉碎钡渣的目的是_________________________________________________ 。
(2)反应釜1中的气体X的化学式为____________ 。
(3)反应釜2中发生复分解反应的化学方程式为__________________________________ 。

(1)粉碎钡渣的目的是
(2)反应釜1中的气体X的化学式为
(3)反应釜2中发生复分解反应的化学方程式为
更新时间:2018-11-11 00:40:18
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】医用氯化钙可用于生产补钙、抗过敏和消炎等药物.以工业碳酸钙(含有少量Al2(CO3)3、Fe2(CO3)3)为原料,经过溶解、除杂、过虑、蒸发结旵等过程,得到较纯的氯化钙晶体,其工艺如下图:

(1)两次加入的酸都是____ (填写酸的名称);其中第二次加入酸的目的是____ 。
(2)滤渣C中一定含有的成分是____ 。

(1)两次加入的酸都是
(2)滤渣C中一定含有的成分是
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】某样品为Cu和CuO的混合物,为测定样品中CuO的含量,甲、乙、丙、丁四位学生用同一种样品分别进行实验,测得的数据如下表:
分析实验数据,回答下列问题:
(1)求混合物中氧化铜的质量分数__________ ;
(2)求硫酸溶液中溶质的质量分数__________ 。
| 物质质量 学生 | 甲 | 乙 | 丙 | 丁 |
| 所取固体样品的质量(g) | 30 | 25 | 20 | 20 |
| 加入硫酸溶液的质量(g) | 100 | 100 | 100 | 120 |
| 反应后剩余固体的质量(g) | 22 | 17 | 12 | 12 |
分析实验数据,回答下列问题:
(1)求混合物中氧化铜的质量分数
(2)求硫酸溶液中溶质的质量分数
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】小明向氢氧化钠溶液中滴加了稀盐酸,发现没有明显现象。为了判断两者是否恰好完全反应,他取少量反应后的溶液加入试管中,滴加几滴无色酚酞试液,振荡后观察到酚酞试液不变色。
(1)根据上述现象,小明得出“两种物质恰好完全反应”的结论。小白认为小明的结论是不合理的,其理由是_______ 。
(2)小白利用pH试纸测反应后溶液的pH,以确定两者是否恰好完全反应。请你选用其它试剂再设计一个实验,以验证氢氧化钠和盐酸是否恰好完全反应(要求写出选用的试剂、可能观察到的现象和相应的结论)______ 。
(3)小白为了继续探究“在氢氧化钠与盐酸反应的过程中,溶液的pH是如何变化的”这一问题,进行如下实验:在一定量的氢氧化钠溶液中逐渐滴加盐酸,用pH试纸测定溶液的pH,记录数据如下表:下图中能合理表示该反应过程中pH变化的图像的是______ 。

(1)根据上述现象,小明得出“两种物质恰好完全反应”的结论。小白认为小明的结论是不合理的,其理由是
(2)小白利用pH试纸测反应后溶液的pH,以确定两者是否恰好完全反应。请你选用其它试剂再设计一个实验,以验证氢氧化钠和盐酸是否恰好完全反应(要求写出选用的试剂、可能观察到的现象和相应的结论)
(3)小白为了继续探究“在氢氧化钠与盐酸反应的过程中,溶液的pH是如何变化的”这一问题,进行如下实验:在一定量的氢氧化钠溶液中逐渐滴加盐酸,用pH试纸测定溶液的pH,记录数据如下表:下图中能合理表示该反应过程中pH变化的图像的是
| 盐酸的体积/mL | 0 | 10 | 19.5 | 20 | 20.5 | 30 | 40 |
| pH | 13 | 12 | 11 | 7 | 3 | 2 | 1 |

您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】兴趣小组考察了某工厂的废水处理工程。了解到该废水中只含有一种酸,为测定其所含酸的质量分数,取该废水200g于烧杯中,逐渐加入硝酸钡溶液,生成的沉淀质量与加入硝酸钡溶液的质量关系如图所示(假设该废水中的其他物质均溶于水且不与硝酸钡溶液反应)。

(1)加入硝酸钡溶液质量为___________时,沉淀刚好不再产生;
(2)计算废水中该酸的质量分数___________。

(1)加入硝酸钡溶液质量为___________时,沉淀刚好不再产生;
(2)计算废水中该酸的质量分数___________。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】牙膏常用碳酸钙、二氧化硅等物质作为摩擦剂,某同学对摩擦剂中碳酸钙的含量进行探究。实验原理:测定如图C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数。查阅资料:①CO2+Ba(OH)2═BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生;②饱和碳酸氢钠溶液可以吸收HCl气体3+HCl═NaCl+CO2↑+H2O;③CO2不会溶于饱和碳酸氢钠溶液。实验装置如图:
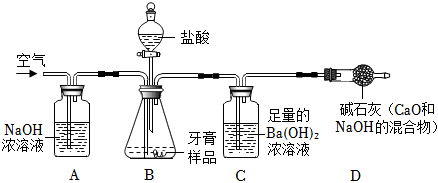
根据探究过程回答下列问题:
(1)实验过程中先后两次鼓入空气,其中第一次鼓入空气的目的是:____________ 。
(2)实验中准确称取2.00g样品三份,进行三次测定,测得BaCO3平均质量为1.97g,则样品中碳酸钙的质量分数为________ 。
(3)下列各项措施中,不能提高测定准确度的是_______ (填字母)。
A.滴加盐酸不宜过快
B.在B﹣C之间增添盛有饱和碳酸氢钠溶液的洗气装置
C.A﹣B之间增添盛有浓硫酸的洗气装置
D.在加入盐酸之前,应排尽装置内的气体
E.滤出的BaCO3沉淀应该洗涤、干燥后再称质量

根据探究过程回答下列问题:
(1)实验过程中先后两次鼓入空气,其中第一次鼓入空气的目的是:
(2)实验中准确称取2.00g样品三份,进行三次测定,测得BaCO3平均质量为1.97g,则样品中碳酸钙的质量分数为
(3)下列各项措施中,不能提高测定准确度的是
A.滴加盐酸不宜过快
B.在B﹣C之间增添盛有饱和碳酸氢钠溶液的洗气装置
C.A﹣B之间增添盛有浓硫酸的洗气装置
D.在加入盐酸之前,应排尽装置内的气体
E.滤出的BaCO3沉淀应该洗涤、干燥后再称质量
您最近一年使用:0次
解答题
|
适中
(0.65)
名校
【推荐3】在除杂质的操作中,为了将杂质完全去除,通常需加入过量的除杂试剂。为了除去 NaCl 样品中混有的少量 Na2SO4和 MgCl2,某校化学课外活动小组设计的提纯 NaCl的流程如图所示:

(1) 加入过量的氢氧化钠可除去的阳离子是_________ (写离子符号)。
(2) 试剂 X 的化学式为________ ,溶液 M 中所含有的阴离子有_________ 。
(3) 某同学用提纯得到的 NaCl晶体配制一定溶质质量分数的氯化钠溶液, 在量取液体时仰视读数, 会导致所配制溶液的溶质质量分数偏________ (填 “大”或 “小”)。

(1) 加入过量的氢氧化钠可除去的阳离子是
(2) 试剂 X 的化学式为
(3) 某同学用提纯得到的 NaCl晶体配制一定溶质质量分数的氯化钠溶液, 在量取液体时仰视读数, 会导致所配制溶液的溶质质量分数偏
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】请分析、比较以下几组化学反应,得出结论.
| 组别 | 化学方程式 | 结论 |
| Ⅰ | 6CO2+6H2O C6H12O6+6O2 C6H12O6+6O2CO2+H2O═H2CO3 | 反应物相同,生成物不同, 原因 |
| Ⅱ | Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O | 反应物相同,生成物不同, 原因 |
| Ⅲ | C+O2(充足) CO2 CO22C+O2(不充足)  2CO 2CO | 反应物相同,生成物不同, 原因 |
| Ⅳ | 2KClO3 2KCl+3O2↑(反应缓慢) 2KCl+3O2↑(反应缓慢)2KClO3  2KCl+3O2↑(反应迅速) 2KCl+3O2↑(反应迅速) | 反应物相同,反应速率不同, 原因 |
| 实践与应用 | 科学探究正努力实现对化学反应的控制,很多化学家致力于研究二氧化碳的“组合转化”技术,把过多二氧化碳转化为有益于人类的物质.若让二氧化碳和氢气在一定条件下反应,可生成一种重要的化工原料,反应的化学方程式如下: 2CO2+6H2  X+4H2O,推断X的化学式是 X+4H2O,推断X的化学式是 | |
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】现欲探究氧化铁能否加快过氧化氢的分解速率,并与二氧化锰的催化效果进行比较,甲、乙、丙三位同学同时进行过氧化氢的分解与气体的收集实验。实验时间均以30s为准(过氧化氢均未全部分解),其他可能影响实验的因素均已忽略。相关数据如下:
(1)甲同学认为乙同学收集到的气体有可能是氮气,乙同学马上从理论上推翻了甲同学的观点,为什么?_______________
(2)乙同学应该如何检验实验所生成的气体___________________ 。
(3)欲探究氧化铁在实验中是否起催化作用,首先应比较_______________ (填“a与b”、“b与c”或“a与c”)的大小,其次需补充做如下实验(无需写出具体操作):①__________________________________ ;②反应前后氧化铁的化学性质有没有改变。
| 同学序号 | 质量分数相同的过氧化氢溶液 | 溶液中加入的物质 | 收集到的气体体积 |
| 甲 | 100mL | 未加其他物质 | amL |
| 乙 | 100mL | 氧化铁0.5g | bmL |
| 丙 | 100mL | 二氧化锰0.5g | cmL |
(1)甲同学认为乙同学收集到的气体有可能是氮气,乙同学马上从理论上推翻了甲同学的观点,为什么?
(2)乙同学应该如何检验实验所生成的气体
(3)欲探究氧化铁在实验中是否起催化作用,首先应比较
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】某同学采用如图装置,用一些植物的器官来代替MnO2作催化剂,分解H2O2制取氧气,记录数据如下表。请依据以下信息分析:

(1)要使胡萝卜能够更快地促进过氧化氢的分解,可采用的方法是______________ 。
(2)当量筒内的水达到80毫升时,打开广口瓶的橡皮塞,立即将带火星的木条伸入瓶内,却发现木条不能复燃。请你解释木条不能复燃的原因是___________________ 。
(3)计算:34克15%的H2O2溶液中的溶质完全分解,能制得氧气的质量是多少______ ?
| 编号 | H2O2溶液的 质量(克) | H2O2溶液的 溶质质量分数 | 植物的器官及质量 | 收集气体的 体积(毫升) | 收集气体的 时间(分钟) |
| 1 | 34 | 15% | 大颗粒胡萝卜16克 | 80 | 18 |
| 2 | 34 | 15% | 大颗粒马铃薯16克 | 80 | 10.5 |
| 3 | 34 | 15% | 小颗粒马铃薯16克 | 80 | 4 |

(1)要使胡萝卜能够更快地促进过氧化氢的分解,可采用的方法是
(2)当量筒内的水达到80毫升时,打开广口瓶的橡皮塞,立即将带火星的木条伸入瓶内,却发现木条不能复燃。请你解释木条不能复燃的原因是
(3)计算:34克15%的H2O2溶液中的溶质完全分解,能制得氧气的质量是多少
您最近一年使用:0次



