暑假期间,宁波某学校的科学兴趣班参观了北仑的一家大型冶炼企业。大家了解到:黄铜渣中约含Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质,处理黄铜渣可得到产品之一——硫酸锌晶体(杂质不溶于水、不参与反应)。同学们又深入车间亲眼目睹了其主要生产流程,总结简化之后,如图所示。请完成以下实验记录:

(1)步骤Ⅰ、Ⅱ中的主要操作均为______________ 。
(2)整个实验过程中发生的化学反应,_______________ 置换反应(填“全部是”、“全不是”或“不全是”)。
(3)溶液B中溶质的质量,与溶液A中的溶质质量相比______________ (填“变大了”、“变小了”或“没有变化”)。

(1)步骤Ⅰ、Ⅱ中的主要操作均为
(2)整个实验过程中发生的化学反应,
(3)溶液B中溶质的质量,与溶液A中的溶质质量相比
更新时间:2018-11-11 00:40:18
|
相似题推荐
解答题
|
适中
(0.65)
【推荐1】现有溶质质量分数20%的硝酸钾溶液150g,将上述溶液平均分成三等分。
(1)往一份溶液中加入10g硝酸钾固体,固体全部溶解。求这时的溶质质量分数。________
(2)将另一份溶液恒温蒸发10g水,未析出晶体,则溶质质量分数变为多少?______________
(3)若要将第三份溶液的溶质质量分数变成30%,需要加入40%的硝酸钾溶液多少克?________________
(1)往一份溶液中加入10g硝酸钾固体,固体全部溶解。求这时的溶质质量分数。
(2)将另一份溶液恒温蒸发10g水,未析出晶体,则溶质质量分数变为多少?
(3)若要将第三份溶液的溶质质量分数变成30%,需要加入40%的硝酸钾溶液多少克?
您最近一年使用:0次
解答题
|
适中
(0.65)
真题
【推荐2】为研究“不同物质在敞口容器久置后的质量变化”,某科学兴趣小组将10.00克下列物质分别盛放于相同的烧杯中,将它们敞口放置在恒温实验室。一段时间后,测得烧杯中物质减小的质量情况见下表。
请回答:
(1)表格中“?”的值是________ 克;
(2)与原饱和硝酸钾溶液相比较,敞口放置24小时的硝酸钾溶液溶质质量分数________ (填“变大”、“变小”或“不变”);
(3)分析上表中水、饱和硝酸钾溶液和稀盐酸敞口放置后的质量减小程度随时间变化不一样,为进一步研究稀盐酸在敞口容器久置后的溶质质量分数变化,小丽进行了下列操作:取敞口放置时间48小时的稀盐酸5.00克于锥形瓶中,滴入两滴指示剂,用溶质质量分数为8%的氢氧化钠溶液逐滴滴入稀盐酸中,至恰好完全反应,共消耗了5.50克氢氧化钠溶液。通过计算,确定散口放置48小时的稀盐酸溶质质量分数是“变大”、“变小”还是“不变”?并对变化的原因作出解释。_______
| 放置时间(小时) | 烧杯中物质减小的质量(克) | |||
| 水 | 饱和氯化钠溶液 | 饱和硝酸钾溶液 | 7.3%的稀盐酸 | |
| 24 | 1.85 | 0.61 | 0.72 | 1.35 |
| 48 | 3.70 | ? | 1.44 | 2.80 |
请回答:
(1)表格中“?”的值是
(2)与原饱和硝酸钾溶液相比较,敞口放置24小时的硝酸钾溶液溶质质量分数
(3)分析上表中水、饱和硝酸钾溶液和稀盐酸敞口放置后的质量减小程度随时间变化不一样,为进一步研究稀盐酸在敞口容器久置后的溶质质量分数变化,小丽进行了下列操作:取敞口放置时间48小时的稀盐酸5.00克于锥形瓶中,滴入两滴指示剂,用溶质质量分数为8%的氢氧化钠溶液逐滴滴入稀盐酸中,至恰好完全反应,共消耗了5.50克氢氧化钠溶液。通过计算,确定散口放置48小时的稀盐酸溶质质量分数是“变大”、“变小”还是“不变”?并对变化的原因作出解释。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】如下甲、乙两图分别为粗盐提纯的一部分装置示意图和某自来水厂净水过程示意图,据图回答:

(1)甲图中的玻璃棒应该轻靠在________ 处;
(2)在将含有泥沙的粗盐提纯的整个过程中,用到玻璃棒多次。其中,第三次使用玻璃棒时的作用是________ ;
(3)图示自来水厂生产自来水时,没有使用的净水方法有_______ 。
A. 沉淀 B. 过滤
B. 过滤  C. 煮沸
C. 煮沸  D. 蒸馏 D.吸附
D. 蒸馏 D.吸附

(1)甲图中的玻璃棒应该轻靠在
(2)在将含有泥沙的粗盐提纯的整个过程中,用到玻璃棒多次。其中,第三次使用玻璃棒时的作用是
(3)图示自来水厂生产自来水时,没有使用的净水方法有
A. 沉淀
 B. 过滤
B. 过滤  C. 煮沸
C. 煮沸  D. 蒸馏 D.吸附
D. 蒸馏 D.吸附
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐2】建筑工地废弃的大理石边角料(主要成分为 ,杂质不参加反应)可用于制备轻质碳酸钙(常用作牙膏中的摩擦剂)。大理石边角料经高温灼烧后分解生成生石灰(主要成分为CaO),生石灰随后与水反应生成石灰乳(主要成分为
,杂质不参加反应)可用于制备轻质碳酸钙(常用作牙膏中的摩擦剂)。大理石边角料经高温灼烧后分解生成生石灰(主要成分为CaO),生石灰随后与水反应生成石灰乳(主要成分为 ),最后向石灰乳中通入
),最后向石灰乳中通入 即可得到轻质碳酸钙,工艺流程如下:
即可得到轻质碳酸钙,工艺流程如下:

(1)操作a的具体步骤包括______ 、洗涤、干燥。
(2)计算本实验中使用的大理石边角料样品中碳酸钙的质量分数。( )
 ,杂质不参加反应)可用于制备轻质碳酸钙(常用作牙膏中的摩擦剂)。大理石边角料经高温灼烧后分解生成生石灰(主要成分为CaO),生石灰随后与水反应生成石灰乳(主要成分为
,杂质不参加反应)可用于制备轻质碳酸钙(常用作牙膏中的摩擦剂)。大理石边角料经高温灼烧后分解生成生石灰(主要成分为CaO),生石灰随后与水反应生成石灰乳(主要成分为 ),最后向石灰乳中通入
),最后向石灰乳中通入 即可得到轻质碳酸钙,工艺流程如下:
即可得到轻质碳酸钙,工艺流程如下:
(1)操作a的具体步骤包括
(2)计算本实验中使用的大理石边角料样品中碳酸钙的质量分数。
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐3】氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:

(1)操作①中必须用到的一种仪器是________ (填序号)。
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是________ (填序号)。

(3)操作⑤中除用到三脚架、酒精灯、玻璃棒、坩埚钳外,还需要用到________ 等仪器。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外还可采取________ 等措施。
(4)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是
_________ (填序号)。
A.食盐没有全部溶解即过滤
B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿
D.器皿上沾有的精盐未全部转移到称量纸上

(1)操作①中必须用到的一种仪器是
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作④中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是

(3)操作⑤中除用到三脚架、酒精灯、玻璃棒、坩埚钳外,还需要用到
(4)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是
A.食盐没有全部溶解即过滤
B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿
D.器皿上沾有的精盐未全部转移到称量纸上
您最近一年使用:0次
解答题
|
适中
(0.65)
【推荐1】中安在线2011年2月15日报道,安徽滁洲正在以石英资源为基础,打造培育千亿元硅产业。石英主要成分为二氧化硅,它是玻璃工业和陶瓷工业的原料,冶金工业的助熔剂。
(1)二氧化硅的结构与金刚石相似,都是由 (填“分子”、“原子”、或“离子”)构成的,二氧化硅属于 (填“酸”、“碱”、“盐”或“氧化物”)。
(2)装有氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是在常温下,NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3和H2O。Na2SiO3使瓶口与瓶塞粘合在一起,则该反应的化学方程式为 。
(3)硅是太阳能电池和电脑芯片不可缺少的材料。生产高纯硅的流程示意图如下:
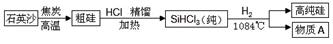
制备粗硅的反应为:SiO2+2C Si+2CO↑,反应的基本类型是 ,还原剂是 。
Si+2CO↑,反应的基本类型是 ,还原剂是 。
(1)二氧化硅的结构与金刚石相似,都是由 (填“分子”、“原子”、或“离子”)构成的,二氧化硅属于 (填“酸”、“碱”、“盐”或“氧化物”)。
(2)装有氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是在常温下,NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3和H2O。Na2SiO3使瓶口与瓶塞粘合在一起,则该反应的化学方程式为 。
(3)硅是太阳能电池和电脑芯片不可缺少的材料。生产高纯硅的流程示意图如下:

制备粗硅的反应为:SiO2+2C
 Si+2CO↑,反应的基本类型是 ,还原剂是 。
Si+2CO↑,反应的基本类型是 ,还原剂是 。
您最近一年使用:0次
解答题
|
适中
(0.65)
名校
【推荐2】A~J都是初中化学中的常见物质,其中D、E对维持自然界生命活动至关重要,A、B为黑色固体,C、G都是金属单质,I为无色气体.它们的相互转化关系如图所示:请回答:

(1)写出A的化学式_______ ;
(2)反应①②③④⑤中属于置换反应的为_______ (填序号);
(3)写出反应②的化学反应中Fe2O3为该反应的_______ 剂;
(4)写出反应⑤的化学方程式________ 。

(1)写出A的化学式
(2)反应①②③④⑤中属于置换反应的为
(3)写出反应②的化学反应中Fe2O3为该反应的
(4)写出反应⑤的化学方程式
您最近一年使用:0次

 ,该反应属于基本反应类型中的
,该反应属于基本反应类型中的 75%的铁矿石,最多可提炼出多少吨铁?(请写出计算过程)
75%的铁矿石,最多可提炼出多少吨铁?(请写出计算过程)

