将一定量的金属 (
( 是
是 、
、 、
、 、
、 中的一种)粉末放入
中的一种)粉末放入 和
和 的混合溶液中,充分反应后过滤,得到滤渣和无色滤液.向滤渣和滤液中分别滴加稀盐酸均无明显现象产生.
的混合溶液中,充分反应后过滤,得到滤渣和无色滤液.向滤渣和滤液中分别滴加稀盐酸均无明显现象产生.
( )金属
)金属 不可能是
不可能是__________
( )滤渣中一定含有的金属是
)滤渣中一定含有的金属是____________________ .
 (
( 是
是 、
、 、
、 、
、 中的一种)粉末放入
中的一种)粉末放入 和
和 的混合溶液中,充分反应后过滤,得到滤渣和无色滤液.向滤渣和滤液中分别滴加稀盐酸均无明显现象产生.
的混合溶液中,充分反应后过滤,得到滤渣和无色滤液.向滤渣和滤液中分别滴加稀盐酸均无明显现象产生.(
 )金属
)金属 不可能是
不可能是(
 )滤渣中一定含有的金属是
)滤渣中一定含有的金属是
更新时间:2019-07-07 14:09:18
|
相似题推荐
解答题
|
较难
(0.4)
【推荐1】小明为了测定某生锈的生铁铁片中铁元素的质量分数,设计并完成了如下实验

(1)小科同学认为装置甲存在缺陷,应该在右侧导管末端放一个燃着的酒精灯,目的是_____ 。
(2)装置乙试管中观察到的实验现象是_____ 。
(3)若室温下氢气的密度为ρg/L,生锈的生铁片中铁元素的质量分数是_____ (用字母表示)
(4)有人认为:“②中所得光亮的银白色铁片的质量,即为此生锈的生铁片中铁元素的质量没有必要进行③的操作”。请判断此观点是否正确,并说明理由:_____ 。
| 实验编号及装置 | 实验步骤 | 实验现象 |
| ①天平 | 称量生锈的生铁铁片的质量 | 质量为mg |
| ②装置甲 | 先通入一段时间CO,然后加热;完全反应后,停止加热;继续通CO至室温 | 表面的变成光亮的银白 |
| ③装置乙 | 将②中生成的光亮的银白色生铁铁片放入稀盐酸中,完全反应 | 试管中……;测得室温下产生气体的体积为VL |

(1)小科同学认为装置甲存在缺陷,应该在右侧导管末端放一个燃着的酒精灯,目的是
(2)装置乙试管中观察到的实验现象是
(3)若室温下氢气的密度为ρg/L,生锈的生铁片中铁元素的质量分数是
(4)有人认为:“②中所得光亮的银白色铁片的质量,即为此生锈的生铁片中铁元素的质量没有必要进行③的操作”。请判断此观点是否正确,并说明理由:
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】烧杯中盛放有一定量的硝酸银和硝酸亚铁的混合溶液,现向溶液中缓缓加入锌粉,经搅拌使其与溶液中的溶质恰好完全反应。现以加入锌粉的质量为横坐标,以烧杯中生成的固体质量为纵坐标, 甲、乙、丙三位同学分别作出了烧杯中的固体质量随加入的锌粉质量变化的大致关系图。其中 A 点表示锌粉与溶液中的溶质恰好完全反应时的质量。
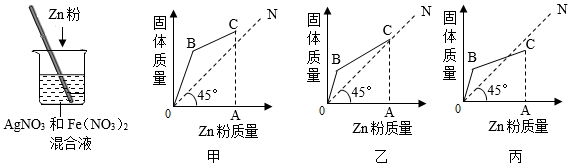
(1)三位同学所作的图中,你认为正确的有_______________________ 。
(2)请解释你认为正确的关系图中烧杯内固体质量变化形成的原因_______________________ 。

(1)三位同学所作的图中,你认为正确的有
(2)请解释你认为正确的关系图中烧杯内固体质量变化形成的原因
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】甲、乙、丙是初中常见物质,它们经一步反应的转化关系如右下图所示,其中部分反应物、生成物及反应条件已略去。

(1)若反应皆为化合反应,且均在点燃条件下发生,则丙的化学式为________ ,乙转化成丙的反应是________ (填“吸热”或“放热”)反应;
(2)若反应皆为置换反应,且均在溶液中进行,甲、乙、丙都为金属,则它们的金属活动性由强到弱的顺序是________ (用“甲”“乙”、“丙”表示);
(3)若反应皆为复分解反应,乙为白色难溶物。
①若甲为常见的酸,甲、乙、丙含相同的原子团,丙溶液为蓝色,则丙生成乙的化学方程式为________ (写出一个即可,下同);
②若甲为常见的碱,且相对分子质量为74,甲、乙、丙含相同的金属元素,则丙生成乙的化学方程式为________ 。

(1)若反应皆为化合反应,且均在点燃条件下发生,则丙的化学式为
(2)若反应皆为置换反应,且均在溶液中进行,甲、乙、丙都为金属,则它们的金属活动性由强到弱的顺序是
(3)若反应皆为复分解反应,乙为白色难溶物。
①若甲为常见的酸,甲、乙、丙含相同的原子团,丙溶液为蓝色,则丙生成乙的化学方程式为
②若甲为常见的碱,且相对分子质量为74,甲、乙、丙含相同的金属元素,则丙生成乙的化学方程式为
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】某科学兴趣小组开展综合实践活动。参观电镀工厂并对镀铜液中的相关成分进行检测。
(1)若要通过置换反应在某铁块表面镀上一层铜,可以选择Cu(NO3)2溶液和CuO中的___________ 。
(2)镀铜的液体是以稀硫酸、硫酸铜为原料按一定比例配制而成。兴趣小组同学用如下方法测定二者的比例:取镀铜液于烧杯中,取300克的NaOH溶液,平均分三次滴入烧杯中,将每次所得沉淀过滤、洗涤、烘干、称量。三次实验数据见下表:
①第2次实验生成9.80克沉淀的过程中,有多少NaOH溶质参加反应_________ ?
②请算出镀铜液中硫酸溶质与硫酸铜溶质的质量比________ 。
(1)若要通过置换反应在某铁块表面镀上一层铜,可以选择Cu(NO3)2溶液和CuO中的
(2)镀铜的液体是以稀硫酸、硫酸铜为原料按一定比例配制而成。兴趣小组同学用如下方法测定二者的比例:取镀铜液于烧杯中,取300克的NaOH溶液,平均分三次滴入烧杯中,将每次所得沉淀过滤、洗涤、烘干、称量。三次实验数据见下表:
| 实验序号 | NaOH溶液/g | 沉淀质量/g |
| 1 | 100 | 4.90 |
| 2 | 100 | 9.80 |
| 3 | 100 | 4.90 |
①第2次实验生成9.80克沉淀的过程中,有多少NaOH溶质参加反应
②请算出镀铜液中硫酸溶质与硫酸铜溶质的质量比
您最近一年使用:0次
解答题
|
较难
(0.4)
名校
【推荐2】如图所示,围棋棋盘上有五枚棋子,代表铁、稀盐酸、氢氧化钡、碳酸钙、硝酸银五种物质,相邻棋子间的连线表示物质间可以反应。已知与戊的反应中:甲−戊的反应类型不同于其它几个反应;丙−戊反应能产生一种气体,且该气体还能与丁反应生成沉淀。请将下表填写完整。______
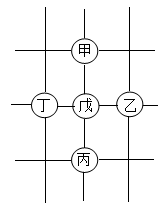
| 甲 | 乙 | 丙 | 丁 | 戊 |
| 碳酸钙 |

您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】将适量黄色的草酸亚铁(FeC2O4·2H2O)粉末加入试管,在酒精灯上边加热边摇动,发生剧烈反应,产生的气体可使燃着的木条熄灭,生成黑色粉末。反应将结束时,用橡皮塞塞好试管,稍冷后,打开塞子将所得的黑色粉末撒在石棉网上,便会立即自燃起来。试回答下列问题:
(1)黑色粉末是什么物质?为什么在空气中自燃:______ 。
(2)反应结束时,用橡皮塞塞好试管有何作用:________ 。
(3)化学反应的快慢与反应物的表面积有何关系?_____ 。
(4)写出草酸亚铁受热分解的化学方程式________ 。
(1)黑色粉末是什么物质?为什么在空气中自燃:
(2)反应结束时,用橡皮塞塞好试管有何作用:
(3)化学反应的快慢与反应物的表面积有何关系?
(4)写出草酸亚铁受热分解的化学方程式
您最近一年使用:0次



