向25g一定质量分数的Ba(OH) 2溶液中先后滴加质量分数为8%的CuSO4溶液和质量分数为9.8%的H2SO4溶液,绘制了滴加过程中加入溶液的质量与产生沉淀的质量关系如图所示。
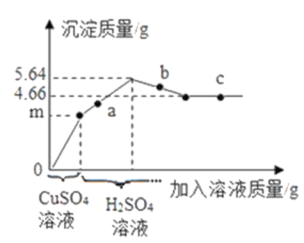
(1)a点对应溶液pH__ (选填“>”、“=”或“<”)7。
(2)取c点对应的溶液滴加NaOH溶液时观察到的现象是_______ 。
(3)通过计算确定m值。__________________
(4)原Ba(OH) 2溶液溶质的质量分数为多少?_____________

(1)a点对应溶液pH
(2)取c点对应的溶液滴加NaOH溶液时观察到的现象是
(3)通过计算确定m值。
(4)原Ba(OH) 2溶液溶质的质量分数为多少?
2019·浙江绍兴·模拟预测 查看更多[6]
2019年浙江省诸暨市六校九年级(下)联考科学试题九年级第一次月考计算专题(已下线)专题08 复分解反应计算-决胜2020年中考科学压轴题全揭秘浙江省台州市临海市第五中学2019年九年级上学期期中科学试题浙江省宁波市2020-2021学年九年级3月月考科学试题浙江省绍兴市2019年中考科学模拟试卷
更新时间:2020-09-29 17:18:00
|
相似题推荐
解答题
|
较难
(0.4)
【推荐1】小明同学想知道实验室用稀盐酸和石灰石制取CO2气体后的滤液中的溶质成分,故和小组成员一起进行了如下操作。取实验后的滤液100克,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:

(1)该滤液中的溶质是________ ,ab段的实验现象________ bc实验过程中出现的现象________ ;
(2)反应到c点时,所得溶液的溶质质量分数是多少?________ (写出计算过程,精确到0.1%)

(1)该滤液中的溶质是
(2)反应到c点时,所得溶液的溶质质量分数是多少?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】漂白粉是一种常用的消毒剂和漂白剂,可将氯气通入石灰乳中制得,其反应原理:
2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
某品牌漂白粉使用说明如图,试计算:

(1)2g漂白粉中含多少克次氯酸钙[Ca(ClO)2]___________
(2)若要制取200g的漂白粉,至少需要多少氯气?___________
2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O
某品牌漂白粉使用说明如图,试计算:

(1)2g漂白粉中含多少克次氯酸钙[Ca(ClO)2]
(2)若要制取200g的漂白粉,至少需要多少氯气?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】小科用如图装置来探究炼铁的反应原理,称取10g赤铁矿样品(主要成分为Fe2O3,杂质不含Fe元素且不与酸反应),铺开在硬质玻璃管中,充分加热至样品完全反应(化学方程式为: ),熄灭酒精喷灯,继续通入CO至硬质玻璃管冷却,将反应后的固体酸洗(除去反应生成的Fe)、干燥,称量剩余固体杂质的质量为2g。
),熄灭酒精喷灯,继续通入CO至硬质玻璃管冷却,将反应后的固体酸洗(除去反应生成的Fe)、干燥,称量剩余固体杂质的质量为2g。

(1)已知发生装置得到的CO气体中混有杂质CO2和H2O,则A装置的作用是______ 。
(2)从环保角度考虑,请写出一种尾气处理方法______ 。
(3)请计算样品中铁元素的质量。(写出计算过程)______
 ),熄灭酒精喷灯,继续通入CO至硬质玻璃管冷却,将反应后的固体酸洗(除去反应生成的Fe)、干燥,称量剩余固体杂质的质量为2g。
),熄灭酒精喷灯,继续通入CO至硬质玻璃管冷却,将反应后的固体酸洗(除去反应生成的Fe)、干燥,称量剩余固体杂质的质量为2g。
(1)已知发生装置得到的CO气体中混有杂质CO2和H2O,则A装置的作用是
(2)从环保角度考虑,请写出一种尾气处理方法
(3)请计算样品中铁元素的质量。(写出计算过程)
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】实验课上,陈佳同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液”,写出生成氢氧化钠的化学反应方程式_____ 。
(1)王凯同学说:“无色溶液中不一定含有氢氧化钠”,需要证明,他做了如下实验
刘阳同学认为王凯同学的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是:_____
(2)刘阳同学设计了另一个实验,请帮助他完成下列实验报告:
(1)王凯同学说:“无色溶液中不一定含有氢氧化钠”,需要证明,他做了如下实验
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有氢氧化钠 |
刘阳同学认为王凯同学的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是:
(2)刘阳同学设计了另一个实验,请帮助他完成下列实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| ②取少量样品于试管中,加入 ②过滤,向滤液中滴加几滴硫酸铜溶液 | ③ ④ | 无色溶液中确实含有氢氧化钠 |
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】某检测站对甲、乙两品牌奶粉进行检测,取甲品牌奶粉样品50克,通过一系列反应使奶粉中蛋白质中的氮元素完全转移到氨气中,用25克溶质质量分数为9.8%的稀硫酸恰好完全吸收,生成硫酸铵。计算并回答下列问题:
(1)50克甲品牌奶粉经过一系列反应产生氨气的质量是多少?_____________ (列式计算)
(2)100克乙品牌奶粉经过一系列反应产生氨气的质量是3.4克,而合格奶粉的国家标准是每100克中含蛋白质约为10g~25g,蛋白质中氮元素的平均质量分数为16%。请通过计算判断乙品牌奶粉是否属于合格奶粉?______________
(1)50克甲品牌奶粉经过一系列反应产生氨气的质量是多少?
(2)100克乙品牌奶粉经过一系列反应产生氨气的质量是3.4克,而合格奶粉的国家标准是每100克中含蛋白质约为10g~25g,蛋白质中氮元素的平均质量分数为16%。请通过计算判断乙品牌奶粉是否属于合格奶粉?
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】4.6克有机物在氧气中完全燃烧生成8.8克二氧化碳和5.4克水,求有机物的化学式。
____________________
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。市场上有一科常见的补铁药物“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色,化学式为C4H4FeO4)。
(1)速力菲药片是____ (选填 “纯净物”或“混合物" )。
(2)某孕妇为了预防缺铁性贫血,按照使用说明书上的用法和用量来服用,则一天孕妇通过药片补充铁元素多少毫克?______
(3)在琥珀酸亚铁片剂中Fe2+的含量为16.0%。该片剂中Fe2+在空气中易变质,国家规定该片剂中Fe2+变质超过10。0%即不能再服用。为检验某药店出售的琥珀酸亚铁片剂是否失效,取10.0g该片剂经测定含Fe2+1.52g。该片剂____ 服用(选填“能”或“不能”)。(Fe2+变质过程中引起片剂总质量的变化忽略不计。)
| 【通用名称】 | 活泼酸亚铁片 | 【商品名称】 | 速力菲 |
| 【成分】 | 每片含琥珀酸亚铁0。1克及其它辅料蔗糖等。 | ||
| 【适应症】 | 缺铁性贫血的预防及治疗。 | ||
【用法与用量】 | 口服 | ||
| 用于治疗:成人一日2~4片,儿童一日1~3片,分次服用。 | |||
| 用于预防:成人-日1片,孕妇一日2片,儿童一日0。5片。 | |||
(1)速力菲药片是
(2)某孕妇为了预防缺铁性贫血,按照使用说明书上的用法和用量来服用,则一天孕妇通过药片补充铁元素多少毫克?
(3)在琥珀酸亚铁片剂中Fe2+的含量为16.0%。该片剂中Fe2+在空气中易变质,国家规定该片剂中Fe2+变质超过10。0%即不能再服用。为检验某药店出售的琥珀酸亚铁片剂是否失效,取10.0g该片剂经测定含Fe2+1.52g。该片剂
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐1】听说墨鱼骨能治疗胃酸过多,好学的小科和小妍想探个究竟。查阅资料,墨鱼骨含碳酸钙80%~85%以上,还含有多种氨基酸。墨鱼骨能治疗胃酸过多的原因是:_________________ (用化学方程式表示)。为了测定墨鱼骨中碳酸钙的含量,他们先将墨鱼骨洗净晒干,并按各自设计实验方法进行研究。
(1)小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克。处理如下: CO2 质量 = 10克 - 5.4克 = 4.6克,设碳酸钙质量为M
CaCO3 ═ CO2↑ + CaO
100 44
M 4.6克
100/M=44/4.6克 所以M = 10.5克
CaCO3% =10.5克/10克×100%=105%
小科的计算结果与事实不符,产生错误的原因是:______ 。
(2)小研用如图所示的实验装置进行实验,其中浓硫酸的作用是______ 。
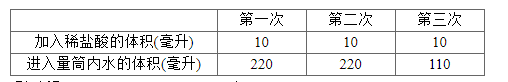
(3)小妍将30mL稀盐酸分3次加入到3克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不再变化时,读出水的体积,结果见下表。已知本实验条件下CO2 的密度为2.0克/升,求:该墨鱼骨粉样品中CaCO3的质量分数。
________ ,
(1)小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克。处理如下: CO2 质量 = 10克 - 5.4克 = 4.6克,设碳酸钙质量为M
CaCO3 ═ CO2↑ + CaO
100 44
M 4.6克
100/M=44/4.6克 所以M = 10.5克
CaCO3% =10.5克/10克×100%=105%
小科的计算结果与事实不符,产生错误的原因是:
(2)小研用如图所示的实验装置进行实验,其中浓硫酸的作用是
(3)小妍将30mL稀盐酸分3次加入到3克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不再变化时,读出水的体积,结果见下表。已知本实验条件下CO2 的密度为2.0克/升,求:该墨鱼骨粉样品中CaCO3的质量分数。

您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐2】大理石是含杂质的碳酸钙, 因具有美丽花纹而被广泛用于建筑物外墙、内壁的贴面和地面铺设。某同学想测出大理石样品中碳酸钙的含量, 进行了如下实验和分析。

(1)取一定量的大理石样品置于图甲的发生装置中,用分液漏斗向下滴加盐酸(方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑,杂质不参加反应) ,产生的二氧化碳气体用含有碱性物质的吸收装置充分吸收。分液漏斗中所加液体不选用硫酸,理由是________ 。
(2)反应前, 测得图甲中锥形瓶内物质的总质量和吸收装置的总质量都为 m 克。实验后, 根据实验数据绘制了图乙, 曲线 a 、b 分别表示锥形瓶内物质的总质量和吸收装置的总质量随反应时间变化的情况。请根据曲线 b 分析计算出大理石样品中碳酸钙的质量。____
(3)请综合分析曲线 a 、b , 计算出实验中所用盐酸的溶质质量分数。___

(1)取一定量的大理石样品置于图甲的发生装置中,用分液漏斗向下滴加盐酸(方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑,杂质不参加反应) ,产生的二氧化碳气体用含有碱性物质的吸收装置充分吸收。分液漏斗中所加液体不选用硫酸,理由是
(2)反应前, 测得图甲中锥形瓶内物质的总质量和吸收装置的总质量都为 m 克。实验后, 根据实验数据绘制了图乙, 曲线 a 、b 分别表示锥形瓶内物质的总质量和吸收装置的总质量随反应时间变化的情况。请根据曲线 b 分析计算出大理石样品中碳酸钙的质量。
(3)请综合分析曲线 a 、b , 计算出实验中所用盐酸的溶质质量分数。
您最近一年使用:0次
解答题
|
较难
(0.4)
【推荐3】工业纯碱中常含有少量的氯化钠。某学习小组对其组成展开探究。现取24g纯碱样品,加入100g水使其完全溶解,再加入96g过量的氯化钙溶液,完全反应后,过滤、洗涤、干燥得沉淀20g。完成下列问题:
(1)反应后溶液中含有的溶质是____________ 。(写化学式)。
(2)通过已知数据,能求出的量有_____ (写字母序号)。
A.反应后溶液的总质量
B.参加反应的氯化钙的质量
C.样品中碳酸钠的质量分数
D.氯化钙溶液中溶质的质量分数
(3)计算反应后溶液中氯化钠的质量分数。(写出计算过程,结果保留到0.1%)_____
(1)反应后溶液中含有的溶质是
(2)通过已知数据,能求出的量有
A.反应后溶液的总质量
B.参加反应的氯化钙的质量
C.样品中碳酸钠的质量分数
D.氯化钙溶液中溶质的质量分数
(3)计算反应后溶液中氯化钠的质量分数。(写出计算过程,结果保留到0.1%)
您最近一年使用:0次






