某化学实验小组制备硫酸亚铁铵晶体并设计实验测定其组成。请分析下列实验步骤,完成 以下小题。已知:铵盐能与强碱反应生成氨气,氨气能与酸反应生成铵盐。
I、向硫酸亚铁溶液中加入饱和硫酸铵溶液,经过“一系列操作”后得到一种浅绿色的硫酸亚铁铵晶体(俗名摩尔盐)。将摩尔盐低温烘干后保存待用
II、称取 7.84g 上述制的摩尔盐,加热至 1000℃ 失去结晶水,质量变为 5.68g
III、确认检查装置气密性良好后,将上述 5.68g 固体放入装置①的锥形瓶中,再用注射器向锥形瓶中加入足量氢氧化钠浓溶液,关闭止水夹 b,打开止水夹 a,鼓入空气,充分吸收产生的气体并测出气体质量为 0.68g
IV、向①中加入适量 3%过氧化氢溶液,使氢氧化亚铁全部转化为氢氧化铁,过滤、洗净、干燥、灼烧后测得其质量为 1.6g。
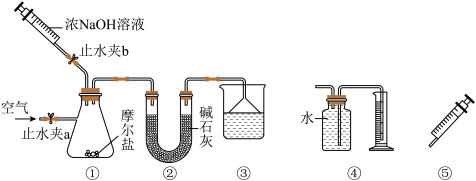
1.关于上述实验的叙述正确的是( )
| A.步骤 I 中没有发生化学变化 |
| B.拉动注射器活塞,③中漏斗内液面上升,说明装置气密性差 |
| C.③中可盛放硫酸,越浓越好 |
| D.步骤 III 中将鼓入空气的目的是使产生的气体全部进入③中 |
2.下列关于制得硫酸亚铁样品的分析正确的是( )
A.化学式是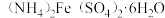 | B.化学式是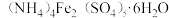 |
| C.该样品至少消耗氢氧化钠 3.6g | D.该样品中铵根含量约为 8.67% |
3.下列对于该实验的反思分析错误的是( )
| A.步骤 I 中烘干时必须保证低温烘干,否则测定的结晶水含量会偏低 |
| B.氢氧化钠必须确保足量,否则样品中含氮量可能会偏低 |
| C.用④代替③收集产生的气体,最终量筒内液体的体积并不是生成气体的体积 |
| D.用⑤代替③收集产生的气体,则 V(NH3)=V(⑤中针筒示数)-V(NaOH 溶液)-V(装置中原有气体) |