2022年江苏省南通市启东市中考二模化学试题
江苏
九年级
模拟预测
2022-05-31
390次
整体难度:
适中
考查范围:
化学与社会发展、物质构成的奥秘、身边的化学物质、化学实验、物质的化学变化
2022年江苏省南通市启东市中考二模化学试题
江苏
九年级
模拟预测
2022-05-31
390次
整体难度:
适中
考查范围:
化学与社会发展、物质构成的奥秘、身边的化学物质、化学实验、物质的化学变化
一、多选题 添加题型下试题
多选题
|
较易(0.85)
1. 人们一直高度关注“食品安全”。下列做法合理的是
| A.霉变大米蒸煮后食用 | B.食盐用于腌制食品 |
| C.用甲醛浸泡海产品 | D.用成分为聚乙烯的塑料包装食品 |
【知识点】 对人体健康危害的物质解读
您最近一年使用:0次
2020-04-19更新
|
79次组卷
|
4卷引用:2020年江苏省扬州高邮市中考一模化学试题
二、选择题 添加题型下试题
选择题-单选题
|
较易(0.85)
解题方法
3. 规范的实验操作是实验成功的保证。如图实验操作正确 的是
A.铁丝在氧气中燃烧 | B.检查装置气密性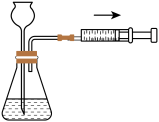 |
C.稀释浓硫酸 | D.检验溶液酸碱性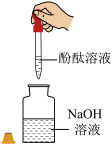 |
您最近一年使用:0次
2022-05-30更新
|
110次组卷
|
5卷引用:2022年江苏省南通市启东市中考二模化学试题
4. 下列说法不正确 的是
| A.只含一种元素的纯净物是单质 |
| B.适度调大燃气灶的进风口可使燃气充分燃烧 |
| C.溶液中有晶体析出时,溶质质量分数一定减小 |
| D.葡萄糖锌(C12H22O14Zn)口服液能为人体提供微量元素Zn |
您最近一年使用:0次
2021-05-25更新
|
98次组卷
|
4卷引用:2021年江苏省南通市中考二模化学试题
选择题-单选题
|
较易(0.85)
名校
解题方法
5. 下列物质的性质与用途不具有 对应性质的是
| A.食醋显酸性,可用于除去水壶中的水垢 |
| B.小苏打受热易分解,可用作油条膨松剂 |
| C.武德合金熔点低,可用于制作保险丝 |
| D.白磷具有易燃性,可用于制造安全火柴 |
您最近一年使用:0次
2022-05-30更新
|
95次组卷
|
3卷引用:2022年江苏省南通市启东市中考二模化学试题
选择题-单选题
|
较易(0.85)
名校
解题方法
6. 电解饱和氯化钠溶液的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑,下列说法中错误的是
2NaOH+H2↑+Cl2↑,下列说法中错误的是
 2NaOH+H2↑+Cl2↑,下列说法中错误的是
2NaOH+H2↑+Cl2↑,下列说法中错误的是| A.农业上常用NaOH改良酸性土壤 | B.保持氯气化学性质的最小粒子是氯分子 |
| C.反应后溶液中钠元素的质量分数变大 | D.电解水实验中不可用氯化钠增强水的导电性 |
您最近一年使用:0次
2022-05-30更新
|
138次组卷
|
4卷引用:2022年江苏省南通市启东市中考二模化学试题
选择题-单选题
|
适中(0.65)
解题方法
7. 2021年中科院航天催化材料实验室将甲烷转化为甲醇(CH3OH,常温下是液态)。实现了天然气的高效利用,反应过程如图所示。下列说法不正确 的是

| A.反应前后铁的质量和化学性质不变 |
| B.该过程中,CH4发生氧化反应 |
| C.反应中O2和CH3OH质量比为1:1 |
| D.生成CH3OH过程中,分子数目减少 |
您最近一年使用:0次
2022-05-30更新
|
153次组卷
|
6卷引用:2022年江苏省南通市启东市中考二模化学试题
选择题-单选题
|
适中(0.65)
名校
解题方法
8. 图一是A、B两种物质的溶解度曲线。t1℃时,将等质量的A和B分别加入盛有100g水的两只烧杯中,充分搅拌并恢复至原温度后,现象如图二所示。下列说法正确 的是


| A.蒸发一定量的水,两烧杯中都一定有固体析出 |
| B.烧杯甲中溶液溶质的质量分数小于烧杯乙中溶液溶质的质量分数 |
| C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体 |
| D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数一定相等(不考虑水的蒸发) |
您最近一年使用:0次
2021-05-25更新
|
315次组卷
|
6卷引用:2021年江苏省南通市中考二模化学试题
选择题-单选题
|
适中(0.65)
解题方法
9. 下列实验方案能 达到实验目的的是
| 选项 | 实验目的 | 操作 |
| A | 配制100g 6%的稀盐酸 | 量取5mL浓盐酸(密度1.2g/mL)溶于94g水中 |
| B | Na2SO4溶液中混有少量MgSO4 | 加入Ba(OH)2溶液至不再产生沉淀,过滤 |
| C | 分离KCl和BaCl2的混合溶液 | 加入过量的K2CO3溶液,过滤、洗涤, 再分别向滤渣和滤液中加入适量稀盐酸 |
| D | 鉴别羊毛和涤纶 | 取样,闻气味 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-30更新
|
108次组卷
|
3卷引用:2022年江苏省南通市启东市中考二模化学试题
选择题-单选题
|
适中(0.65)
名校
解题方法
10. 从微观上看,化学反应是微观粒子按一定的数目关系进行的。已知一定质量的甲与18g乙恰好完全反应生成丙和丁。反应中所有物质的分子数随反应过程的变化如图所示。

( 表示氧原子、
表示氧原子、 表示氢原子、
表示氢原子、 表示氮原子)。
表示氮原子)。
下列说法正确的是

(
 表示氧原子、
表示氧原子、 表示氢原子、
表示氢原子、 表示氮原子)。
表示氮原子)。下列说法正确的是
| A.反应前甲的质量为6.8g |
| B.乙的化学式为NO2 |
| C.t时刻甲、丙的质量相等 |
| D.该反应基本反应类型为置换反应 |
您最近一年使用:0次
2022-01-19更新
|
252次组卷
|
5卷引用:江苏省南通市海门区2021-2022学年九年级上学期期末化学试题
三、填空与简答 添加题型下试题
11. 宏观辨识与微观探析是重要的化学核心素养。

(1)①表中不同种元素最本质的区别是原子中______ 不同。
②铝离子的核外电子数为______ 。
③镁元素与氮元素(化合价与氨气中相同)形成化合物的化学式为______ 。
④氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻。其主要原因是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅(SiF4)气体和水,该反应的化学方程式为______ 。
(2)Zn和NaHSO4溶液反应的微观示意图如图。

该反应中实际参加反应的粒子______ (填粒子名称)。
(3)硫及其化合物的“化合价-物质类别”关系如图。

物质X的化学式为______ ,写出由物质Y和小苏打转化为Na2SO4的化学方程式为______ 。

(1)①表中不同种元素最本质的区别是原子中
②铝离子的核外电子数为
③镁元素与氮元素(化合价与氨气中相同)形成化合物的化学式为
④氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻。其主要原因是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅(SiF4)气体和水,该反应的化学方程式为
(2)Zn和NaHSO4溶液反应的微观示意图如图。

该反应中实际参加反应的粒子
(3)硫及其化合物的“化合价-物质类别”关系如图。

物质X的化学式为
您最近一年使用:0次
2022-05-30更新
|
86次组卷
|
3卷引用:2022年江苏省南通市启东市中考二模化学试题
填空与简答-流程题
|
适中(0.65)
解题方法
12. 化学兴趣小组的同学们利用废硫酸液制备K2SO4,设计的流程如图所示:
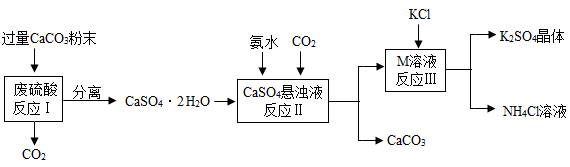
(1)写出反应I的化学方程式:_______ 。
(2)反应Ⅱ控制温度控制在40℃~60℃的原因_______ (填序号)。
a提高温度至40℃,增大反应速率 b增大CO2的溶解度 c温度不高于60℃,防止氨水分解
(3)反应Ⅱ生成了一种可用作氮肥的物质M,M的化学式为_______ 。
(4)上述流程中可循环使用的物质有CO2和_______ (填化学式)。
(5)反应Ⅲ中相关物质在25℃时的溶解度如表,反应Ⅲ在常温下(25℃)能实现的原因是_______ 。
(6)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是_______ 。

(1)写出反应I的化学方程式:
(2)反应Ⅱ控制温度控制在40℃~60℃的原因
a提高温度至40℃,增大反应速率 b增大CO2的溶解度 c温度不高于60℃,防止氨水分解
(3)反应Ⅱ生成了一种可用作氮肥的物质M,M的化学式为
(4)上述流程中可循环使用的物质有CO2和
(5)反应Ⅲ中相关物质在25℃时的溶解度如表,反应Ⅲ在常温下(25℃)能实现的原因是
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g | 34.0 | 11.1 | 37.2 | 19.5 |
您最近一年使用:0次
2021-05-25更新
|
199次组卷
|
5卷引用:2021年江苏省南通市中考二模化学试题
2021年江苏省南通市中考二模化学试题(已下线)2022江苏中考风向标-流程题2022年江苏省南通市启东市中考二模化学试题(已下线)化学-(南通专用)【试题猜想】2022年中考考前最后一卷2023年江苏省南通市崇川区中考二模联考化学试题
13. 化学是造福于人类的科学,请利用所学知识回答下列问题。
Ⅰ、化学与生活息息相关
(1)胃药中有一种氢氧化铝片用作抗酸药,可中和胃里过多的胃酸,其原理是______ (用化学方程式表示)。
(2)使用过氧乙酸消毒前要把200g 20%过氧乙酸稀释至0.5%,需要加水的质量为______ g。
Ⅱ、化学指导人类合理利用资源
(3)工业上用乙烯(C2H4)在一定条件下生产乙醇(C2H5OH),反应的示意图如图:
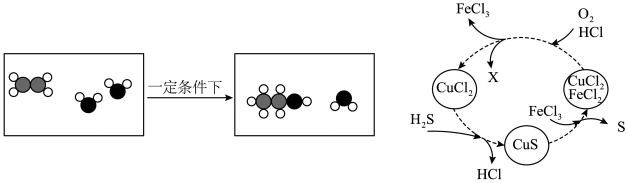
反应中乙烯与另一反应物的质量之比为______ ,乙醇又称酒精,可作燃料,若酒精灯内的酒精不小心洒出,在桌面燃烧起来,采用的灭火方法是______ 。
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可回收S,该转化过程中物质X的化学式为______ 。
Ⅲ、化学促进科学技术的发展
(5)中国自主研制的新一代战斗机,其中机翼前后缘采用了玻璃纤维增强塑料(玻璃钢),驾驶舱盖和挡风玻璃采用了丙烯酸酯透明塑料。其中玻璃纤维增强塑料属于______ (填字母)。
a.金属材料 b.合成材料 c.复合材料
(6)战机材料中还含有锌、铁、铜三种金属,为比较其活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的有______ (填序号)。
a.ZnCl2溶液中加入足量铜粉后,再加入铁粉
b.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
c.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
Ⅰ、化学与生活息息相关
(1)胃药中有一种氢氧化铝片用作抗酸药,可中和胃里过多的胃酸,其原理是
(2)使用过氧乙酸消毒前要把200g 20%过氧乙酸稀释至0.5%,需要加水的质量为
Ⅱ、化学指导人类合理利用资源
(3)工业上用乙烯(C2H4)在一定条件下生产乙醇(C2H5OH),反应的示意图如图:

反应中乙烯与另一反应物的质量之比为
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可回收S,该转化过程中物质X的化学式为
Ⅲ、化学促进科学技术的发展
(5)中国自主研制的新一代战斗机,其中机翼前后缘采用了玻璃纤维增强塑料(玻璃钢),驾驶舱盖和挡风玻璃采用了丙烯酸酯透明塑料。其中玻璃纤维增强塑料属于
a.金属材料 b.合成材料 c.复合材料
(6)战机材料中还含有锌、铁、铜三种金属,为比较其活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的有
a.ZnCl2溶液中加入足量铜粉后,再加入铁粉
b.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
c.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
您最近一年使用:0次
2022-05-30更新
|
126次组卷
|
3卷引用:2022年江苏省南通市启东市中考二模化学试题
四、科学探究题 添加题型下试题
科学探究题
|
较难(0.4)
名校
解题方法
14. 某化学兴趣小组对二氧化碳的制备和性质展开探究活动。
Ⅰ、二氧化碳的制备

(1)用图1所示实验装置制备CO2,写出仪器M的名称:______ ;
(2)若将长颈漏斗换为分液漏斗,其优点是______ 。
(3)写出用该装置制取CO2的化学方程式______ 。
(4)若用图2收集并测量生成的CO2的体积,植物油上方原有的空气对实验结果______ (填“有”或“无”)明显影响。
Ⅱ、某化学兴趣小组在一次实验活动中发现镁、钠都能在纯净的二氧化碳气体中燃烧,反应后冷却,瓶底除了有黑色颗粒,瓶壁上还都附着白色物质。经检验黑色颗粒是炭。他们对镁、钠在二氧化碳气体中燃烧后生成的白色物质分别进行了如下探究:
【探究问题一】镁在纯净的二氧化碳中燃烧生成的白色物质是什么?
同学们首先排除了是Mg(OH)2的可能性,理由是______ 。
【做出猜想】白色固体可能是①MgO、②MgCO3、③MgO和MgCO3的混合物。
【进行实验】取少量白色固体,加入足量的稀盐酸,观察到______ 现象,猜想①正确。
【探究问题二】钠在纯净的二氧化碳中燃烧生成的白色物质是什么?
【查阅资料】信息1:钠能与冷水发生剧烈反应; 信息2:Na2O+H2O=2NaOH。
【实验设计】甲组方案:
甲组结论:白色固体为Na2O和Na2CO3的混合物。
乙组方案:取5.3g白色固体样品进行下列操作:

(1)操作①是______ 。
(2)该组同学测得m=______ g,结合样品质量进行分析,最终得出结论:白色固体为Na2CO3。
【实验反思】(1)为何甲、乙两组所得结论不相符,某同学分析后指出甲组方案不科学,应该将甲组方案中的Ba(OH)2溶液改为______ 溶液才合理。
(2)乙组结论正确,钠在二氧化碳中燃烧的化学方程式为______ 。
(3)通过探究,你对燃烧或灭火有什么新的启示?______ (写一点)。
Ⅰ、二氧化碳的制备

(1)用图1所示实验装置制备CO2,写出仪器M的名称:
(2)若将长颈漏斗换为分液漏斗,其优点是
(3)写出用该装置制取CO2的化学方程式
(4)若用图2收集并测量生成的CO2的体积,植物油上方原有的空气对实验结果
Ⅱ、某化学兴趣小组在一次实验活动中发现镁、钠都能在纯净的二氧化碳气体中燃烧,反应后冷却,瓶底除了有黑色颗粒,瓶壁上还都附着白色物质。经检验黑色颗粒是炭。他们对镁、钠在二氧化碳气体中燃烧后生成的白色物质分别进行了如下探究:
【探究问题一】镁在纯净的二氧化碳中燃烧生成的白色物质是什么?
同学们首先排除了是Mg(OH)2的可能性,理由是
【做出猜想】白色固体可能是①MgO、②MgCO3、③MgO和MgCO3的混合物。
【进行实验】取少量白色固体,加入足量的稀盐酸,观察到
【探究问题二】钠在纯净的二氧化碳中燃烧生成的白色物质是什么?
【查阅资料】信息1:钠能与冷水发生剧烈反应; 信息2:Na2O+H2O=2NaOH。
【实验设计】甲组方案:
| 实验步骤 | 实验现象 | 结论 |
| 取少量白色物质于试管中,加水溶解,加入足量Ba(OH)2溶液 | 白色物质中有Na2CO3 | |
| 静置后,向上层清液中滴加酚酞试液 | 溶液变红 | 白色物质中有Na2O |
乙组方案:取5.3g白色固体样品进行下列操作:

(1)操作①是
(2)该组同学测得m=
【实验反思】(1)为何甲、乙两组所得结论不相符,某同学分析后指出甲组方案不科学,应该将甲组方案中的Ba(OH)2溶液改为
(2)乙组结论正确,钠在二氧化碳中燃烧的化学方程式为
(3)通过探究,你对燃烧或灭火有什么新的启示?
您最近一年使用:0次
2022-05-30更新
|
129次组卷
|
2卷引用:2022年江苏省南通市启东市中考二模化学试题
五、计算题 添加题型下试题
计算题
|
适中(0.65)
解题方法
15. 化石燃料的燃烧、硫酸的生产都产生二氧化硫,被雨水吸收后会形成酸雨,使农作物、建筑物等遭到破坏。环保部门为精确测定某硫酸厂周围空气中二氧化硫的含量,进行如下实验:
步骤1 取空气样品1000 m3缓缓通过足量氯水(化学方程式:SO2+Cl2+2H2O=2HCl+H2SO4),
步骤2 在所得溶液中加入过量的氯化钡溶液,产生的白色沉淀质量为2.33g。
(1)配制氯化钡溶液时,需用到的玻璃仪器有烧杯、量筒和______ ;
(2)上述实验中加入过量的氯化钡溶液的目的______ ;
(3)我国的环境空气质量标准中对空气中二氧化硫的最高浓度限值(单位体积的空气中所含二氧化硫的质量)如表所示,请通过计算说明此空气中二氧化硫的浓度级别。
步骤1 取空气样品1000 m3缓缓通过足量氯水(化学方程式:SO2+Cl2+2H2O=2HCl+H2SO4),
步骤2 在所得溶液中加入过量的氯化钡溶液,产生的白色沉淀质量为2.33g。
(1)配制氯化钡溶液时,需用到的玻璃仪器有烧杯、量筒和
(2)上述实验中加入过量的氯化钡溶液的目的
(3)我国的环境空气质量标准中对空气中二氧化硫的最高浓度限值(单位体积的空气中所含二氧化硫的质量)如表所示,请通过计算说明此空气中二氧化硫的浓度级别。
浓度限值(mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
您最近一年使用:0次
2022-05-30更新
|
80次组卷
|
2卷引用:2022年江苏省南通市启东市中考二模化学试题
试卷分析
整体难度:适中
考查范围:化学与社会发展、物质构成的奥秘、身边的化学物质、化学实验、物质的化学变化
试卷题型(共 15题)
题型
数量
多选题
1
选择题
9
填空与简答
3
科学探究题
1
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、多选题 | |||
| 1 | 0.85 | 对人体健康危害的物质 | |
| 二、选择题 | |||
| 2 | 0.85 | 碱的定义 氧化物的定义 人体内的常量元素 常见物品质材的辨别 | 单选题 |
| 3 | 0.85 | 铁在氧气中燃烧及其实验 浓硫酸的稀释 溶液酸碱性及pH相关关系 气密性检测 | 单选题 |
| 4 | 0.85 | 单质和化合物的判断 固体溶解度的影响因素 其他人体必需微量元素对人体的作用 燃料充分燃烧的方法及其重要性 | 单选题 |
| 5 | 0.85 | 金属的物理通性与用途 酸的通性 常见盐的俗名、用途 燃烧的定义及条件 | 单选题 |
| 6 | 0.85 | 有关质量守恒定律的计算 水的组成实验 几种常见碱的物理性质及用途 分子是保持物质化学性质的最小微粒 | 单选题 |
| 7 | 0.65 | 催化剂的概念、性质与用途 氧化反应概念及判断 化学方程式含义 根据化学方程式计算质量比 | 单选题 |
| 8 | 0.65 | 饱和溶液和不饱和溶液判断 固体溶解度的影响因素 溶解度的相关计算 | 单选题 |
| 9 | 0.65 | 配制一定溶质质量分数的计算 盐类参与的反应 羊毛、合成纤维、棉的鉴别 | 单选题 |
| 10 | 0.65 | 置换反应 用质量守恒定律确定物质组成 根据化学方程式计算质量比 | 单选题 |
| 三、填空与简答 | |||
| 11 | 0.65 | 离子中各类微粒间数值关系 元素的概念 化学式书写及读法 盐类参与的反应 | 填空题 |
| 12 | 0.65 | 复分解反应的实质与应用 酸的通性 盐类参与的反应 | 流程题 |
| 13 | 0.65 | 金属活动顺序理解和判断 有关溶液浓缩、稀释的计算 中和反应的实际应用 新型材料 | 填空题 |
| 四、科学探究题 | |||
| 14 | 0.4 | 化学方程式与实验的计算 制取二氧化碳的原理 盐类参与的反应 设计实验探究物质的成分 | |
| 五、计算题 | |||
| 15 | 0.65 | 含杂质的化学方程式计算 配制一定质量分数溶液的仪器 盐类参与的反应 | |



