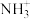2022年江苏省盐城市射阳县中考模考化学试题
江苏
九年级
二模
2022-07-03
106次
整体难度:
容易
考查范围:
身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验、物质的化学变化
2022年江苏省盐城市射阳县中考模考化学试题
江苏
九年级
二模
2022-07-03
106次
整体难度:
容易
考查范围:
身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验、物质的化学变化
一、选择题 添加题型下试题
选择题-单选题
|
较易(0.85)
解题方法
1. 下列做法不利于实现“碳中和”的是
| A.大力推行植树造林 | B.提倡使用节能产品 |
| C.提倡公民绿色出行 | D.化石燃料过度使用 |
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
解题方法
您最近一年使用:0次
选择题-选择题组
|
较易(0.85)
阅读下列材料,完成下列小题 。
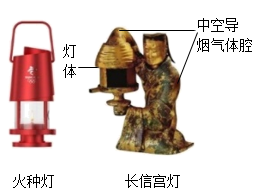
2022 年北京冬奥会火种灯其创意源自于青铜器精品“中华第一灯”——西汉长信宫灯。其灯体外部材料使用了再生铝合金,并首创双层玻璃结构。设计者在火种灯内外灯罩之间设计了一个导流通道, 既保证了灯具的进气量,又能够让火焰的高度适中,使燃料丙烷(C3H8)充分燃烧而不产生黑烟和异味,保持火种灯外观清洁、透亮,在低温、严寒、大风等环境下都不会熄灭。
3.下列说法正确的是
4.下列关于丙烷的说法中错误的是
5.下列关于燃烧说法错误的是
2022 年北京冬奥会火种灯其创意源自于青铜器精品“中华第一灯”——西汉长信宫灯。其灯体外部材料使用了再生铝合金,并首创双层玻璃结构。设计者在火种灯内外灯罩之间设计了一个导流通道, 既保证了灯具的进气量,又能够让火焰的高度适中,使燃料丙烷(C3H8)充分燃烧而不产生黑烟和异味,保持火种灯外观清洁、透亮,在低温、严寒、大风等环境下都不会熄灭。

3.下列说法正确的是
| A.铝是地壳中含量最多的金属元素 | B.人类使用金属铜晚于铝 |
| C.铝元素位于元素周期表第二周期 | D.铝较活泼不耐腐蚀 |
| A.丙烷属于有机物 | B.丙烷中含有 3 个碳原子和 8 个氧原子 |
| C.丙烷的相对分子质量为 44 | D.丙烷中碳元素和氢元素的质量比为 9:2 |
| A.燃烧属于化学变化 | B.火种灯导流通道的作用是提供充足的氧气 |
| C.所有的燃烧都能生成二氧化碳和水 | D.丙烷充分燃烧的产物与甲烷充分燃烧的产物相同 |
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
解题方法
6. 钪(Sc)是一种“工业的维生素”。如图为钪在元素周期表中的相关信息及其原子的结构示意图。下列说法正确的是
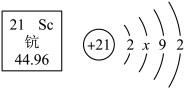

| A.钪属于非金属元素 | B.钪原子的中子数为 21 |
| C.钪原子核外有四个电子层 | D.原子结构示意图中,x=10 |
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
解题方法
8. 古籍《天工开物》有“煤饼烧石成灰”的记载。“烧石成灰”是指高温条件下碳酸钙转化为生石灰。下列说法正确的是
| A.石转化为灰的反应属于化合反应 | B.“灰遇水成浆”,“浆”的主要成分为氧化钙 |
| C.“灰遇水成浆”是吸热反应 | D.“浆”在空气中久置又会生成“石” |
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
解题方法
9. 下列有关实验说法正确的是
| A.向 AgNO3溶液中滴加 NaCl 溶液无明显现象 |
| B.CO 还原 Fe2O3,红色固体变为黑色 |
| C.将久置于空气中的铝片放入稀硫酸中,铝片表面立即产生大量气泡 |
| D.用广泛 pH 试纸测定某溶液酸碱度为 6.5 |
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
解题方法
10. 建构化学基本观念是学好化学的基础,以下观点对应的说法不正确的是
| A.元素观:水是由水元素组成的 |
| B.微粒观:保持液氢化学性质的最小粒子是氢分子 |
| C.变化观:铁和盐酸反应生成氯化亚铁和氢气 |
| D.守恒观:2g 氢气和 16g 氧气充分反应生成 18g 水 |
您最近一年使用:0次
选择题-单选题
|
较易(0.85)
解题方法
11. “宏观辨识与微观探析”是化学学科的核心素养之一。下列关于宏观和微观间联系的叙述错误的是
| A.分离液态空气制氧气,说明分子可以再分 |
| B.切洋葱时可闻到刺激性气味,说明分子在不断运动 |
| C.6000L氧气可以压缩进40L的钢瓶中,说明加压可使分子间的间隔变小 |
| D.酸碱中和反应都生成水,其实质是H+与OH-结合生成了H2O |
您最近一年使用:0次
2022-03-17更新
|
84次组卷
|
3卷引用:2022年河南省信阳市中考一模化学试题
12. 下列各组物质同时加到水中,最终得到无色透明溶液的是
| A.CuSO4、HCl、KCl | B.FeCl3、KOH、NaCl |
| C.Na2CO3、BaCl2、NaOH | D.Na2SO4、HCl、KNO3 |
您最近一年使用:0次
2022-07-03更新
|
213次组卷
|
2卷引用:2022年江苏省盐城市射阳县中考模考化学试题
选择题-单选题
|
适中(0.65)
解题方法
13. 如图是甲和乙两种物质的溶解度曲线。下列说法正确的是
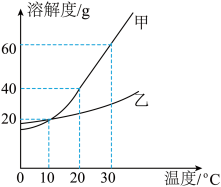

| A.10℃时,甲与乙的饱和溶液中溶质质量相等 |
| B.20℃时,甲饱和溶液的溶质质量分数为 40% |
| C.甲的饱和溶液中含有少量乙,可通过降温结晶的方法提纯甲 |
| D.将甲、乙的两种饱和溶液分别由 30℃降温至 20℃,析出甲的质量一定比析出乙的质量大 |
您最近一年使用:0次
2022-06-30更新
|
48次组卷
|
3卷引用:2022年江苏省盐城市射阳县中考模考化学试题
选择题-单选题
|
较难(0.4)
解题方法
14. 下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 检验二氧化碳气体 | 用燃着的木条伸入集气瓶内,观察火焰是否熄灭 |
| B | 除去二氧化碳中混有的一氧化碳 | 点燃 |
| C | 分离CaCl2、NaCl溶液 | 加适量Na2CO3溶液,过滤、洗涤,再向滤渣中滴加适量稀盐酸 |
| D | 鉴别CO(NH2)2和KCl固体 | 加入熟石灰研磨,闻气味 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
选择题-单选题
|
较难(0.4)
解题方法
15. 将 16g CuO 粉末加入到 200g 一定质量分数的稀 H2SO4溶液中,微热到 CuO 完全溶解,再向溶液中加入 Wg 铁粉,使溶液中的溶质完全反应后过滤,将滤渣在低温下烘干,干燥后固体质量仍然为Wg。下列分析不正确的是
| A.W≥12.8 | B.滤渣一定为混合物 |
| C.滤液的溶质为 FeSO4 | D.所用稀 H2SO4溶质的质量分数为 11.2% |
您最近一年使用:0次
二、填空与简答 添加题型下试题
16. Ⅰ.化学帮助我们认识身边的物质。
现有:①氧化钙 ②氢氧化钠 ③硝酸铵 ④甲烷 ⑤硝酸钾 ⑥纯碱,选择适当物质的序号填空。
(1)溶于水温度降低的盐____________ ;
(2)广泛用于生产玻璃、造纸、纺织生产的盐___________ ;
(3)常用作食品干燥剂____________ ;
(4)可用作炉具清洁剂的碱____________ ;
(5)一种由三种元素组成的复合肥料____________ ;
(6)最简单的有机物____________ 。
Ⅱ.化学与生活息息相关,请运用化学知识回答以下问题。
(7)市场上出售的净水器利用____________ 来吸附水中的颜色和异味;
(8)洗涤剂去油污利用的是其____________ 作用;
(9)坏血病是因为缺乏____________ 所致;
(10)放置的铁锅出现锈蚀,主要是铁与____________ 发生化学反应所致。
现有:①氧化钙 ②氢氧化钠 ③硝酸铵 ④甲烷 ⑤硝酸钾 ⑥纯碱,选择适当物质的序号填空。
(1)溶于水温度降低的盐
(2)广泛用于生产玻璃、造纸、纺织生产的盐
(3)常用作食品干燥剂
(4)可用作炉具清洁剂的碱
(5)一种由三种元素组成的复合肥料
(6)最简单的有机物
Ⅱ.化学与生活息息相关,请运用化学知识回答以下问题。
(7)市场上出售的净水器利用
(8)洗涤剂去油污利用的是其
(9)坏血病是因为缺乏
(10)放置的铁锅出现锈蚀,主要是铁与
您最近一年使用:0次
三、实验题 添加题型下试题
实验题
|
适中(0.65)
17. 实验室常用稀盐酸制取二氧化碳
(1)配制 200g 质量分数为 7.3%的稀盐酸
①需要质量分数为 36.5%的浓盐酸____________ g。
②用量筒量取水时,俯视读数,会导致配制得到的溶液浓度____________ (选填“偏大”、“偏小”)。
③混匀时用到的玻璃仪器有烧杯、____________ 。
(2)制取二氧化碳

①仪器 a 的名称是___________ 。
②实验室制备二氧化碳的原理是___________ (用化学方程式表示)。实验室可以按照“B→F→F→D” 的装置顺序制取并收集干燥、纯净的 CO2。第一个 F 装置盛放饱和 NaHCO3溶液的作用是___________ , 第二个 F 装置盛放的试剂是___________ 。
③在B装置中连接压强传感器,测得压强变化情况如图。下列说法正确的是___________ 。

A.ab 段长颈漏斗中液面逐渐上升
B.bc 段石灰石与稀盐酸脱离接触
C.c 点的对应操作可能是打开弹簧夹
(3)生成二氧化碳量的测定
选择 G 装置可测定生成 CO2的体积,其中植物油的作用是__________ 。
(1)配制 200g 质量分数为 7.3%的稀盐酸
①需要质量分数为 36.5%的浓盐酸
②用量筒量取水时,俯视读数,会导致配制得到的溶液浓度
③混匀时用到的玻璃仪器有烧杯、
(2)制取二氧化碳

①仪器 a 的名称是
②实验室制备二氧化碳的原理是
③在B装置中连接压强传感器,测得压强变化情况如图。下列说法正确的是

A.ab 段长颈漏斗中液面逐渐上升
B.bc 段石灰石与稀盐酸脱离接触
C.c 点的对应操作可能是打开弹簧夹
(3)生成二氧化碳量的测定
选择 G 装置可测定生成 CO2的体积,其中植物油的作用是
您最近一年使用:0次
四、填空与简答 添加题型下试题
填空与简答-填空题
|
较难(0.4)
解题方法
18. 能源既是国家经济发展的命脉,也是国家发展战略的重要支柱。
(1)传统的化石能源有煤、石油、__________ ,它们是__________ (选填“可再生”或“不可再生”)能源。
(2)氢能源是一种清洁的新能源。
①制氢:可利用太阳能和化石燃料来制备氢气。
途径Ⅰ:光分解水,过程如图 1。该过程中生成的氢气与氧气在相同条件下的体积之比为__________ ; ZnFe2O4在该反应中起__________ 作用,其中铁元素的化合价为__________ 。

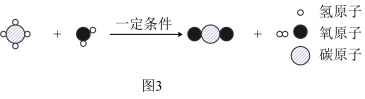
途径Ⅱ:化石燃料催化重整制氢,如甲烷制氢过程如图 3。该流程中甲烷和水蒸气反应的化学方程式是__________ 。
②储氢:镁铜合金(Mg2Cu)是一种潜在的储氢材料,在氩气保护下,将一定量比的 Mg、Cu 单质在一定温度下熔炼获得。储氢过程如图 2。
A.镁铜合金(Mg2Cu)属于__________ (选填“合成材料”、“金属材料”或“复合材料”)。
B.已知: ,22.4 g 合金 Mg2Cu 完全吸氢后所得混合物与过量盐酸反应,放出 H2的质量为
,22.4 g 合金 Mg2Cu 完全吸氢后所得混合物与过量盐酸反应,放出 H2的质量为__________ 。
③用氢:目前,以 H2作为能源的氢氧燃料电池不断取得技术上的突破。燃料电池将化学能直接转化为__________ 能。
(1)传统的化石能源有煤、石油、
(2)氢能源是一种清洁的新能源。
①制氢:可利用太阳能和化石燃料来制备氢气。
途径Ⅰ:光分解水,过程如图 1。该过程中生成的氢气与氧气在相同条件下的体积之比为

途径Ⅱ:化石燃料催化重整制氢,如甲烷制氢过程如图 3。该流程中甲烷和水蒸气反应的化学方程式是

②储氢:镁铜合金(Mg2Cu)是一种潜在的储氢材料,在氩气保护下,将一定量比的 Mg、Cu 单质在一定温度下熔炼获得。储氢过程如图 2。
A.镁铜合金(Mg2Cu)属于
B.已知:
 ,22.4 g 合金 Mg2Cu 完全吸氢后所得混合物与过量盐酸反应,放出 H2的质量为
,22.4 g 合金 Mg2Cu 完全吸氢后所得混合物与过量盐酸反应,放出 H2的质量为③用氢:目前,以 H2作为能源的氢氧燃料电池不断取得技术上的突破。燃料电池将化学能直接转化为
您最近一年使用:0次
五、科学探究题 添加题型下试题
科学探究题
|
较难(0.4)
解题方法
19. 酸在工业、医药等领域的应用特别广泛。某化学兴趣小组对盐酸、硫酸的相关性质展开了如下项目式探究。
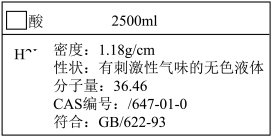
任务一:初识盐酸和硫酸。
某酸溶液由于标签被腐蚀,无法看清药品名称和化学式。根据残留的部分信息可以判断出该酸为__________ (写出化学式)。
任务二:探究酸的性质
【进行实验】
【交流讨论】
(1)硫酸和盐酸部分化学性质相同,其本质原因是溶液中都有__________ (写出离子符号)。
(2)与稀酸反应放出气体的固体__________ 是活泼金属(选填“一定”或“不一定”)。
任务三:再探盐酸和硫酸
【提出问题】为什么盐酸、硫酸部分化学性质不同?
【查阅资料】①电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小;
②相同温度下同种溶液电导率越大离子浓度越大。
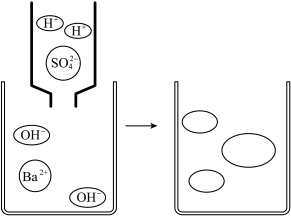
【进行实验】同学对这个问题进行了如下探究:用滴定管分别向 Ba(OH)2溶液中匀速滴加稀盐酸和稀硫酸,观察现象并分别绘制出电导率随温度变化的曲线 1(滴入盐酸)、曲线 2(滴入硫酸)。
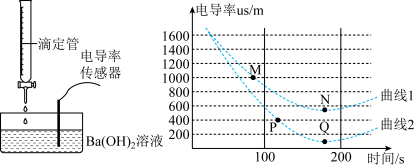
【交流讨论】
(1)请写出曲线 1 中反应的化学反应方程式___________ ,其中点 M 处烧杯中溶液溶质有___________ (写化学式)。
(2)曲线 2 的微观本质如图,请将图补充完整___________ 。
(3)根据该实验,下列所得结论正确的是___________ (填序号)。
A.溶液离子浓度越大,电导率越强
B.N 点和 Q 点是中和反应的结束点
C.随着酸的不断增加,电导率最终趋近于稳定值
【实验结论】盐酸和硫酸中酸根离子不同,也可体现酸的个性。

任务一:初识盐酸和硫酸。
某酸溶液由于标签被腐蚀,无法看清药品名称和化学式。根据残留的部分信息可以判断出该酸为
任务二:探究酸的性质
【进行实验】
| 实验内容 | 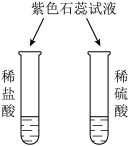 | 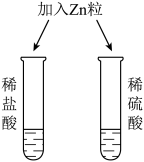 |  | 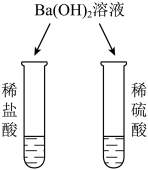 |
| 实验现象 | 溶液都 | 都有 | 都有气体生成 | 盐酸中无明显现象硫酸中有白色沉淀生成 |
(1)硫酸和盐酸部分化学性质相同,其本质原因是溶液中都有
(2)与稀酸反应放出气体的固体
任务三:再探盐酸和硫酸
【提出问题】为什么盐酸、硫酸部分化学性质不同?
【查阅资料】①电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小;
②相同温度下同种溶液电导率越大离子浓度越大。
【进行实验】同学对这个问题进行了如下探究:用滴定管分别向 Ba(OH)2溶液中匀速滴加稀盐酸和稀硫酸,观察现象并分别绘制出电导率随温度变化的曲线 1(滴入盐酸)、曲线 2(滴入硫酸)。

【交流讨论】
(1)请写出曲线 1 中反应的化学反应方程式
(2)曲线 2 的微观本质如图,请将图补充完整

(3)根据该实验,下列所得结论正确的是
A.溶液离子浓度越大,电导率越强
B.N 点和 Q 点是中和反应的结束点
C.随着酸的不断增加,电导率最终趋近于稳定值
【实验结论】盐酸和硫酸中酸根离子不同,也可体现酸的个性。
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:身边的化学物质、化学与社会发展、物质构成的奥秘、化学实验、物质的化学变化
试卷题型(共 17题)
题型
数量
选择题
13
填空与简答
2
实验题
1
科学探究题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 空气的污染与防治 资源综合利用和新能源开发的重要意义 常见几种燃料使用对环境的影响 | 单选题 |
| 2 | 0.85 | 离子符号的含义及书写 元素符号书写及含义 化学式书写及读法 | 单选题 |
| 3-5 | 0.85 | 根据化学式计算相对分子质量 根据化学式计算元素质量比 金属与氧气反应 燃烧的定义及条件 | 选择题组 |
| 6 | 0.85 | 原子中各类微粒的数值关系 原子结构示意图含义及应用 元素周期表及元素分类 周期表信息示意图及结构示意图的综合考查 | 单选题 |
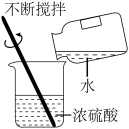
| 7 | 0.85 | 浓硫酸的稀释 溶液的酸碱性的判断与pH的测定 物质的加热 过滤 | 单选题 |
| 8 | 0.85 | 分解反应 强碱露置在空气中的变质 生石灰的性质及用途 | 单选题 |
| 9 | 0.85 | 一氧化碳的还原性 金属与氧气反应 溶液的酸碱性的判断与pH的测定 盐类参与的反应 | 单选题 |
| 10 | 0.65 | 不含杂质的化学方程式计算 金属与酸反应原理 多种多样的物质及其组成 分子是保持物质化学性质的最小微粒 | 单选题 |
| 11 | 0.85 | 微粒的观点解释现象 分子、原子的区别与联系 中和反应的概念及微观本质 | 单选题 |
| 12 | 0.85 | 复分解反应发生的条件 常见酸碱盐的溶解性 常见物质的颜色 | 单选题 |
| 13 | 0.65 | 结晶分离混合物 固体溶解度曲线的应用 溶解度的相关计算 溶质质量分数的涵义 | 单选题 |
| 14 | 0.4 | 二氧化碳的检验、验满及净化 二氧化碳不可燃、不支持燃烧性质 碱的通性 盐类参与的反应 | 单选题 |
| 15 | 0.4 | 不含杂质的化学方程式计算 金属与盐溶液反应 金属与酸反应原理 溶液和化学方程式的综合计算 | 单选题 |
| 二、填空与简答 | |||
| 16 | 0.85 | 活性炭的吸附性 乳化现象及应用 几种常见碱的物理性质及用途 常见化肥的种类及性质 | 填空题 |
| 18 | 0.4 | 不含杂质的化学方程式计算 化合价代数和的计算与应用 金属与酸反应原理 化石燃料的形成及现状 | 填空题 |
| 三、实验题 | |||
| 17 | 0.65 | 二氧化碳制取的综合考查 固体配制一定质量分数溶液 万用瓶的使用 根据图像分析结论 | |
| 四、科学探究题 | |||
| 19 | 0.4 | 酸的通性 常见的酸碱指示剂及其变色情况 盐类参与的反应 设计实验探究物质的成分 | |