17. 过氧化钙晶体(CaO
2•xH
2O)是优良的供氧剂,受热会逐渐失水,120℃时完全分解为CaO
2,350℃时CaO
2迅速分解为CaO和O
2。
(一)【性质探究】取少量CaO
2于试管中加过量稀盐酸,无气泡产生;再加少量MnO
2粉末,产生大量气泡。静置、取上层清液,逐渐加入碳酸钠溶液,先产生大量气泡,再出现白色沉淀。
⑴CaO
2和盐酸发生复分解反应的化学方程式为
___。
⑵加入碳酸钠溶液,产生的气体是
___;出现白色沉淀,说明上层清液中含
___。
(二)【制备流程】
方法1:由Ca(OH)
2为原料制备CaO
2•8H
2O流程如下:
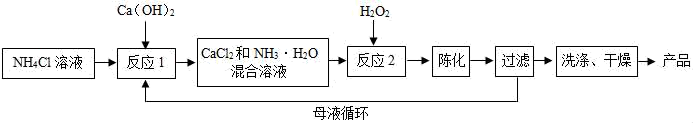
陈化:让初生晶体和母液放置一段时间,使晶体由小长大。
⑴将反应2及陈化的化学方程式补充完整:CaCl
2+H
2O
2+2NH
3•H
2O+6
___=CaO
2•8H
2O↓+2NH
4Cl
⑵检验固体是否洗净的方法是:
___。
⑶制备过程中除水外可循环使用的物质是:
___(填化学式)。
方法2:由鸡蛋壳(含较多CaCO
3)为原料制备CaO
2•8H
2O流程如下:
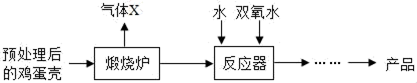
⑷反应器中由化合反应生成CaO
2•8H
2O,反应化学方程式为:
___。
⑸在反应器中,应
___。
①先加水冷却后再加双氧水
②先加双氧水冷却后再加水
⑹若煅烧充分,则获得的CaO
2•8H
2O中还含有的固体杂质是
___(填化学式)。
⑺“绿色化学”是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO
2•8H
2O
的反应符合“绿色化学”的是
___(填“方法1”或“方法2”)。
(三)【组成测定】若所得产品为CaO
2•xH
2O,下列装置可测定该产品的组成(样品中的杂质受热不反应)。
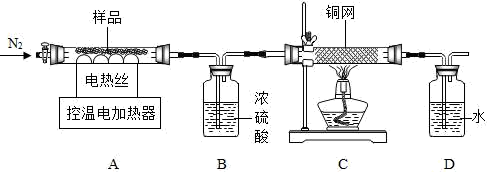
⑴实验前先缓慢通N
2一段时间,控温将样品加热到350℃至CaO
2分解完全;继续缓慢通N
2,其目的是
___(答一点即可)。
⑵装置B作用是
___(填序号)
①测定产生的H
2O质量
②便于观察和控制气流速度
⑶若2.7g样品,加热到350℃至CaO
2分解完全,测得B装置重1.44g、C中铜网增重0.16g。则x=
___。
【反思】若先加热A,后加热C装置,测得x值
___(填“偏大”、“偏小”或“不变”)。