2014-2015山东省淄博市临淄区皇城镇二中八年级下学期期中化学试卷
山东
九年级
期中
2015-06-02
372次
整体难度:
容易
考查范围:
物质的化学变化、化学实验、物质的组成与结构、身边的化学物质
一、选择题 添加题型下试题
| A.鲜牛奶变质 | B.粮食酿成酒 | C.钢丝球刷碗 | D.煤炭的燃烧 |
【知识点】 质量守恒定律内容及适用范围解读
①原子数目②原子种类③分子数目④分子种类⑤元素种类⑥物质的总质量⑦物质的种类
| A.①②⑤⑥ | B.①②③⑤ | C.①②⑤⑦ | D.③④⑥⑦ |
【知识点】 质量守恒定律的微观解释解读
| A.燃烧前后蜡烛质量不变 |
| B.蜡烛减少的质量等于生成的二氧化碳和水的质量 |
| C.蜡烛燃烧后生成物的质量之和等于蜡烛减少的质量与消耗氧气的质量之和 |
| D.燃烧前蜡烛的质量与氧气质量之和等于生成的二氧化碳与水的质量之和 |
| A.20℃,1L水与1L酒精混合后的体积等于2L |
| B.20℃,1g镁在1g氧气充分燃烧后,生成氧化镁2g |
| C.20℃,1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫 |
| D.20℃,1个氢分子与1个氧分子结合生成2个水分子 |
| A.碳原子 | B.氧原子 | C.氮原子 | D.氢原子 |
【知识点】 质量守恒定律的微观解释解读
A. | B.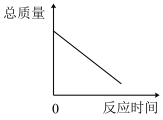 | C. | D.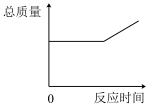 |
【知识点】 质量守恒定律内容及适用范围解读
 2N2+6H2O ,则X的化学式为
2N2+6H2O ,则X的化学式为| A.NH3 | B.NO2 | C.CH4 | D.C2H6 |
【知识点】 根据方程式推测化学式解读
| A.化学反应发生时不一定能观察到明显的现象 |
| B.从元素周期表中可以查出元素的相对原子质量 |
| C.配平化学方程式的依据是质量守恒定律 |
| D.书写化学方程式时,生成物中只要有气体生成就必须注明“↑”符号 |
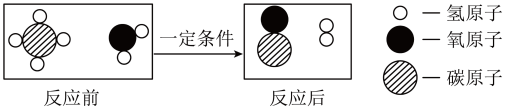
根据以上微观示意图得出的结论中,正确的是
| A.反应前后各元素的化合价均不变 |
| B.水煤气的成分是一氧化碳和氢气 |
| C.该反应中含氢元素的化合物有3种 |
| D.该反应的化学方程式中甲烷和水的质量之比为1:1 |
| A.27:32:102 | B.27:24:43 | C.108:96:204 | D.4:3:2 |
【知识点】 根据化学方程式计算质量比解读
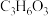 ),使肌肉酸痛。放松一段时间后由于乳酸与吸入的氧气反应生成二氧化碳和水,肌肉的酸痛感消失。表示该反应的化学方程式正确的是( )
),使肌肉酸痛。放松一段时间后由于乳酸与吸入的氧气反应生成二氧化碳和水,肌肉的酸痛感消失。表示该反应的化学方程式正确的是( )A.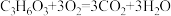 | B. |
C.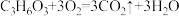 | D.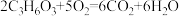 |
| A.拉瓦锡 | B.波义耳 | C.汤姆森 | D.卢瑟福 |

| A.水在通电的条件下生成氢气和氧气 |
| B.反应物是水,生成物是氢气和氧气,反应条件是通电 |
| C.2个水在通电的条件下生成2个氢气和1个氧气 |
| D.每36份质量的水在通电的条件下生成4份质量的氢气和32份质量的氧气 |
【知识点】 化学方程式含义解读 电解水实验的现象和结论解读
| A.反应前物质的总质量等于反应后物质的总质量 |
| B.化合物中元素化合价的正价代数和与负价的代数和相等 |
| C.化学反应前后各种原子的个数相等 |
| D.同种元素的原子和离子的电子数相等 |
| A.16 | B.32 | C.64 | D.96 |
【知识点】 有关质量守恒定律的计算解读
| A.因为H2O和H2O2的组成元素相同,所以它们的分解产物也相同 |
| B.因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳、氢元素 |
| C.因为化学变化都遵循质量守恒定律,所以质量不发生改变的变化一定是化学变化 |
| D.因为水受热变成水蒸气时质量没有发生改变,所以该变化也遵循质量守恒定律 |
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 3 | 5 | 20 | 7 |
| 反应后质量/g | 10 | 5 | 8 | 待测 |
通过分析,判断下列说法正确的是
| A.测得反应后丁物质的质量为5g |
| B.乙物质一定是催化剂 |
| C.该反应是化合反应 |
| D.该反应是分解反应 |
| A.质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关 |
| B.通过化学变化,只能改变世界上物质的种类,不能改变物质的总质量 |
| C.质量守恒定律为定量揭示化学变化的规律,提供了理论依据 |
| D.随着科技的发展,精密仪器为我们定量研究化学变化创造了条件 |
【知识点】 质量守恒定律内容及适用范围解读
二、填空与简答 添加题型下试题
(1)Cu+O2
 CuO2 违背了
CuO2 违背了(2)H2O
 H2↑+O2 ↑违背了
H2↑+O2 ↑违背了【知识点】 用质量守恒定律确定物质组成解读

(1)试写出上述四个实验中发生反应的化学方程式:
| A. | B. |
| C. | D. |
①
③
(3)实验室通常用过氧化氢溶液和二氧化锰来制取氧气,请你写出该反应的化学方程式
①
②
③
(1)氢氧化钠(NaOH)溶液和硫酸铜(CuSO4)溶液反应,产生氢氧化铜沉淀[Cu(OH)2],生成的硫酸钠(Na2SO4)留在溶液中。
(2)白磷在空气中燃烧,生成五氧化二磷。
(3)甲烷(CH4)燃烧生成二氧化碳和水。
【知识点】 化学方程式的书写解读 根据化学方程式计算质量比解读
三、计算题 添加题型下试题
题目:将15g氯酸钾(KClO3)和3g二氧化锰[MnO2(作催化剂)]混合放入大试管中加热,能较快的分解生成氯化钾(KCl)和氧气。当收集到所需要的氧气后,停止加热,待试管冷却后,称量剩余固体的质量为13.2g,求生成的氯化钾的质量。
(1)张明同学很快得到15g+3g-13.2g是
(2)下面是两位同学根据化学方程式计算的过程,请你在下边的横线上帮他们改正其中的错误:
解:设生成氯化钾的质量是
 g。
g。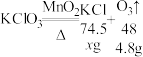
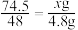
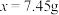
答:生成的氯化钾的质量是7.45g。
【知识点】 不含杂质的化学方程式计算解读
四、实验题 添加题型下试题
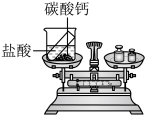
(1)根据实验目的,小明应该测量的数据是
(2)实验步骤如下:
①按如图方式放好仪器,使天平平衡,记录称量数据。
②将小试管中的稀盐酸全部倒入烧杯中,观察到烧杯剧烈反应,并有
③当反应结束时,同学们发现天平的指针偏向右边。同学们又重新称量,记录了数据。他们感到困惑:其他操作均正常,实验现象与数据为何与预测结果不符?请你帮他们分析导致天平不平衡的原因是
(3)同学们经过讨论,意识到了自己所犯的错误,有
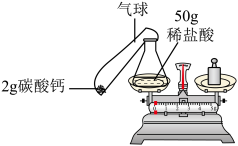
实验步骤如下:
①按如图方式放好仪器,使天平平衡,记录称量数据。
②将碳酸钙粉末全部倒入到锥形瓶中,观察现象。
③当反应结束后,气球完全鼓起,他们发现天平的指针仍然偏向右边,你认为出现该实验现象的合理解释最应该是下列各项中的
A.该反应前后原子的种类、数目变少
B.该反应生成物的总质量小于反应物的总质量
C.空气的浮力作用干扰了实验结果
D.生成气体的反应不遵守质量守恒定律
若不考虑该因素的影响,该反应是否遵循质量守恒定律?
五、计算题 添加题型下试题
【实验目的】测定大理石样品中碳酸钙的质量分数。
【查阅资料】二氧化硅等杂质不溶于水,也不与盐酸反应。
【实验过程】准确称量12g大理石样品于烧杯中,向其中加入80mL盐酸(HCl),立即将烧杯放到电子秤上称量。每分钟记录一次数据(提示:反应结束后盐酸有剩余;碳酸钙和稀盐酸反应后生成氯化钙、水和二氧化碳;称量的质量包括烧杯)。相关的实验数据如下表:
| 时间/分 | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 质量/g | 152.0 | 150.0 | 148.5 | 148.0 | 147.6 | 150.0 | 147.6 | 147.6 | 147.6 |
(1)表中有一个称量数据是不合理的,该数据的测定时间是第 分钟。
(2)整个过程中产生二氧化碳的质量是 g。
(3)计算样品中碳酸钙的质量分数。(写出计算过程,计算结果保留一位小数)
试卷分析
导出试卷题型(共 27题)
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.85 | 质量守恒定律内容及适用范围 | 单选题 |
| 2 | 0.85 | 质量守恒定律的微观解释 | 单选题 |
| 3 | 0.85 | 质量守恒定律内容及适用范围 蜡烛燃烧的实验探究及产物分析 | 单选题 |
| 4 | 0.85 | 化学方程式含义 | 单选题 |
| 5 | 0.65 | 化学方程式含义 根据化学方程式计算质量比 微粒的观点解释现象 | 单选题 |
| 6 | 0.65 | 质量守恒定律的微观解释 | 单选题 |
| 7 | 0.65 | 质量守恒定律内容及适用范围 | 单选题 |
| 8 | 0.85 | 根据方程式推测化学式 | 单选题 |
| 9 | 0.85 | 化学反应现象和结论判断 用质量守恒定律确定物质组成 化学方程式的书写 元素周期表信息示意图 | 单选题 |
| 10 | 0.65 | 根据化学方程式计算质量比 微粒图像的分析及应用 常见元素、原子团的化合价 | 单选题 |
| 11 | 0.85 | 根据化学方程式计算质量比 | 单选题 |
| 12 | 0.94 | 化学方程式的书写 | 单选题 |
| 13 | 0.85 | 化学发展史 | 单选题 |
| 14 | 0.85 | 化学方程式含义 电解水实验的现象和结论 | 单选题 |
| 15 | 0.85 | 质量守恒定律内容及适用范围 质量守恒定律的微观解释 同一元素的离子与原子相互转化 常用化合价规律 | 单选题 |
| 16 | 0.65 | 有关质量守恒定律的计算 | 单选题 |
| 17 | 0.65 | 质量守恒定律内容及适用范围 用质量守恒定律确定物质组成 分子是保持物质化学性质的最小微粒 | 单选题 |
| 18 | 0.65 | 催化剂的概念、性质与用途 化合反应 分解反应 有关质量守恒定律的计算 | 单选题 |
| 19 | 0.85 | 实验探究质量守恒定律 | 单选题 |
| 20 | 0.65 | 质量守恒定律内容及适用范围 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.65 | 化学方程式的书写 金属与氧气反应 电解水原理 | 填空题 |
| 22 | 0.85 | 用质量守恒定律确定物质组成 | 填空题 |
| 23 | 0.65 | 化学方程式含义 化学方程式的书写 物质与氧气反应的共性分析 过氧化氢制取氧气实验 | 简答题 |
| 24 | 0.85 | 化学方程式的书写 根据化学方程式计算质量比 | 填空题 |
| 三、计算题 | |||
| 25 | 0.65 | 不含杂质的化学方程式计算 | |
| 27 | 0.65 | 有关质量守恒定律的计算 含杂质的化学方程式计算 制取二氧化碳的原理 溶质质量分数结合化学方程式的计算 | |
| 四、实验题 | |||
| 26 | 0.65 | 质量守恒定律内容及适用范围 实验探究质量守恒定律 质量守恒定律的微观解释 | |







