2022年全国初中化学学科竞赛试题
全国
九年级
竞赛
2022-11-01
2029次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学与社会发展、化学实验、物质构成的奥秘
2022年全国初中化学学科竞赛试题
全国
九年级
竞赛
2022-11-01
2029次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、化学与社会发展、化学实验、物质构成的奥秘
一、选择题 添加题型下试题
选择题-单选题
|
适中(0.65)
名校
解题方法
1. 描述物质变化的成语有:①滴水成冰;②死灰复燃;③木已成舟;④火烧赤壁;⑤沙里淘金;⑥火上浇油;⑦百炼成钢;⑧花香四溢;⑨玉石俱焚,其中属于化学变化的是
| A.②③④⑤⑥⑦ | B.②④⑤⑥⑦⑨ | C.①③④⑤⑧⑨ | D.②④⑥⑦⑨ |
【知识点】 化学变化与物理变化判断解读
您最近一年使用:0次
2022-10-31更新
|
651次组卷
|
5卷引用:2022年全国初中化学学科竞赛试题
选择题-单选题
|
适中(0.65)
解题方法
2. 纳米铁粉在空气中能自燃并生成一种红色氧化物。对比铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧的事实,某同学得出的下列结论正确的是
| A.纳米铁粉在空气中自燃的产物是四氧化三铁 |
| B.相同的反应物在不同条件下生成物可能不同 |
| C.有些物质燃烧时温度不需要达到着火点 |
| D.反应物间的接触面积大小不是反应能否发生的因素之一 |
您最近一年使用:0次
2022-10-31更新
|
483次组卷
|
5卷引用:【市级联考】四川省内江市2019届九年级上学期期末考试化学试题
【市级联考】四川省内江市2019届九年级上学期期末考试化学试题2022年全国初中化学学科竞赛试题2023分层教学_人教版_第七单元 课题1 燃烧和灭火 课时1_中等题(已审)2023分层教学_鲁教版_第六单元 第一节 燃烧与灭火第2课时_能力题(已审)(已下线)吉林省辽源市西安区2023-2024学年九年级上学期化学期末试卷.
选择题-单选题
|
较易(0.85)
解题方法
3. 常温下,氯气与苛性钠溶液反应的产物是氯化钠、次氯酸钠(NaClO)和水。该反应中未涉及 到的氯元素的化合价为
| A.-1 | B.+1 | C.-2 | D.0 |
【知识点】 常用化合价规律解读 化合价代数和的计算与应用解读
您最近一年使用:0次
2022-10-31更新
|
383次组卷
|
2卷引用:2022年全国初中化学学科竞赛试题
二、多选题 添加题型下试题
多选题
|
适中(0.65)
解题方法
4. 我国拥有丰富的页岩气,它与天然气的主要成分相同。下列关于页岩气的说法正确的是
| A.它是混合物 | B.它的主要成分是一种有机物 |
| C.它是可再生能源 | D.点燃该气体无需验纯 |
您最近一年使用:0次
多选题
|
适中(0.65)
解题方法
5. 下列实验操作不能达到目的的是
| A.向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,则证明BaCl2溶液有酸性 |
| B.准确称取1.5gCa(OH)2,常温下配制50g3%的Ca(OH)2溶液 |
| C.在实验室,用98%的浓硫酸来配制50g9.8%的稀硫酸 |
| D.可通过灼热的铜粉除去CO2中的O2 |
您最近一年使用:0次
三、选择题 添加题型下试题
选择题-单选题
|
适中(0.65)
解题方法
6. 下列事实不能作为相应观点的证据的是
| A.尘土飞扬,说明分子是运动的 |
| B.电解水得到氢气和氧气,说明分子是可分的 |
| C.气体被压缩后体积发生了较大变化,说明气体分子间的间隔较大 |
| D.往水杯中倒水,可以倒到稍稍高出杯沿,而水不会满溢出来,说明分子间存在引力 |
【知识点】 微粒的观点解释现象解读 原子是化学变化中最小的粒子
您最近一年使用:0次
2022-10-31更新
|
359次组卷
|
2卷引用:2022年全国初中化学学科竞赛试题
7. 归纳法是学习化学的重要方法之一,下列图示正确的是
A.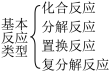 化学反应分类 化学反应分类 | B.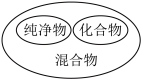 物质分类 物质分类 |
C.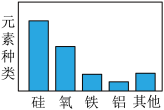 地壳中元素含量 地壳中元素含量 | D.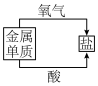 金属的化学性质 金属的化学性质 |
您最近一年使用:0次
2022-03-26更新
|
475次组卷
|
7卷引用:2020年山东省日照市东港区新营中学中考三模化学试题
2020年山东省日照市东港区新营中学中考三模化学试题2019年湖北省武汉市武昌区中考一模化学试题2022年海南省定安县中考一模化学试题2022年山东省滨州市阳信县第三实验中学中考模拟化学试题2022年全国初中化学学科竞赛试题(已下线)黄金卷03-【赢在中考·黄金8卷】备战2023年中考化学全真模拟卷(海南专用)2023年山东省聊城市阳谷县九年级化学竞赛试题
选择题-单选题
|
适中(0.65)
名校
8. 超临界流体是温度和压力同时高于临界值的流体,也即压缩到具有接近液体密度的气体,是物质介于气态和液态之间的一种新的状态。目前应用最广的是超临界二氧化碳,它可作为溶剂、发泡剂取代某些有机溶剂、氟氯代烷等。下列有关说法中错误的是
| A.超临界二氧化碳与其气态或液态之间的转化是物理变化 |
| B.超临界二氧化碳的形成,引起二氧化碳化学性质的改变 |
| C.超临界二氧化碳可用于中药、香料中有效成分的提取 |
| D.用超临界二氧化碳代替氟氯代烷可减轻对臭氧层的破坏 |
您最近一年使用:0次
2019-10-06更新
|
574次组卷
|
5卷引用:江苏省启东市长江中学2016-2017学年九年级上学期12月月考化学试题
江苏省启东市长江中学2016-2017学年九年级上学期12月月考化学试题2020年广西北部湾经济区同城中考模拟(三)化学试题(已下线)《单元测试定心卷》第六单元 燃烧与燃料(基础过关)-2020-2021学年九年级化学上册单元测试定心卷(鲁教版)2022年全国初中化学学科竞赛试题湖南省怀化市溆浦县溆浦县第一中学2023-2024学年九年级上学期模拟预测化学试题
四、多选题 添加题型下试题
多选题
|
较难(0.4)
解题方法
10. 下列装置能达到对应实验目的是
A. 比较MnO2和Fe2O3的催化效果 比较MnO2和Fe2O3的催化效果 |
B. 制取并收集CO2气体 制取并收集CO2气体 |
C. 确认CO2和NaOH已发生反应 确认CO2和NaOH已发生反应 |
D. 氨气与滴有酚酞的水形成红色喷泉 氨气与滴有酚酞的水形成红色喷泉 |
您最近一年使用:0次
多选题
|
适中(0.65)
解题方法
12. 溶液的密度随固体溶质溶解的增多而增大,某溶质的饱和溶液还能继续溶解一定质量的其他溶质,如图,一个悬挂在弹簧秤上的物体浸没在Ba(OH)2饱和溶液中,在恒温条件下,加入一些下列物质,能使弹簧秤读数变大的是(物体不与溶液发生化学反应)


| A.H2O | B.CuSO4溶液 | C.Ba(OH)2晶体 | D.BaCl2晶体 |
【知识点】 饱和溶液和不饱和溶液判断解读 碱的通性解读
您最近一年使用:0次
五、选择题 添加题型下试题
选择题-单选题
|
较易(0.85)
解题方法
13. 除去下列物质中混有的少量杂质所选用的操作方法,正确的是
| 选项 | 物质 | 操作方法 |
| A | O2中混有少量HCl气体 | 将气体通过足量NaOH溶液 |
| B | CuO中混有少量碳粉 | 加入适量稀盐酸,过滤,洗涤,干燥 |
| C | NaCl溶液中混有少量CaCl2 | 加入过量Na2CO3溶液、过滤 |
| D | Cu(NO3)2溶液中混有少量CuCl2 | 加入适量AgNO3溶液、过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
选择题-单选题
|
较难(0.4)
名校
14. 在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,下图一定不正确的是
A. | B.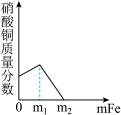 |
C. | D.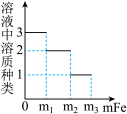 |
【知识点】 金属与盐溶液反应 金属活动顺序图像分析
您最近一年使用:0次
2022-01-08更新
|
872次组卷
|
9卷引用:广西河池市凤山县太平初中2019届九年级下学期中考二模化学试题
六、多选题 添加题型下试题
多选题
|
较难(0.4)
解题方法
15. 某无色气体可能含有H2O、CO2、CO、H2中的一种或几种,若将该气体依次通过以下实验装置(假设每步操作中,参加反应的气体均完全反应或被吸收),下列实验设计能达到预期要求的是


| A.气体依次通过D→E来验证是否含有CO2和H2O |
| B.气体依次通过B→A→E来验证是否含有H2 |
| C.气体依次通过E→D→C→B→A→D→E来验证是否含有H2O、CO2、CO、H2 |
| D.气体依次通过C→A→D来验证是否含有CO |
您最近一年使用:0次
七、填空与简答 添加题型下试题
填空与简答-填空题
|
较难(0.4)
解题方法
16. 宏观和微观相联系是化学独特的思维方式。
(1)微观探析化学反应的规律是化学科学的核心任务。根据下列微观示意图回答问题:

①从微粒的角度说明图A反应的实质是___________ (书写离子方程式);
②图B所示反应中,参加反应的微粒是___________ 、___________ (写出微粒的符号)。
(2)化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1摩尔任何物质中含有构成它的微粒个数都是6.02×1023个,1摩尔任何物质的质量是以克为单位,数值上都等于该物质的相对分子质量。例如1摩尔水的各种量关系如下:

①1摩尔水中氢原子数目是___________ 个;
②1摩尔水中氧元素质量为___________ g;
③3.01×1023个氧原子为___________ 摩尔
(1)微观探析化学反应的规律是化学科学的核心任务。根据下列微观示意图回答问题:

①从微粒的角度说明图A反应的实质是
②图B所示反应中,参加反应的微粒是
(2)化学上有一种能将微观粒子数目与宏观物质质量联系起来的量,叫物质的量,其单位是摩尔。1摩尔任何物质中含有构成它的微粒个数都是6.02×1023个,1摩尔任何物质的质量是以克为单位,数值上都等于该物质的相对分子质量。例如1摩尔水的各种量关系如下:

①1摩尔水中氢原子数目是
②1摩尔水中氧元素质量为
③3.01×1023个氧原子为
您最近一年使用:0次
填空与简答-科普阅读题
|
适中(0.65)
解题方法
17. 甲酸(HCOOH)与浓硫酸共热到60~80℃可发生脱水型的分解反应,并由此而制得CO气体。实验室用甲酸和浓硫酸混合后制取CO时,常不需加热,其具体操作方法如下:在试管内倒入一定体积的甲酸,然后再小心、缓慢地沿试管壁倒入等体积的浓硫酸,这时可见试管内液体分上、下两层,在两层液体的界面处有少量气泡,轻轻振动试管,可见液体交界面气泡增多,改变振动的力度可控制气泡产生的速率。试回答下列问题:
(1)用上述方法制取CO的化学反应方程式为___________ ;
(2)用该法制CO不需加热的原因___________ ;
(3)以上操作方法可控制反应速率的原因___________ 。
(1)用上述方法制取CO的化学反应方程式为
(2)用该法制CO不需加热的原因
(3)以上操作方法可控制反应速率的原因
您最近一年使用:0次
填空与简答-填空题
|
适中(0.65)
解题方法
18. 如图是一个电池的示意图,该装置可产生气体和电流。老师告诉同学们,只要用两种不同的导体做电极,用水果代替实验中的稀硫酸也可以组成一个电池,产生电流的原理是一样的。同学们很感兴趣,在课外实验中,同学们进行了水果电池的制作,记录了以下的实验数据:不同电极时单个西红柿水果电池的电流和电压:

注:除电极材料不一样外,其它实验条件相同,请回答以下问题:
(1)如图装置中能量的转变是从化学能转变为电能。该实验经过一段时间后溶液pH的变化是___________ (选填“增大”、“减小”、“不变”),质量减少的电极是___________ 。
(2)假如改用镁片和碳棒做电极,其它实验条件不变,根据上表的实验数据,你猜想产生的电压应比表中三种电池产生的电压___________ (选填“都大”、“都小”、“处在它们之间”或“无法判断”)。

| 电极 | 碳棒一铜片 | 碳棒一铁片 | 碳棒一锌片 |
| 电流强度(mA) | 1.43 | 4.26 | 4.63 |
| 电压(V) | 0.6 | 1.2 | 1.3 |
(1)如图装置中能量的转变是从化学能转变为电能。该实验经过一段时间后溶液pH的变化是
(2)假如改用镁片和碳棒做电极,其它实验条件不变,根据上表的实验数据,你猜想产生的电压应比表中三种电池产生的电压
您最近一年使用:0次
填空与简答-流程题
|
适中(0.65)
解题方法
19. 黑白复印机用的墨粉中常添加Fe3O4粉末。Fe3O4是由Fe2+、Fe3+和O2-按1∶2∶4的个数比构成的。下图是氧化沉淀法生产Fe3O4粉末的流程简图。已知第④步反应中各元素化合价保持不变。

(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4的___________ 性,还利用了Fe3O4是黑色的性质。
(2)四氧化三铁与盐酸反应方程式为___________ 。
(3)第②步加入试剂X,试剂X的名称是___________ 。
(4)在第③步反应是要向溶液中通入O2,以使生成的Fe(OH)2部分转化成Fe(OH)3,写出反应的化学方程式___________ 。在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于___________ ,才能确保第④步最终完全反应生成Fe3O4.
(5)操作Y的流程为___________ 、___________ 、晾干。

(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4的
(2)四氧化三铁与盐酸反应方程式为
(3)第②步加入试剂X,试剂X的名称是
(4)在第③步反应是要向溶液中通入O2,以使生成的Fe(OH)2部分转化成Fe(OH)3,写出反应的化学方程式
(5)操作Y的流程为
您最近一年使用:0次
填空与简答-填空题
|
适中(0.65)
解题方法
20. 工业上通过如下转化可制得KClO3晶体:
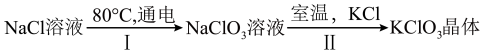
(1)I反应中,被还原的物质是___________ 。
(2)II中析出晶体后的母液中的溶质的化学式为___________ 。
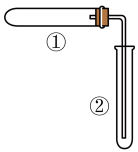
(3)用如图装置(夹持、加热装置已略去)进行实验,②中有现象,但该现象不能作为判断①中发生了化学反应的依据的是___________。
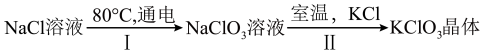
(1)I反应中,被还原的物质是
(2)II中析出晶体后的母液中的溶质的化学式为
(3)用如图装置(夹持、加热装置已略去)进行实验,②中有现象,但该现象不能作为判断①中发生了化学反应的依据的是___________。

| 选项 | ①中实验 | ②中现象 |
| A | 加热氯酸钾和二氧化锰的混合物 | 伸入试管内的带火星木条复燃 |
| B | 加热碱式碳酸铜固体 | 澄清石灰水变浑浊 |
| C | 加热铜丝 | 伸入水中导管口有气泡冒出 |
| D | 加热氯化铵和熟石灰的混合物 | 酚酞溶液变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
填空与简答-流程题
|
困难(0.15)
解题方法
21. 硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应,用以回收S,其物质转化如图所示。

(1)反应中当34gH2S转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O2的质量为___________ 。
(2)在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施是___________ 。
(3)写出图中从左往右逆时针各步转化的化学方程式:___________ 、___________ 、4FeCl2+___________ +4HCl=4FeCl3+___________ 。

(1)反应中当34gH2S转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O2的质量为
(2)在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施是
(3)写出图中从左往右逆时针各步转化的化学方程式:
您最近一年使用:0次
填空与简答-推断题
|
适中(0.65)
解题方法
22. 小明用六块积木A~F分别对应铁、二氧化碳、硫酸、氢氧化钙、碳酸钠、氯化钡中的一种物质,按照物质能反应的积木就叠放在一起,不反应的积木间就不接触的原则,搭成下图所示形状。已知E的物质类别与其他5种不同,B与C反应可以生成F,请完成下列问题:

(1)C的化学式为___________ ,D的俗称为___________ 。
(2)写出A与B反应的化学方程式___________ ,C与D的基本反应类型是___________ 。
(3)写出F物质的一个用途___________ 。

(1)C的化学式为
(2)写出A与B反应的化学方程式
(3)写出F物质的一个用途
您最近一年使用:0次
八、实验题 添加题型下试题
实验题
|
适中(0.65)
解题方法
23. 无焰食品加热器常被用于野外加热食物,它所用的材料有镁、铁、氯化钠。使用时加入水,利用镁和水反应产生热来加热。下面是在15℃、1个标准大气压的环境中对上述材料进行的研究。
实验l:将一定质量的镁条、铁粉和氯化钠加入盛有适量水的隔热容器中,连续搅拌,每隔一段时间记录一次温度,在图甲上绘得曲线1:然后把相同质量的镁条剪成若干细条,重复上述实验,绘得曲线2:再取相同质量的镁粉重复上述实验,绘得曲线3。
实验2:把2.4g镁粉、5.85g氯化钠和一定质量的铁粉混合,放入盛有100mL水的隔热容器中,并不断搅拌,一段时间后测出容器内升高的最高温度。图乙是在改变铁粉质量的实验条件下,绘得的温度变化曲线。实验3:把2.4g镁粉、28g铁粉和一定质量的氯化钠混合,放入盛有100mL水的隔热容器中,并不断搅拌,一段时间后测出容器内升高的最高温度。图丙是在改变氯化钠质量的实验条件下,绘得的温度变化曲线。

(1)通过实验l可以发现影响镁和水反应快慢的因素是___________ 。
(2)实验3中,当NaCl质量大于7.31g,实验就不必再做的原因是___________。
(3)如果在实验3中加入了3.66g的NaCl,容器中混合物升高的最高温度最接近___________ 。
(4)根据图乙和丙,在设计无焰食物加热器时,如果所用镁粉的质量为2.4g,则取7.31gNaCl和___________ g铁粉时,能做到用尽可能少的材料产生尽可能多的热量。
实验l:将一定质量的镁条、铁粉和氯化钠加入盛有适量水的隔热容器中,连续搅拌,每隔一段时间记录一次温度,在图甲上绘得曲线1:然后把相同质量的镁条剪成若干细条,重复上述实验,绘得曲线2:再取相同质量的镁粉重复上述实验,绘得曲线3。
实验2:把2.4g镁粉、5.85g氯化钠和一定质量的铁粉混合,放入盛有100mL水的隔热容器中,并不断搅拌,一段时间后测出容器内升高的最高温度。图乙是在改变铁粉质量的实验条件下,绘得的温度变化曲线。实验3:把2.4g镁粉、28g铁粉和一定质量的氯化钠混合,放入盛有100mL水的隔热容器中,并不断搅拌,一段时间后测出容器内升高的最高温度。图丙是在改变氯化钠质量的实验条件下,绘得的温度变化曲线。

(1)通过实验l可以发现影响镁和水反应快慢的因素是
(2)实验3中,当NaCl质量大于7.31g,实验就不必再做的原因是___________。
| A.加入更多的NaCl不再改变反应快慢 | B.加入NaCl会使反应变慢 |
| C.水已沸腾,不会再有温度变化 | D.需要加入更多的铁粉来提高温度 |
(4)根据图乙和丙,在设计无焰食物加热器时,如果所用镁粉的质量为2.4g,则取7.31gNaCl和
【知识点】 催化剂的概念、性质与用途解读 根据图像分析结论 操作目的分析
您最近一年使用:0次
实验题
|
较难(0.4)
名校
24. 晶体硅是一种重要的非金属材料。制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅,同时得到一种可燃性气体。
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl SiHCl3+H2
SiHCl3+H2
③SiHCl3与过量H2在1000~1100℃反应制得纯硅。
已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为_____ 。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为:_____ 。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①装置B中的试剂是_____ ,装置C中的烧瓶需要加热,其目的是:_____ 。
②装置D不能采用普通玻璃管的原因是_____ ,装置D中发生反应的化学方程式为_____ 。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及_____ 。
①高温下用碳还原二氧化硅制得粗硅,同时得到一种可燃性气体。
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl
 SiHCl3+H2
SiHCl3+H2③SiHCl3与过量H2在1000~1100℃反应制得纯硅。
已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为:
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①装置B中的试剂是
②装置D不能采用普通玻璃管的原因是
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及
您最近一年使用:0次
2019-09-03更新
|
496次组卷
|
3卷引用:湖北省黄冈中学2016年自主招生理科实验班预录考试化学模拟试题(B卷)
九、计算题 添加题型下试题
计算题
|
适中(0.65)
解题方法
25. 化学反应在防治环境污染中扮演了重要角色。某工厂废气中的SO2,可用以下方式处理。
方式一:2SO2+O2+2CaO=2CaSO4
方式二:2SO2+O2+4NaOH=2Na2SO4+2H2O
试计算:(已知:CaSO4的价格为700元/吨)
(1)若用方式一处理9.6tSO2,所得产品价值多少元?
(2)若用方式二处理9.6tSO2,刚好用去50t一定浓度的NaOH溶液,求所得溶液的溶质质量分数(最终结果精确到0.1%)。
方式一:2SO2+O2+2CaO=2CaSO4
方式二:2SO2+O2+4NaOH=2Na2SO4+2H2O
试计算:(已知:CaSO4的价格为700元/吨)
(1)若用方式一处理9.6tSO2,所得产品价值多少元?
(2)若用方式二处理9.6tSO2,刚好用去50t一定浓度的NaOH溶液,求所得溶液的溶质质量分数(最终结果精确到0.1%)。
您最近一年使用:0次
十、综合应用题 添加题型下试题
综合应用题
|
较难(0.4)
26. 固体铵盐A、B的成分可能是(NH4)2SO4、NH4HSO4,或是两者的混合物.甲、乙两个研究性学习小组要确定A和B的成分,并测定B中氮元素的质量分数.

(1)甲实验小组的同学取了数份相同质量的样品A溶于水,然后加入40% NaOH溶液(图中用氢氧化钠质量表示),水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用足量浓硫酸完全吸收,浓硫酸增重的质量如图.分析该图象并回答下列问题:
①写出ab段涉及的化学方程式:_____ .
②样品A的成分是_____ ,C点的数值是_____ .
(2)乙实验小组的同学取了数份不同质量的样品B,测定方法与甲组同学大部分相同,不同的是,他们将不同质量的铵盐分别加入到50.00mL NaOH溶液中(含8.12g NaOH),测定结果如下:
①分析实验数据可知,实验编号为_____ 的实验中,氢氧化钠足量,铵盐中的铵根离子完全转化成气体.
②计算B中氮元素的质量分数.______ (保留两位小数)

(1)甲实验小组的同学取了数份相同质量的样品A溶于水,然后加入40% NaOH溶液(图中用氢氧化钠质量表示),水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用足量浓硫酸完全吸收,浓硫酸增重的质量如图.分析该图象并回答下列问题:
①写出ab段涉及的化学方程式:
②样品A的成分是
(2)乙实验小组的同学取了数份不同质量的样品B,测定方法与甲组同学大部分相同,不同的是,他们将不同质量的铵盐分别加入到50.00mL NaOH溶液中(含8.12g NaOH),测定结果如下:
实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
铵盐的质量(g) | 10.00 | 20.00 | 30.00 | 50.00 |
浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
①分析实验数据可知,实验编号为
②计算B中氮元素的质量分数.
您最近一年使用:0次
2019-06-04更新
|
391次组卷
|
2卷引用:湖南省湘西吉首市丹青中学2019届九年级下学期中考模拟化学试题
试卷分析
整体难度:适中
考查范围:物质的化学变化、身边的化学物质、化学与社会发展、化学实验、物质构成的奥秘
试卷题型(共 26题)
题型
数量
选择题
9
多选题
6
填空与简答
7
实验题
2
计算题
1
综合应用题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.65 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.65 | 铁在氧气中燃烧及其实验 燃烧的定义及条件 燃料充分燃烧的方法及其重要性 常见物质的颜色 | 单选题 |
| 3 | 0.85 | 常用化合价规律 化合价代数和的计算与应用 | 单选题 |
| 6 | 0.65 | 微粒的观点解释现象 原子是化学变化中最小的粒子 | 单选题 |
| 7 | 0.85 | 化合反应 纯净物和混合物的判断 地壳中元素的含量 酸的通性 | 单选题 |
| 8 | 0.65 | 化学性质和物理性质 化学变化与物理变化判断 二氧化碳对生活环境的影响 | 单选题 |
| 9 | 0.65 | 中和反应的实际应用 合理使用化肥和农药 对人体健康危害的物质 某些元素的缺乏症 | 单选题 |
| 13 | 0.85 | 酸的通性 碱的通性 盐类参与的反应 转化为沉淀 | 单选题 |
| 14 | 0.4 | 金属与盐溶液反应 金属活动顺序图像分析 | 单选题 |
| 二、多选题 | |||
| 4 | 0.65 | 纯净物和混合物的判断 有机物定义和常见的有机物 化石燃料的形成及现状 | |
| 5 | 0.65 | 金属与氧气反应 溶解度的相关计算 浓溶液稀释配制一定质量分数溶液 盐类参与的反应 | |
| 10 | 0.4 | 催化剂的概念、性质与用途 制取二氧化碳的装置 二氧化碳与碱的反应及实验 常见的酸碱指示剂及其变色情况 | |
| 11 | 0.65 | 酸的通性 生石灰的性质及用途 常见的酸碱指示剂及其变色情况 盐类参与的反应 | |
| 12 | 0.65 | 饱和溶液和不饱和溶液判断 碱的通性 | |
| 15 | 0.4 | 二氧化碳的检验、验满及净化 二氧化碳与碱的反应及实验 一氧化碳还原氧化铜实验 氢气还原金属氧化物 | |
| 三、填空与简答 | |||
| 16 | 0.4 | 微粒图像的分析及应用 物质的量与微粒数目间的计算 中和反应的概念及微观本质 | 填空题 |
| 17 | 0.65 | 化学方程式的书写 浓硫酸的物理、化学性质 燃料充分燃烧的方法及其重要性 | 科普阅读题 |
| 18 | 0.65 | 金属与酸反应原理 金属活动顺序理解和判断 应用金属活动性解释相关现象 溶液酸碱性及pH相关关系 | 填空题 |
| 19 | 0.65 | 用质量守恒定律确定物质组成 化学方程式的书写 碱的通性 过滤 | 流程题 |
| 20 | 0.65 | 还原剂、氧化剂 二氧化碳的检验、验满及净化 溶液、溶质和溶剂概念 铵根离子的验证 | 填空题 |
| 21 | 0.15 | 化学方程式的书写 不含杂质的化学方程式计算 盐类参与的反应 | 流程题 |
| 22 | 0.65 | 化学方程式的书写 酸的通性 盐类参与的反应 物质推断的综合应用 | 推断题 |
| 四、实验题 | |||
| 23 | 0.65 | 催化剂的概念、性质与用途 根据图像分析结论 操作目的分析 | |
| 24 | 0.4 | 化学方程式的书写 碳单质与某些氧化物的反应 氢气的制备及应用 | |
| 五、计算题 | |||
| 25 | 0.65 | 不含杂质的化学方程式计算 溶质质量分数结合化学方程式的计算 碱的通性 | |
| 六、综合应用题 | |||
| 26 | 0.4 | 不含杂质的化学方程式计算 碱的通性 设计实验探究物质的成分 | |







