2023年江苏省南通市通州区平潮中学中考二模化学试题
江苏
九年级
模拟预测
2023-05-22
169次
整体难度:
适中
考查范围:
化学与社会发展、物质构成的奥秘、身边的化学物质、化学实验、物质的化学变化
一、选择题 添加题型下试题
| A.补充钙元素可以预防儿童佝偻病 | B.焚烧废旧塑料可以防止白色污染 |
| C.不得使用工业盐亚硝酸钠腌制火腿 | D.可用小苏打作油条膨松剂 |
【知识点】 对人体健康危害的物质解读 人体内的常量元素解读
| A.尿素[CO(NH2)2]和硝酸钾都属于复合化肥 | B.铁合金和涤纶都属于合成材料 |
| C.氮、铁是人体必需的微量元素 | D.水银、液氧都属于单质 |
| A.金刚石硬度大,可用于切割玻璃 | B.一氧化碳具有可燃性,可用于冶炼金属 |
| C.铝具有良好的延展性,可用于制防锈漆 | D.浓硫酸具有吸水性,可用作食品干燥剂 |
A.K+、Cl-、Mg2+、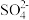 | B.Na+、K+、Cu2+、Cl- |
C. 、Na+、Cl-、 、Na+、Cl-、 | D.Ag+、 、Mg2+、Cl- 、Mg2+、Cl- |
【知识点】 复分解反应发生的条件解读 溶液中物质是否共存相关判断解读

| A.图A是一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 |
| B.图B是高温灼烧一定质量的大理石 |
| C.图C是将等质量的Mg、Fe分别与溶质质量分数相同的足量稀硫酸反应 |
| D.图D是向一定质量的HCl和MgCl2的混合溶液中,逐滴加入NaOH溶液 |
【知识点】 金属与酸反应的图像解读 图像分析溶质质量分数的变化解读
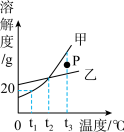
| A.图中P点所表示的溶液是t3℃时甲的饱和溶液 |
| B.可用t1℃时20%的甲溶液配制10%的甲溶液 |
| C.若甲中含有少量乙,可采用冷却热饱和溶液的方法提纯甲 |
| D.分别将t3℃等质量的甲、乙饱和溶液降温至t2℃,所得溶液中溶质质量相等 |
选项 | 物质 | 所选试剂 | 操作方法 |
A | HCl气体(H2O) | 固体氢氧化钠 | 通过装有试剂的干燥管,收集 |
B | CaCl2溶液(HCl) | 碳酸钙粉末 | 加过量试剂,充分反应,过滤 |
C | KNO3溶液(CuSO4) | Ba(OH)2溶液 | 加过量试剂,充分反应,过滤 |
D | CaO固体(CaCl2) | 水 | 加足量试剂,溶解、过滤、蒸发结晶 |
| A.A | B.B | C.C | D.D |
| A.化学与生活 | B.对安全的认识 |
| ①电木插座破裂后,可用加热方法修补 ②用燃烧闻气味的方法区分羊毛和涤纶 ③厨房里可用食醋区分小苏打和食盐 | ①点燃可燃性气体前一定要验纯 ②海鲜食品喷洒甲醛溶液防腐 ③煤矿矿井要保持通风、严禁烟火 |
| C.用“化学”眼光分析 | D.化学实验数据 |
| ①洗涤剂去除油污是因为乳化作用 ②喝汽水打嗝是因为气体溶解度随温度升高而减小 ③成人每天需摄入一定量蛋白质,青少年需要量更大 | ①用10mL量筒量取7.5mL水 ②用托盘天平称量5.6g 铁粉 ③pH试纸测定某浓度盐酸pH为3.6 |
| A.A | B.B | C.C | D.D |

| A.物质X的化学式是Cl |
B.一个Cl原子的质量为 g g |
| C.t时刻,H2和HCl的质量相等 |
| D.反应开始时,物质X的质量为34.5g |
【知识点】 用质量守恒定律确定物质组成解读
二、填空与简答 添加题型下试题
(1)氯化铁、水、铜、C60四种物质中,由分子构成的物质是

(2)图甲中X的值是
(3)图乙所示的化学方程式为
(4)图丙(价类二维图)中,a处物质的化学式为

【知识点】 微粒图像的分析及应用解读 化学式图示的分析解读
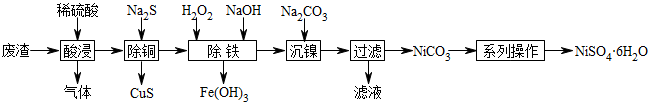
已知:镍(Ni)能与稀硫酸反应生成NiSO4和H2。
(1)“酸浸”时要充分搅拌,其目的是
(2)写出“除铜”时发生复分解反应的化学方程式:
(3)“除铁”加入H2O2溶液的目的是
(4)检验“沉镍”过程中Ni2+已完全沉淀的方法是(含实验操作及实验现象):
(5)“系列操作”主要包括硫酸溶解、
Ⅰ、火是文明的起源,取火的方法,经历了漫长的演变过程。
(1)古代人使用的“火折子”吹气即可燃,“火折子”的制作材料中有硫磺。硫在氧气中燃烧的化学方程式为
(2)1830年,法国人发明了摩擦火柴,将白磷、硫、KClO3、MnO2混合做火柴,摩擦生热使白磷燃烧,利用白磷燃烧的热量使KClO3分解,然后是硫燃烧。该过程中KClO3分解的化学反应方程式为
Ⅱ、化学指导人类合理利用资源
(3)把煤隔绝空气加强热的过程属于
(4)下列关于石油的叙述不正确的是
a.石油是一种化工产品 b.石油是一种混合物
c.可利用石油产品发电 d.将石油分馏可得到多种产品
(5)埋于海底将来可能会替代化石燃料的新能源是
Ⅲ、化学促进科学技术的发展
(6)中国自主研制的新一代战斗机,其中机翼前后缘采用了玻璃纤维增强塑料(玻璃钢),驾驶舱盖和 挡风玻璃采用了丙烯酸酯透明塑料。其中玻璃纤维增强塑料属于
a.金属材料 b.合成材料 c.复合材料
(7)战机材料中还含有锌、铁、铜三种金属,为比较其活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的的有
a.ZnCl2溶液中加入足量铜粉后,再加入铁粉
b.ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液
c.稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
三、科学探究题 添加题型下试题
【容器底部固体成分探究】取出容器底部剩余的固体物质,用水清洗干燥。
| 实验操作 | 实验现象 | 解释与结论 |
| ①用磁铁靠近固体物质甲 | 固体物质不能被吸引 | 固体物质中不含铁单质 |
| ②将固体物质甲放入盐酸中 | 固体消失,溶液变成 | 固体物质主要是氧化铁 |
某研究小组设计如下图所示实验,探究CO2和H2在一定条件下反应的产物。

查阅资料:①CO2和H2在合适催化剂和一定条件下反应转化为CO和H2O;
②无水硫酸铜为白色固体,遇水变蓝。
(1)A装置发生的化学方程式:
(2)不观察B装置中的现象,仅凭C装置中黑色固体变为红色,D装置中澄清石灰水变浑浊,该小组同学认为不能确定CO2和H2已经发生了反应,其理由是
(3)该小组讨论后,认为该实验装置还存在的一个缺陷是
【NaOH溶液与CO2的反应探究】

(4)某小组需要从逸出气体(CO2、H2)中获得一瓶干燥纯净的氢气,用上述装置完成实验,装置的连接顺序为:
(5)装置乙中NaOH溶液发生的化学方程式:
(6)对乙装置反应后溶液中溶质成分做出如下猜测并进行实验:
猜想一:NaOH、Na2CO3猜想二:Na2CO3
实验验证:
| 实验操作 | 实验现象 | 解释与结论 |
| 实验一:取乙装置中反应后的液体,加入过量的BaCl2溶液 | 产生白色沉淀 | 溶质中含有Na2CO3 |
| 实验二:静置、取实验一中反应后的上层清液,滴入酚酞试液 | 溶液变红 | 溶质中含有 |
②下列物质能替代实验二中酚酞溶液,并达到实验目的的是
A.稀盐酸 B.二氧化碳 C.硫酸镁溶液 D.硝酸铜
【知识点】 设计实验探究物质的成分解读 根据现象推测结论 根据现象进行成分推测
四、综合应用题 添加题型下试题
(1)“黑火药”爆炸时发生的主要反应是:S+2KNO3+3C═K2S+3CO2↑+
(2)古代曾用硝土[含有Ca(NO3)2、少量NaCl等]和草木灰(含有K2CO3)作原料制取KNO3。某化学兴趣小组设计了如下实验流程:
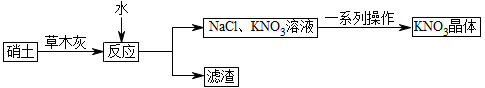
“反应”过程中的化学方程式为
(3)现代国防、开矿等使用的烈性炸药,主要成分为硝化甘油(C3H5O9N3)。硝化甘油在人体内能缓慢氧化生成一种氮的氧化物,用于治疗心绞痛。合成硝化甘油的化学方程式为C3H8O3+3HNO3═C3H5O9N3+3H2O。现用100g质量分数为37.8%硝酸和足量甘油反应,理论上可以生成多少硝化甘油?
试卷分析
试卷题型(共 15题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.65 | 对人体健康危害的物质 人体内的常量元素 | 单选题 |
| 2 | 0.65 | 单质和化合物的判断 常见化肥的种类及性质 人体内的微量元素——碘、铁元素 塑料、合成橡胶、合成纤维 | 单选题 |
| 3 | 0.85 | 金刚石的相关知识 一氧化碳的还原性 金属与氧气反应 浓硫酸做干燥剂 | 单选题 |
| 4 | 0.94 | 过滤操作要点 氢气的物理性质 仪器连接 液体药品的取用 | 单选题 |
| 5 | 0.65 | 复分解反应发生的条件 溶液中物质是否共存相关判断 | 单选题 |
| 6 | 0.65 | 金属与酸反应的图像 图像分析溶质质量分数的变化 | 单选题 |
| 7 | 0.85 | 结晶分离混合物 固体溶解度曲线的应用 溶解度的相关计算 溶质质量分数的涵义 | 单选题 |
| 8 | 0.85 | 生石灰的性质及用途 碱的通性 盐类参与的反应 | 单选题 |
| 9 | 0.4 | 乳化现象及应用 对人体健康危害的物质 羊毛、合成纤维、棉的鉴别 托盘天平的正确使用方法和注意事项 | 单选题 |
| 10 | 0.4 | 用质量守恒定律确定物质组成 | 单选题 |
| 二、填空与简答 | |||
| 11 | 0.4 | 微粒图像的分析及应用 化学式图示的分析 | 填空题 |
| 12 | 0.65 | 复分解反应的定义 过氧化氢制取氧气实验 结晶分离混合物 盐类参与的反应 | 流程题 |
| 13 | 0.85 | 化学变化与物理变化判断 化学方程式的书写 氯酸钾制取氧气 资源综合利用和新能源开发的重要意义 | 填空题 |
| 三、科学探究题 | |||
| 14 | 0.4 | 设计实验探究物质的成分 根据现象推测结论 根据现象进行成分推测 | |
| 四、综合应用题 | |||
| 15 | 0.65 | 根据方程式推测化学式 溶质质量分数结合化学方程式的计算 盐类参与的反应 | |

 倾倒液体
倾倒液体 储存氢气
储存氢气 过滤
过滤 连接仪器
连接仪器

