26. 铜是人类使用最早的金属,铜及铜的化合物在生产、生活中应用广泛。
Ⅰ.对铜制品的认识
(1)深埋于地下的古代青铜器能保存至今的原因除了铜的金属活动性弱,不易生锈外,从金属制品锈蚀的条件分析还可能是
_________。
(2)《吕氏春秋·别类篇》载有“金柔锡柔,合两柔则刚”,表明我们的祖先已认识到铜锡合金与纯铜的
_________不同。
Ⅱ.铜的冶炼
如图1为古法炼铜流程,以孔雀石[主要成分为Cu
2(OH)
2CO
3]和木炭为原料,经高温煅烧,冷却得到块状金属铜。

查阅资料:
① 孔雀石受热分解生成CuO、H
2O和CO
2。
② 铜的熔点为1083.4℃,氧气充足时炭火温度可达1200℃左右。
(3)Cu
2 (OH)
2CO
3受热分解反应的化学方程式是
___________。
(4)冶炼产物是铜块而不是散落在炭粉中的铜颗粒,原因是
_____。
Ⅲ.硫酸铜制取及应用
方案一:
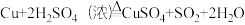
方案二:将废铜屑倒入稀硫酸中,控温80℃并通入氧气制备硫酸铜。
(5)图2是方案二实验室模拟工业制备硫酸铜的装置。反应的化学方程式为
_____。

(6)从绿色化学的观点出发,上述两个方案中,你认为比较合理的是
_____(填“方案一”或“方案二”)。
(7)切割钢板时,通常利用硫酸铜溶液在钢板上先画出红线,该反应的化学方程式为
________。
(8)工业上用含有硫酸铜的微蚀刻废液(含有一定量Cu
2+、H
+、

、H
2O
2和微量Fe
3+)来制备高纯度碱式碳酸铜[Cu
2 (OH)
2CO
3],用于生产木材防腐剂等。其制备过程如图3所示:

① 第二次“沉淀”时的反应为
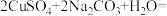
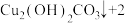 ______
______
。
② 第二次“沉淀”时,若有少量5Cu(OH)
2·2CuCO
3生成,则产品中铜元素的质量分数
_____。(填“偏大”“偏小”或“不变”)
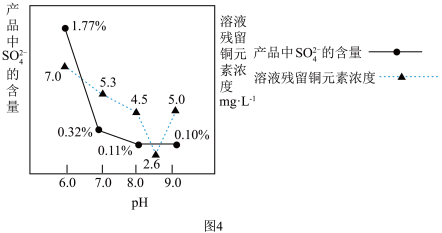
③ 加入Na
2CO
2进行反应时,反应液pH对产品中

的含量以及反应液中Cu
2+沉淀效率的影响如图4所示,此时溶液pH最好控制在
_____。