江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
江苏
九年级
阶段练习
2018-04-04
402次
整体难度:
较易
考查范围:
物质的化学变化、化学与社会发展、身边的化学物质、物质构成的奥秘、化学实验
江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
江苏
九年级
阶段练习
2018-04-04
402次
整体难度:
较易
考查范围:
物质的化学变化、化学与社会发展、身边的化学物质、物质构成的奥秘、化学实验
一、选择题 添加题型下试题
选择题-单选题
|
容易(0.94)
名校
1. 下列过程主要属于化学变化的是
| A.石油分馏 | B.碘的升华 | C.氧气液化 | D.铜器锈蚀 |
【知识点】 化学变化与物理变化判断解读
您最近一年使用:0次
2018-04-03更新
|
114次组卷
|
4卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
容易(0.94)
名校
2. 空气是人类生存所必需的重要资源。下列措施不利于建设“蓝天工程”的是
| A.严禁露天焚烧农作物秸秆 | B.大力推行汽车使用天然气或氢气为燃料 |
| C.加强植树造林,增大绿化面积 | D.生产中加大煤炭和石油等燃料的使用量 |
您最近一年使用:0次
2018-04-03更新
|
64次组卷
|
3卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
您最近一年使用:0次
2018-04-03更新
|
74次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
您最近一年使用:0次
2017-10-24更新
|
150次组卷
|
5卷引用:江苏省常州市武进区2018届九年级中考二模化学试题
选择题-单选题
|
较易(0.85)
名校
5. 下列有关浓硫酸说法中错误的是
| A.浓硫酸具有吸水性,可用于干燥某些气体 |
| B.浓硫酸具有脱水性,可以使纸张碳化 |
| C.浓硫酸具有酸性,可与铜反应生成氢气 |
| D.浓硫酸具有强腐蚀性,使用时要特别小心 |
您最近一年使用:0次
2018-04-03更新
|
272次组卷
|
3卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
容易(0.94)
名校
6. 下图是简易净水器,其中同时具有过滤与吸附作用的是


| A.纱布 | B.石英砂 | C.小卵石 | D.活性炭 |
【知识点】 活性炭的吸附性 简易净水器的构造和各部分的作用解读
您最近一年使用:0次
2018-01-19更新
|
241次组卷
|
12卷引用:湖北省大冶市东片八校2018届九年级上学期联考理综化学试题
湖北省大冶市东片八校2018届九年级上学期联考理综化学试题人教版2018届九年级一轮复习化学专题练习:专题2 水江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题江苏省扬州市竹西中学2018届九年级3月质量检测化学试题(已下线)热点专题3 水的净化-2020年《三步冲刺中考·化学》之热点专题冲刺(通用版)(已下线)【万唯原创】2018年河南省中考化学面对面卷九年级第四单元2020年海南省中考二模化学试题(已下线)【万唯原创】2018年陕西省中考化学面对面卷九年级练习册模块一-主题3(已下线)【万唯原创】2018年山西省中考化学试题研究卷练习册九年级模块一第4讲(已下线)【万唯原创】2018年广东省中考化学试题研究卷九年级练习册第3讲黑龙江省齐齐哈尔市铁锋区2021-2022学年九年级上学期期中模拟化学试题1贵州省遵义市绥阳县2023-2024学年九年级上学期期中化学试题
选择题-单选题
|
较易(0.85)
名校
7. 已知 2NaClO3+H2SO4+SO2===2X+2NaHSO4 由此可知X物质的化学式为
| A.NaCl | B.ClO2 | C.NaClO | D.Cl2O |
【知识点】 根据方程式推测化学式解读
您最近一年使用:0次
2018-04-03更新
|
92次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
容易(0.94)
名校
您最近一年使用:0次
2018-04-03更新
|
91次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
9. 下列有关实验现象的描述中,正确的是
| A.加热碱式碳酸铜,绿色粉末逐渐变黑,试管口有小水滴 |
| B.细铁丝在氧气中燃烧,火星四射,生成红棕色固体 |
| C.镁条在空气中燃烧,产生黑烟,生成白色粉末 |
| D.少量氧化铜中加入稀硫酸,有气泡产生,黑色粉末逐渐消失,溶液变蓝 |
您最近一年使用:0次
2018-04-03更新
|
59次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
10. 下列措施是为了降低化学反应速率的是
| A.食品放在冰箱中贮藏 |
| B.双氧水制氧气时加入少量二氧化锰 |
| C.试管中进行氧化铜与稀硫酸反应时,稍微加热 |
| D.铁粉代替铁钉与稀硫酸反应制取氢气 |
您最近一年使用:0次
2018-04-03更新
|
55次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
您最近一年使用:0次
2018-04-03更新
|
105次组卷
|
4卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
12. 下列常见物质的俗名与化学式对应正确的是
| A.烧碱 Na2CO3 | B.小苏打 NaHCO3 | C.熟石灰CaO | D.铜绿CuSO4·5H2O |
【知识点】 常见酸、碱的俗称及化学式解读 碳酸氢钠、碳酸钠、碳酸钙解读
您最近一年使用:0次
2018-04-03更新
|
77次组卷
|
3卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
13. 钛(Ti)合金板常用于大型建筑,已知钛原子核内有22个质子,则下列叙述中错误的是
| A.每个TiO2分子中含有一个氧分子 | B.Ti可以表示一个钛原子 |
| C.Ti原子的核外有22个电子 | D.TiO2属于金属氧化物 |
您最近一年使用:0次
2018-04-03更新
|
69次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
14. 维生素B9也叫叶酸,其化学式为C19H19N7O6。下列有关叶酸的说法中正确的是
| A.叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成 |
| B.叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6 |
| C.叶酸中氮元素的质量分数大于氧元素的质量分数 |
| D.叶酸的相对分子质量为441g |
您最近一年使用:0次
2018-04-03更新
|
106次组卷
|
4卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
适中(0.65)
名校
15. A、B两种固体物质的溶解度曲线如图所示,下列说法正确的是


| A.A物质的溶解度大于B物质; |
| B.t1℃时,A、B饱和溶液溶质质量分数都为25% |
| C.t2℃时A、B的饱和溶液降温至t1℃,所得溶液溶质质量分数相等 |
| D.t2℃时,用等质量的A、B分别配制成饱和溶液,所得溶液质量A<B; |
您最近一年使用:0次
2018-04-03更新
|
116次组卷
|
3卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
16. 下列说法中不属于大气污染治理措施的是
| A.外出时使用PM2.5口罩,减少有害物质的吸入 |
| B.改燃煤为燃气,可减少废气中SO2等有害物质的量 |
| C.利用太阳能、潮汐能、风力发电,以获取清洁能源 |
| D.煤炭燃烧后的烟气,经石灰浆处理后再排放 |
您最近一年使用:0次
2018-04-03更新
|
53次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
适中(0.65)
名校
17. 下列各组离子在无色透明溶液中能大量共存的是
| A.Cu2+、Na+、SO42-、Cl- | B.K+、Na+、CO32—、NO3- |
| C.OH-、CO32-、Ca2+、Na+ | D.Mg2+、Na+、OH-、CO32- |
您最近一年使用:0次
2018-04-03更新
|
159次组卷
|
3卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
较易(0.85)
名校
18. 实验室可用下图发生装置制取H2 ,下列说法错误的是


| A.关闭活塞,通过向长颈漏斗中加水可检查该装置的气密性 |
| B.若用浓盐酸代替稀硫酸可使制得的氢气纯度更高 |
| C.旋转活塞可以控制反应的发生和停止 |
| D.因导管口有活塞,故长颈漏斗下端可不必伸入液面以下 |
您最近一年使用:0次
2018-04-03更新
|
105次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
选择题-单选题
|
适中(0.65)
19. 除去下列物质中含有的杂质,所选用试剂和方法错误的是
| 物质 | 杂质 | 所加试剂 | 主要方法 | |
| A | H2O | 悬浮物 | 明矾 | 吸附 |
| B | NaNO3溶液 | NaCl | 过量AgNO3溶液 | 过滤 |
| C | CO | CO2 | NaOH溶液 | 干燥 |
| D | Ag | Fe | 稀盐酸 | 过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-09-14更新
|
146次组卷
|
6卷引用:四川省巴中市2017年中考化学试题
四川省巴中市2017年中考化学试题江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题(已下线)【中考考点总动员】-考点10 盐和化肥江苏省东台和盐都2018届九年级第二次模拟检测化学试题(已下线)【万唯原创】2018年安徽省中考化学面对面卷练习册九年级选择题分类集训命题点92020年甘肃省天水市甘谷县中考二模化学试题
选择题-单选题
|
较难(0.4)
名校
20. 有一包粉末,已知由BaSO4、FeCl3、Ba(NO3)2、Na2SO4、NaOH、NaCl中的几种组成。为了确定其成分,现进行以下实验,各步骤均已充分反应。
步骤一:取一定质量的粉末,加水搅拌后过滤,得到有色沉淀甲和无色溶液A;
步骤二:向步骤一的沉淀甲中加入足量稀盐酸,固体全部消失并得到黄色溶液;
步骤三:将步骤一得到的无色溶液A进行如下图所示的实验。
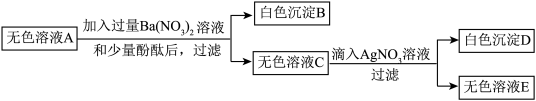
则下列说法中正确的是:
步骤一:取一定质量的粉末,加水搅拌后过滤,得到有色沉淀甲和无色溶液A;
步骤二:向步骤一的沉淀甲中加入足量稀盐酸,固体全部消失并得到黄色溶液;
步骤三:将步骤一得到的无色溶液A进行如下图所示的实验。

则下列说法中正确的是:
| A.原白色粉末中一定有FeCl3、Na2SO4、NaOH |
| B.有色沉淀甲可能是Fe(OH)3和BaSO4 的混合物 |
| C.若将步骤二中的盐酸换成硝酸,则可确定原白色粉末是否含有NaCl |
| D.原白色粉末中FeCl3和NaOH的质量比为65:48 |
【知识点】 盐类参与的反应解读 设计实验探究物质的成分解读
您最近一年使用:0次
2018-04-03更新
|
149次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
二、填空与简答 添加题型下试题
填空与简答-填空题
|
较易(0.85)
名校
21. 化学用语是学习化学的重要工具
(1)按要求写出相应的化学符号
①碳原子_____ ②空气中最多的气体_______ ③锌离子______ ④两个碳酸根离子______
⑤缺少后会导致骨质疏松的元素_________ ⑥“西气东输”中的“气”是_______
(2)按要求写出相应的化学方程式,并注明反应的基本类型
①铝在空气中形成致密的保护膜________________________ ,反应类型____________
②用氢氧化镁治疗胃酸过多_______________________ ,反应类型____________
③水在通电条件下分解________________________ ,反应类型____________
④用锌与稀硫酸反应制取氢气________________________ ,反应类型____________
(1)按要求写出相应的化学符号
①碳原子
⑤缺少后会导致骨质疏松的元素
(2)按要求写出相应的化学方程式,并注明反应的基本类型
①铝在空气中形成致密的保护膜
②用氢氧化镁治疗胃酸过多
③水在通电条件下分解
④用锌与稀硫酸反应制取氢气
您最近一年使用:0次
2018-04-03更新
|
68次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
填空与简答-填空题
|
适中(0.65)
名校
22. 化学与生活密切相关。
Ⅰ.在“①稀硫酸、②水、③熟石灰、④酒精、⑤氯化钾、⑥铁粉”中,请选择适当物质的序号 填空:
(1)用于改良酸性土壤的是____________ , (2)用于清除铁锈的是_________ ,
(3)实验室常用的液体燃料是____________ , (4)最常见的溶剂____________ ,
(5)用于防止食物变质的双吸剂____________ , (6)可作钾肥的是____________ 。
Ⅱ.合现有下列五种物质A. 食盐 B. 小苏打 C. 苹果 D. 葡萄糖 E. 维生素A
请按下列要求填空(填序号)。
富含维生素C的是___________ ;可直接进入血液,补充能量的是 ________ ;既可作为疏松剂,又可治疗胃酸过多的是 ________ ;食用过多会引起血压升高的 ________ ;夜盲症患者可以在医生的指导下补充大量 ________ 进行治疗。
Ⅲ.材料是人类生产和生活的物质基础,合理使用材料可以改善我们的生活。
(1)钢铁的生产与使用是人类文明和生活进步的一个重要标志。
①工业上用赤铁矿炼铁的主要化学反应方程式:_______________________________ ,实验室完成此实验是要注意先 ____________ 再 ___________ ,目的是为了 _____________ 。
②我们还可以采用湿法冶金获得金属,请写出铁与硫酸铜溶液反应的化学方程式:______________ 。
③ 炒过菜的铁锅未及时洗净擦干,第二天便会因腐蚀出现红褐色锈斑。铁锅的腐蚀主要是铁与_______ 和 _______ 反应造成,铁锈的主要成分是 ________ 。为防止铁制品锈蚀,可采取的方法有 _____________ (只需填写一种即可)。
(2) 体育场馆建设需大量建筑材料。下列材料属于复合材料的是________ (填字母) ,属于合成材料的是 ________ (填字母)。
a. 石灰石 b. 玻璃钢 c. 玻璃 d 钢筋混凝土 e 聚氯乙烯塑料
Ⅳ.化学的发展为人类解决能源危机带来了曙光。
(1)化学电池是一种高效利用能源的装置,电池在使用时将_______ 能转化为_______ 能
(2)下图是某电池的内部结构示意图,

①其中正极为_______ ,负极为_______ 。
②请写出用二氧化锰和双氧水混合制取氧气的化学方程式__________________ 。
③电池材料中的糊状电解质中含有淀粉,我们可以用________ (填试剂名称)来检验,检验时课观察到__________________ 。
④电解液中的氯化铵,再农业生产中可做______ 肥,施用时要注意__________________ 。
Ⅰ.在“①稀硫酸、②水、③熟石灰、④酒精、⑤氯化钾、⑥铁粉”中,请选择适当物质的
(1)用于改良酸性土壤的是
(3)实验室常用的液体燃料是
(5)用于防止食物变质的双吸剂
Ⅱ.合现有下列五种物质A. 食盐 B. 小苏打 C. 苹果 D. 葡萄糖 E. 维生素A
请按下列要求填空(填序号)。
富含维生素C的是
Ⅲ.材料是人类生产和生活的物质基础,合理使用材料可以改善我们的生活。
(1)钢铁的生产与使用是人类文明和生活进步的一个重要标志。
①工业上用赤铁矿炼铁的主要化学反应方程式:
②我们还可以采用湿法冶金获得金属,请写出铁与硫酸铜溶液反应的化学方程式:
③ 炒过菜的铁锅未及时洗净擦干,第二天便会因腐蚀出现红褐色锈斑。铁锅的腐蚀主要是铁与
(2) 体育场馆建设需大量建筑材料。下列材料属于复合材料的是
a. 石灰石 b. 玻璃钢 c. 玻璃 d 钢筋混凝土 e 聚氯乙烯塑料
Ⅳ.化学的发展为人类解决能源危机带来了曙光。
(1)化学电池是一种高效利用能源的装置,电池在使用时将
(2)下图是某电池的内部结构示意图,

①其中正极为
②请写出用二氧化锰和双氧水混合制取氧气的化学方程式
③电池材料中的糊状电解质中含有淀粉,我们可以用
④电解液中的氯化铵,再农业生产中可做
您最近一年使用:0次
2018-04-03更新
|
84次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
三、科学探究题 添加题型下试题
科学探究题
|
较易(0.85)
名校
23. 某同学逛超市时发现食品添加剂中有“碳酸氢铵”,感觉很惊讶,“碳酸氢铵”是臭粉啊,怎么可以放进食品?于是开展了以下探究,请你帮助完成下列相关问题。
(1)查阅资料:
①食用级碳酸氢铵比较纯净,可作膨松剂,一般用在油炸食品中,水蒸食品中不用;
②常温常压下,1体积水约能溶解600体积氨气,其水溶液呈弱碱性。
③碱石灰是氧化钙和氢氧化钠的混合物。
(2)产生疑惑:臭粉为何可以作膨松剂?为何一般适用于油炸食品而不适用于水蒸食品?

(3)实验设计:实验装置如图,图一是检验装置,图二是收集装置,取适量碳酸氢铵分别置于两试管中,按如图进行实验。
(4)现象与分析:
①图一:B中现象是_________________ ,C中发生反应的化学方程式是 _______________ 。
②图三:装置E的作用是_________________ ,用F装置收集氨气,说明氨气具有_________________ 性质,取下F,塞紧橡皮塞,用注射器向F中注入少量水,振荡,可看到的现象是_________________ ,拔出橡皮塞闻到氨味。
(5)解释与结论:①有臭味的碳酸氢铵添加到食品中,如果油炸,则含有的少量碳酸氢铵受热时完全分解,产生的气体使食品膨胀,且生成物可以迅速挥发而离开食品,没有残留物,其臭味会消失,碳酸氢铵受热发生反应的化学方程式是_________________ ②添加碳酸氢铵的食品如果水蒸,则 _________________ 。
通过上述探究该明白了:高纯度的碳酸氢铵可以作为食品添加剂,但同一食品添加剂并不适合所有食品,使用食品添加剂需严格控制用量。
(1)查阅资料:
①食用级碳酸氢铵比较纯净,可作膨松剂,一般用在油炸食品中,水蒸食品中不用;
②常温常压下,1体积水约能溶解600体积氨气,其水溶液呈弱碱性。
③碱石灰是氧化钙和氢氧化钠的混合物。
(2)产生疑惑:臭粉为何可以作膨松剂?为何一般适用于油炸食品而不适用于水蒸食品?

(3)实验设计:实验装置如图,图一是检验装置,图二是收集装置,取适量碳酸氢铵分别置于两试管中,按如图进行实验。
(4)现象与分析:
①图一:B中现象是
②图三:装置E的作用是
(5)解释与结论:①有臭味的碳酸氢铵添加到食品中,如果油炸,则含有的少量碳酸氢铵受热时完全分解,产生的气体使食品膨胀,且生成物可以迅速挥发而离开食品,没有残留物,其臭味会消失,碳酸氢铵受热发生反应的化学方程式是
通过上述探究该明白了:高纯度的碳酸氢铵可以作为食品添加剂,但同一食品添加剂并不适合所有食品,使用食品添加剂需严格控制用量。
您最近一年使用:0次
科学探究题
|
适中(0.65)
名校
24. 过氧化钙晶体(化学式为:CaO2·yH2O,化学式中的“yH2O”称为结晶水),常温该晶体下为白色,能溶于酸,难溶于水、乙醇,是一种温和的氧化剂,常用于鱼类长途运输的增氧剂等。
(1) 过氧化钙晶体可用下列方法制备:
CaCl2+H2O2+NH3+H2O CaO2·yH2O↓+NH4Cl。
CaO2·yH2O↓+NH4Cl。
用如下制取装置制备过氧化钙晶体。

①装置A中生成的气体为________ ,此装置在初中化学实验中可用于制取_______ (填某气体);仪器X的名称为________ 。
②装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ. 该反应是放热反应,温度低有利于提高CaO2·yH2O产率;
Ⅱ.____________________________
③反应结束后,经过滤、洗涤、低温烘干可获得CaO2·yH2O。检验晶体已洗涤干净的方法为:取最后一次洗涤液,滴加____________ ,若__________ ,则晶体已经洗涤干净。
(2)为确定过氧化钙晶体的组成,某化学兴趣小组称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水),根据下图可知y=_______ , 350℃时发生的分解反应方程式为_______________ 。

(1) 过氧化钙晶体可用下列方法制备:
CaCl2+H2O2+NH3+H2O
 CaO2·yH2O↓+NH4Cl。
CaO2·yH2O↓+NH4Cl。用如下制取装置制备过氧化钙晶体。

①装置A中生成的气体为
②装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ. 该反应是放热反应,温度低有利于提高CaO2·yH2O产率;
Ⅱ.
③反应结束后,经过滤、洗涤、低温烘干可获得CaO2·yH2O。检验晶体已洗涤干净的方法为:取最后一次洗涤液,滴加
(2)为确定过氧化钙晶体的组成,某化学兴趣小组称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水),根据下图可知y=

【知识点】 不含杂质的化学方程式计算解读 设计实验探究物质的成分解读
您最近一年使用:0次
2018-04-03更新
|
127次组卷
|
2卷引用:江苏省扬州市竹西中学2018届九年级下学期第一次月考化学试题
试卷分析
整体难度:较易
考查范围:物质的化学变化、化学与社会发展、身边的化学物质、物质构成的奥秘、化学实验
试卷题型(共 24题)
题型
数量
选择题
20
填空与简答
2
科学探究题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.94 | 空气污染及其保护 | 单选题 |
| 3 | 0.85 | 盐的组成及分类 | 单选题 |
| 4 | 0.85 | 置换反应 | 单选题 |
| 5 | 0.85 | 应用金属活动性解释相关现象 浓硫酸的物理、化学性质 浓硫酸做干燥剂 | 单选题 |
| 6 | 0.94 | 活性炭的吸附性 简易净水器的构造和各部分的作用 | 单选题 |
| 7 | 0.85 | 根据方程式推测化学式 | 单选题 |
| 8 | 0.94 | 化学发展史 | 单选题 |
| 9 | 0.85 | 铁在氧气中燃烧及其实验 酸的通性 盐类参与的反应 镁在氧气中燃烧及其实验 | 单选题 |
| 10 | 0.85 | 催化剂的概念、性质与用途 金属与酸反应原理 酸的通性 | 单选题 |
| 11 | 0.85 | 化学式书写及读法 | 单选题 |
| 12 | 0.85 | 常见酸、碱的俗称及化学式 碳酸氢钠、碳酸钠、碳酸钙 | 单选题 |
| 13 | 0.85 | 氧化物的定义 氧化物的定义 原子中各类微粒的数值关系 原子中各类微粒的数值关系 元素符号书写及含义 元素符号书写及含义 化学式、分子式及涵义 化学式、分子式及涵义 | 单选题 |
| 14 | 0.85 | 化学式、分子式及涵义 根据化学式计算相对分子质量 根据化学式计算元素质量比 根据化学式计算元素质量分数 | 单选题 |
| 15 | 0.65 | 固体溶解度曲线的应用 固体溶解度的影响因素 溶解度的相关计算 | 单选题 |
| 16 | 0.85 | 空气污染及其保护 | 单选题 |
| 17 | 0.65 | 复分解反应发生的条件 常见酸碱盐的溶解性 溶液中物质是否共存相关判断 | 单选题 |
| 18 | 0.85 | 金属与酸反应原理 气体发生、收集装置 | 单选题 |
| 19 | 0.65 | 金属与酸反应原理 自来水厂净化过程 盐类参与的反应 除杂 | 单选题 |
| 20 | 0.4 | 盐类参与的反应 设计实验探究物质的成分 | 单选题 |
| 二、填空与简答 | |||
| 21 | 0.85 | 化学方程式的书写 化学式书写及读法 | 填空题 |
| 22 | 0.65 | 化学方程式的书写 中和反应的实际应用 合理使用化肥和农药 常见物品质材的辨别 | 填空题 |
| 三、科学探究题 | |||
| 23 | 0.85 | 化学方程式的书写 常见的酸碱指示剂及其变色情况 盐类参与的反应 | |
| 24 | 0.65 | 不含杂质的化学方程式计算 设计实验探究物质的成分 | |




